Clear Sky Science · de
Ein Ensemble-Machine-Learning-Klassifikator zur Diagnose der Parkinson-Krankheit mittels optischer Kohärenztomographie-Angiographie
Warum die Augen verborgene Hirnkrankheiten offenbaren können
Die Parkinson-Krankheit wird in der Regel erst diagnostiziert, nachdem Zittern, Steifheit oder verlangsamte Bewegungen auftreten — Anzeichen dafür, dass sich das Gehirn bereits über Jahre verändert hat. Diese Studie untersucht eine unerwartete Abkürzung: winzige Blutgefäße im hinteren Augenbereich mit einem schmerzfreien Bildgebungsverfahren zu betrachten und dann künstliche Intelligenz zu nutzen, um Menschen zu identifizieren, die möglicherweise früher und objektiver Parkinson haben als es heutige Untersuchungen erlauben.
Das Gehirn durch das Auge betrachten
Das lichtempfindliche Gewebe im hinteren Teil des Auges, die Netzhaut, ist im Grunde ein zugänglicher Teil des Gehirns. Sie teilt ähnliche Nerven und Blutgefäße, kann aber nichtinvasiv in der Klinik untersucht werden. Die Forschenden verwendeten eine Technologie namens optische Kohärenztomographie-Angiographie (OCTA), die detaillierte, farbstofffreie Karten der retinalen Durchblutung liefert. Da Parkinson mit Problemen in kleinen Blutgefäßen an anderen Stellen des Körpers in Verbindung gebracht wurde, fragten sie, ob subtile Veränderungen in diesen retinalen Netzwerken als „Fenster“ zur frühen Erkrankung dienen könnten.
Augenscans in Zahlen überführen
In einer retrospektiven Studie sammelte das Team OCTA-Scans von 53 Personen mit Parkinson und 39 gesunden, altersangepassten Freiwilligen. Sie konzentrierten sich auf zwei Schichten retinaler Gefäße: eine oberflächliche Schicht nahe der Oberfläche und eine tiefere darunter. Aus jeder Schicht segmentierten sie automatisch die zentrale foveale avaskuläre Zone — die winzige, gefäßfreie Vertiefung, die für scharfes Sehen nötig ist — sowie die umliegenden Kapillaren. Anschließend wandelten sie jedes Bild in 22 numerische Messgrößen um. Einige beschrieben die Form der fovealen Zone, beispielsweise wie rund, glatt oder unregelmäßig ihr Rand war. Andere erfassten die Dichte der Blutgefäße insgesamt und in einem Ring um die Fovea. Zusammen quantifizierten diese Messwerte die mikrovaskuläre Gesundheit mit weit mehr Nuancen, als ein menschliches Auge beurteilen könnte. 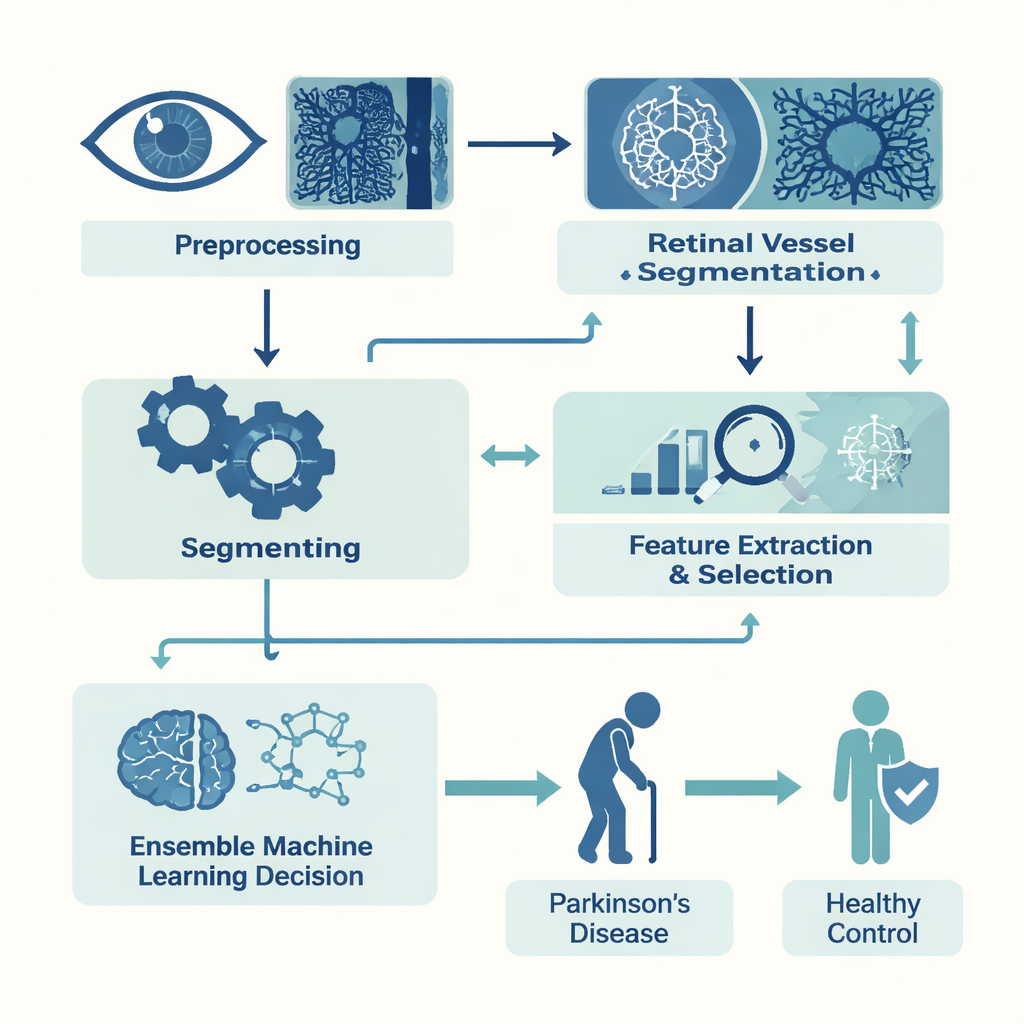
Eine KI trainieren, Parkinson-Muster zu erkennen
Mit diesen Messwerten bauten die Forschenden Computermodelle, um Parkinson-Scans von gesunden zu unterscheiden. Da ihr Datensatz überschaubar war, nutzten sie zunächst Feature-Selection-Techniken, um die 22 Messgrößen auf die informativste Teilmenge zu reduzieren und damit Rauschen und Overfitting zu verringern. Anschließend trainierten sie mehrere gängige Machine-Learning-Algorithmen, darunter baumbasierte Entscheidungsmodelle und einen k-Nearest-Neighbors-Klassifikator. Schließlich kombinierten sie die drei stärksten Performer — XGBoost, Random Forest und K-Nearest Neighbors — zu einem gewichteten „Ensemble“, sodass jede Modellstimme entsprechend ihrer durchschnittlichen Leistungsfähigkeit zählte.
Was die Modelle in der Netzhaut fanden
Im Vergleich zu gesunden Freiwilligen zeigten Personen mit Parkinson eindeutige Hinweise auf veränderte retinale Mikrozirkulation. Messwerte der Gefäßdichte lagen niedriger, und die zentrale foveale Zone war tendenziell weniger regelmäßig in der Form — weniger rund, weniger glatt und weniger kompakt — in beiden Gefäßschichten, oberflächlich und tief. Bei Tests mit zuvor ungesehenen Daten klassifizierte das Ensemble-Modell etwa drei von vier Augen korrekt. Besonders auffällig war eine Sensitivität von 90 %: Neun von zehn Parkinson-Fällen wurden korrekt erkannt. Die Spezifität war moderater, etwas über der Hälfte, was bedeutet, dass einige gesunde Personen fälschlich als erkrankt eingestuft wurden. Die Fläche unter der Receiver-Operating-Characteristic-Kurve (AUC), eine übliche Zusammenfassung der diagnostischen Leistung, lag bei 0,75 und deutet auf eine nützliche, aber nicht definitive Unterscheidung hin. 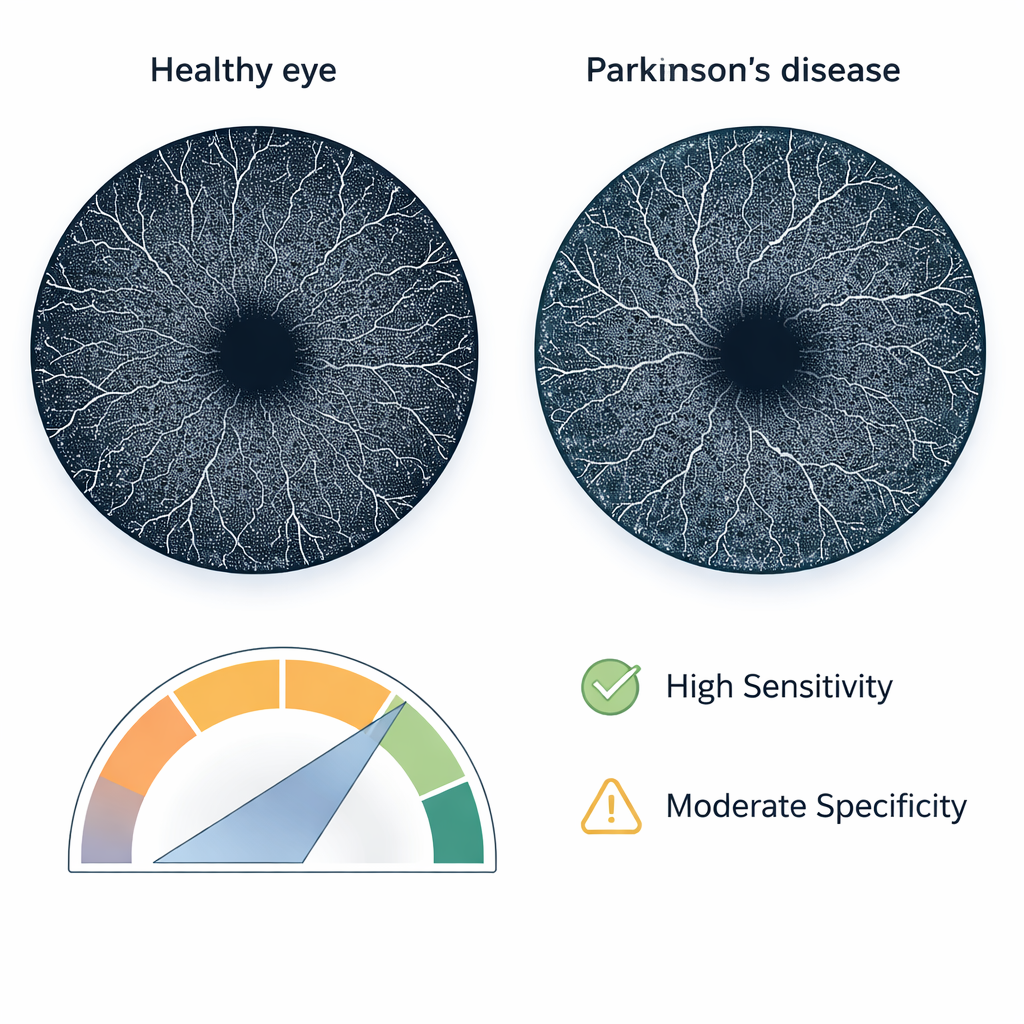
Vom Algorithmus zur Klinik
Um über die Theorie hinauszukommen, verpackte das Team seine Methoden in ein Prototyp-Softwarewerkzeug namens Parkinson’s Disease Artificial Intelligence (PDAI). Über eine einfache grafische Oberfläche können Kliniker OCTA-Scans laden, die automatisch nachgezeichneten Blutgefäße und die zentrale foveale Zone prüfen, die wichtigsten numerischen Merkmale einsehen und eine sofortige Vorhersage erhalten, ob ein Scan denen von Parkinson-Patienten ähnelt. Da das System auf handverlesenen, klar definierten Messgrößen basiert und nicht auf einer undurchsichtigen "Black Box", sind die Beiträge zu jeder Entscheidung für Kliniker leichter interpretierbar und potenziell mit zugrunde liegender Biologie in Beziehung zu setzen.
Was das für Patienten bedeutet
Diese Arbeit bietet noch keinen eigenständigen Test für Parkinson, zeigt aber, dass ein schneller, nichtinvasiver Augenscan, analysiert mit sorgfältig gestalteten Machine-Learning-Methoden, krankheitsbedingte Veränderungen mit hoher Sensitivität erfassen kann. In der Praxis könnte ein solches Werkzeug eines Tages als Screening-Hilfe dienen — Augenärzten und Neurologen dabei helfen zu entscheiden, wer näher überwacht oder frühzeitig zur weiteren Abklärung überwiesen werden sollte, lange bevor beeinträchtigende Symptome auftreten. Größere, multizentrische Studien sind weiterhin erforderlich, doch die Studie legt nahe, dass die Augen tatsächlich ein praktikables Frühwarnsignal für die Parkinson-Krankheit liefern könnten.
Zitation: Hasanshahi, M., Mehdizadeh, A., Mahmoudi, T. et al. An ensemble machine learning classifier for Parkinson’s disease diagnosis using optical coherence tomography angiography. Sci Rep 16, 7297 (2026). https://doi.org/10.1038/s41598-026-38407-9
Schlüsselwörter: Parkinson-Krankheit, Retinalbildgebung, OCTA, Machine Learning, Früherkennung