Clear Sky Science · de
Prognosemodell auf Basis maschinellen Lernens zu Stammzell‑ähnlichkeit und angiogenese‑bezogenen Genen zur Vorhersage von Prognose und Immuninfiltration bei Patienten mit HCC
Warum diese Forschung für Leberkrebspatienten wichtig ist
Das hepatozelluläre Karzinom, die häufigste Form von Leberkrebs, tritt auch nach Behandlung oft erneut auf oder streut. Diese Studie untersucht, warum das geschieht und wie Ärzte besser vorhersagen können, welche Patienten das höchste Risiko tragen. Durch die Kombination großer Genomdatenbestände mit modernen Methoden des maschinellen Lernens entwickelten die Forschenden ein Werkzeug, das zwei einflussreiche Krebs‑Eigenschaften verbindet – „Stammzell‑ähnlichkeit“ (Zellen, die sich wie hartnäckige Samen verhalten) und Neubildung von Blutgefäßen – und diese mit Überlebenschancen sowie der wahrscheinlichen Reaktion auf immunbasierte Therapien verknüpft.
Krebs‑„Saatzellen“ und neue Blutgefäße
Viele Tumoren enthalten eine kleine Gruppe von Zellen, die wie Samen agieren. Diese Krebsstammzellen können sich selbst erneuern, Therapien widerstehen und den Tumor nach Operation oder Chemotherapie wieder anstoßen. Gleichzeitig müssen Tumoren neue Blutgefäße bilden, um Sauerstoff und Nährstoffe zu erhalten, damit sie wachsen und sich ausbreiten können. Neuere Arbeiten zeigen, dass diese beiden Prozesse miteinander verflochten sind: stammzellähnliche Krebszellen geben Signale ab, die das Gefäßwachstum fördern, während die gefäßreiche Umgebung diesen Saatzellen das Überleben erleichtert. Das Verständnis und die gleichzeitige gezielte Bekämpfung dieser Wechselwirkung ist besonders wichtig beim Leberkrebs, der stark vaskularisiert ist und zu Rückfällen neigt.
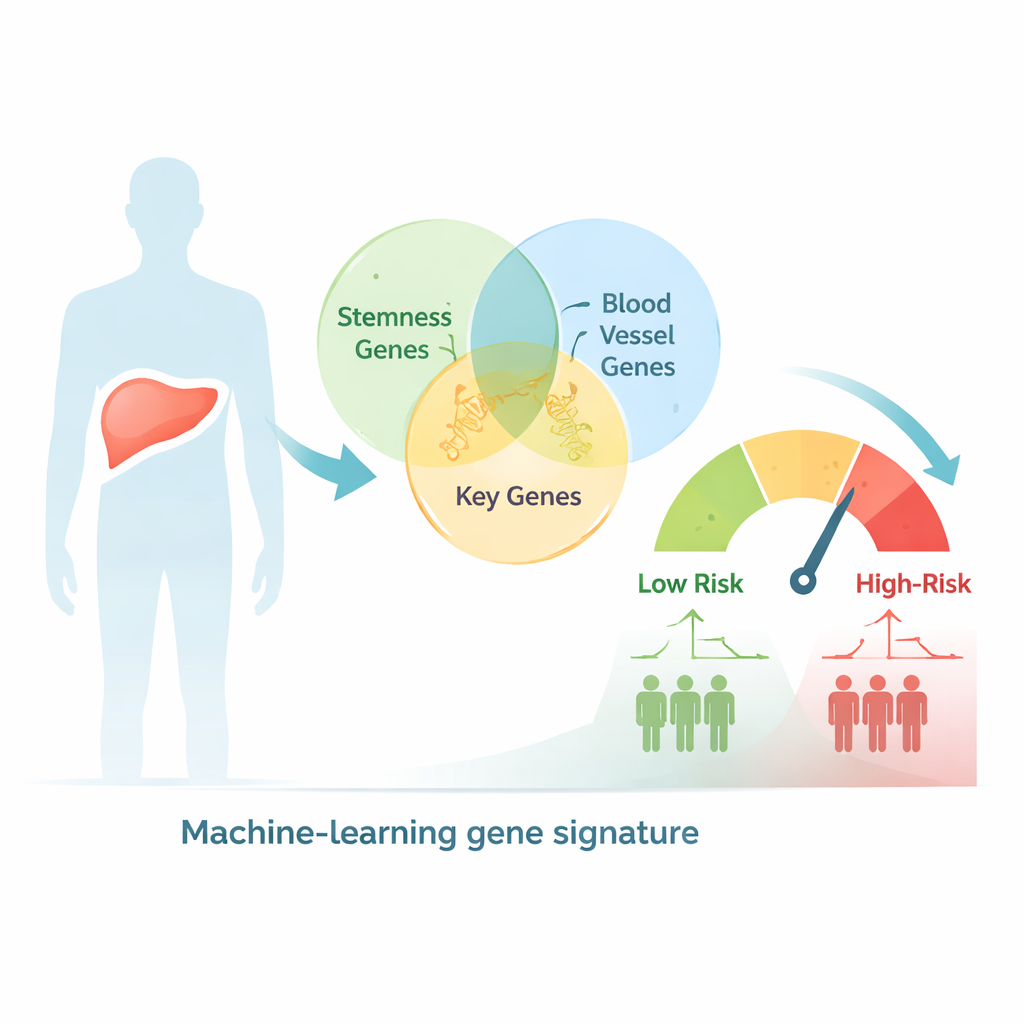
Mit Big Data Patienten nach Risiko sortieren
Die Forschenden begannen mit der Suche in einer großen Datenbank menschlicher Gene nach Genen, die sowohl mit stammzellähnlichem Verhalten als auch mit Gefäßbildung verknüpft sind, und identifizierten mehr als 2.600 überlappende Kandidaten. Anschließend untersuchten sie Leberkrebsproben hunderter Patienten, deren Tumor‑Genaktivität und klinische Verläufe in öffentlichen Krebsdatenbanken erfasst waren. Mit statistischen Tests und Clustering‑Methoden gruppierten sie die Patienten in zwei genetische Subtypen, die deutliche Unterschiede in Stadium, Tumorgröße und Überleben zeigten, was darauf hindeutet, dass kombinierte Stammzell‑ und gefäßbezogene Signale aussagekräftige biologische Informationen in dieser Erkrankung widerspiegeln.
Aufbau eines Neun‑Gen‑Risikoscores
Aus diesem großen Genpool verwendete das Team einen maschinellen Lernansatz, um auf nur neun Schlüsselgene zu reduzieren, deren kombinierte Aktivität am besten vorhersagte, wie lange Patienten überlebten. Diese neun Gene dienten zur Berechnung eines Risikoscores für jede Person. Patienten mit hohem Score hatten eine signifikant kürzere Gesamtüberlebenszeit, sowohl im ursprünglichen Datensatz als auch in einer unabhängigen Kohorte von Leberkrebspatienten zur Validierung. Die Genauigkeit des Modells war konkurrenzfähig mit oder besser als viele bestehende Instrumente, und wenn der Score mit einfachen klinischen Informationen wie dem Tumorstadium in einem sogenannten Nomogramm kombiniert wurde, verbesserte sich die Vorhersage des Überlebens für 1, 3 und 5 Jahre weiter.
Verbindungen zum Immunsystem und zur Therapieansprechbarkeit
Das Team untersuchte außerdem, was der Neun‑Gen‑Score über das Immummilieu des Tumors aussagt. Niedrigrisiko‑Tumoren zeigten tendenziell ein stärkeres „Entzündungsbild“, mit höheren Spiegeln verschiedener Immunzellen und stärkeren Aktivitätssignalen von Angriffspfaden. Hochrisiko‑Tumoren dagegen wiesen Muster auf, die mit Immunflucht und höheren Mutationsraten in wichtigen Genen wie TP53 vereinbar sind. Anhand etablierter computergestützter Tools, die abschätzen, wie Tumoren auf moderne Immuntherapien reagieren könnten, deutete die Studie darauf hin, dass Niedrigrisiko‑Patienten besser auf Checkpoint‑Inhibitoren ansprechen könnten als Hochrisiko‑Patienten. Obwohl diese Prognosen noch in realen Behandlungsszenarien geprüft werden müssen, weisen sie auf eine praktische Möglichkeit hin, Patienten zu identifizieren, die von solchen Medikamenten am meisten profitieren könnten.
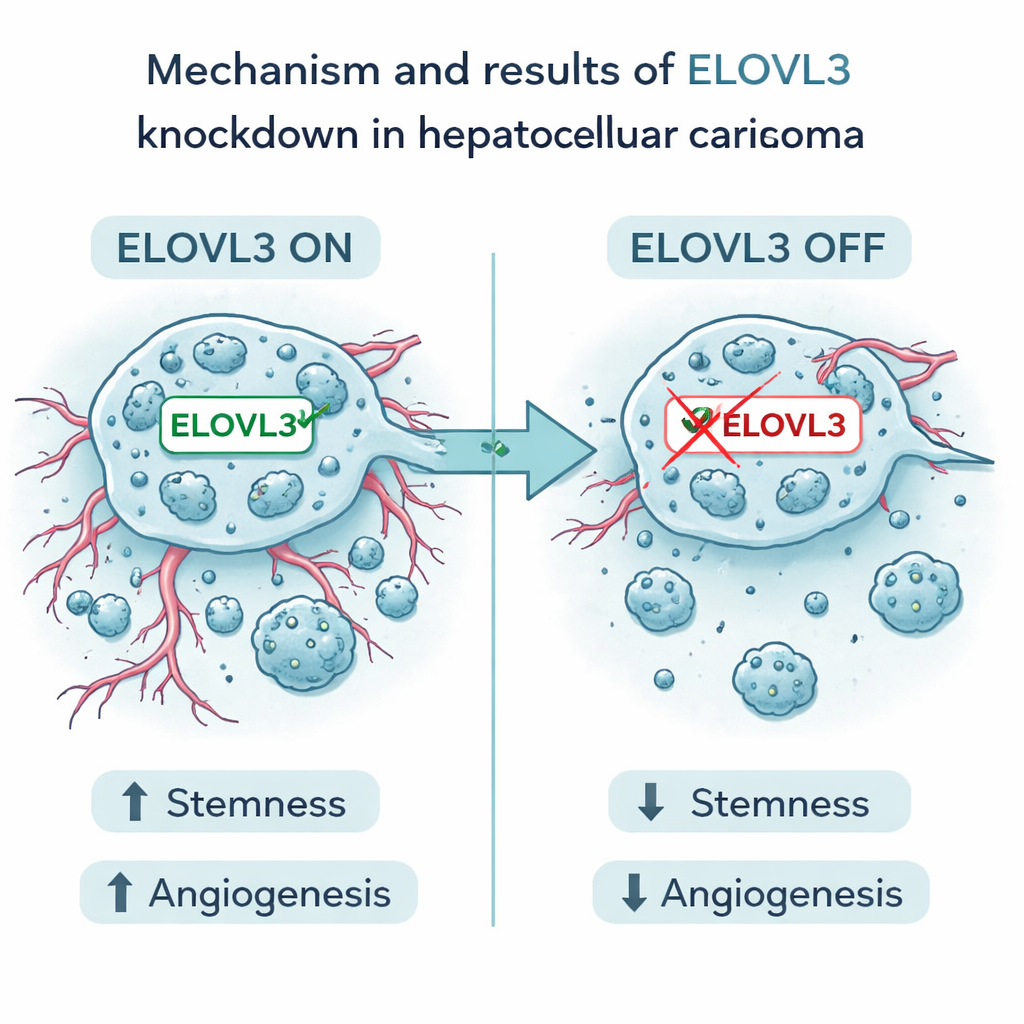
Fokussierung auf ein vielversprechendes Ziel
Unter den neun Genen stach eines namens ELOVL3 hervor. Hohe Expression dieses Gens war mit schlechterem Überleben verbunden. In Laborversuchen reduzierten die Autoren ELOVL3 in menschlichen Leberkrebszellen. Das verringerte ihre Fähigkeit, stammzellähnliche Cluster zu bilden, und senkte die Spiegel bekannter Stammzellmarker. Außerdem reduzierte es die Produktion und Freisetzung zweier wichtiger gefäßfördernder Faktoren, VEGFA und FGF2. Die Krebszellen zeigten geringeres Wachstum, weniger Migration und Invasion, und in Mausmodellen waren Tumoren mit reduziertem ELOVL3 kleiner und wiesen weniger Merkmale aggressiven Verhaltens auf. Diese Befunde stützen die Idee, dass ELOVL3 sowohl das stammzellähnliche Verhalten von Leberkrebszellen als auch ihre Fähigkeit zur Ausbildung unterstützender Blutgefäße fördert.
Was das für die zukünftige Versorgung bedeuten könnte
Einfach gesagt liefert diese Arbeit zwei zentrale Botschaften. Erstens kann ein einfacher Neun‑Gen‑Score aus Tumorproben Leberkrebspatienten in höher‑ und niedrigrisiko Gruppen einteilen und Hinweise darauf geben, wie sie auf immunbasierte Therapien reagieren könnten. Zweitens scheint eines der Gene in diesem Score, ELOVL3, an der Schnittstelle zwischen Regenerationsfähigkeit des Tumors und dessen Fähigkeit zur Gefäßbildung zu stehen und ist damit ein attraktives Ziel für zukünftige Medikamente. Obwohl Modell und Ziel in prospektiven klinischen Studien bestätigt werden müssen, eröffnen sie die Möglichkeit für individuellere Behandlungsansätze beim Leberkrebs und für Kombinationsstrategien, die sowohl die Krebs‑„Saatzellen“ als auch ihre Blutversorgung blockieren.
Zitation: Cheng, F., Shi, Y., Gao, X. et al. Machine learning-based prognostic model of stemness and angiogenesis-related genes for predicting prognosis and immune infiltration in patients with HCC. Sci Rep 16, 7271 (2026). https://doi.org/10.1038/s41598-026-38379-w
Schlüsselwörter: hepatozelluläres Karzinom, Krebsstammzellen, Angiogenese, prognostische Gensignatur, ELOVL3