Clear Sky Science · de
Variabilität von Referenzgenen nach Alter und Geschlecht bei 5XFAD-Mäusen verdeutlicht Normalisierungsprobleme in Alzheimer-Modellen
Warum diese Mausstudie für die Alzheimer-Forschung wichtig ist
Wenn Wissenschaftler nach Frühwarnzeichen oder Behandlungseffekten bei Alzheimer suchen, messen sie häufig, wie stark verschiedene Gene im Gehirn ein- oder ausgeschaltet sind. Um jedoch festzustellen, ob sich ein Gen wirklich verändert hat, brauchen sie zunächst ein konstantes „Maß“ zum Vergleich: Referenzgene, von denen angenommen wird, dass sie stabil bleiben. Diese Studie zeigt, dass diese angeblich konstanten Gene in einem schnell fortschreitenden Mausmodell der Alzheimer-Krankheit keineswegs so stabil sind, wie viele Forscher annehmen — insbesondere über unterschiedliche Altersstufen, Hirnregionen und zwischen Männchen und Weibchen hinweg.
Wie Forscher die genetische Aktivität des Gehirns lesen
Moderne Hirnforschung stützt sich oft auf eine Methode namens RT-qPCR, die zählt, wie viel von einer bestimmten Genbotschaft in einer Gewebeprobe vorliegt. Da Proben nie exakt die gleiche Gesamtmenge an Material enthalten, normalisieren Forscher ihre Messungen an ein oder mehrere Referenzgene, oft als „housekeeping“-Gene bezeichnet, die unter verschiedenen Bedingungen konstant sein sollten. In der Praxis verändern Krankheiten wie Alzheimer jedoch Zelltypen, Stoffwechsel und Entzündungsprozesse im Gehirn massiv, was die Niveaus dieser Referenzgene stillschweigend verschieben kann. Wenn sich das Referenzmaß selbst verschiebt, können darauf basierende Messungen irreführend sein und echte biologische Veränderungen über- oder unterschätzen.
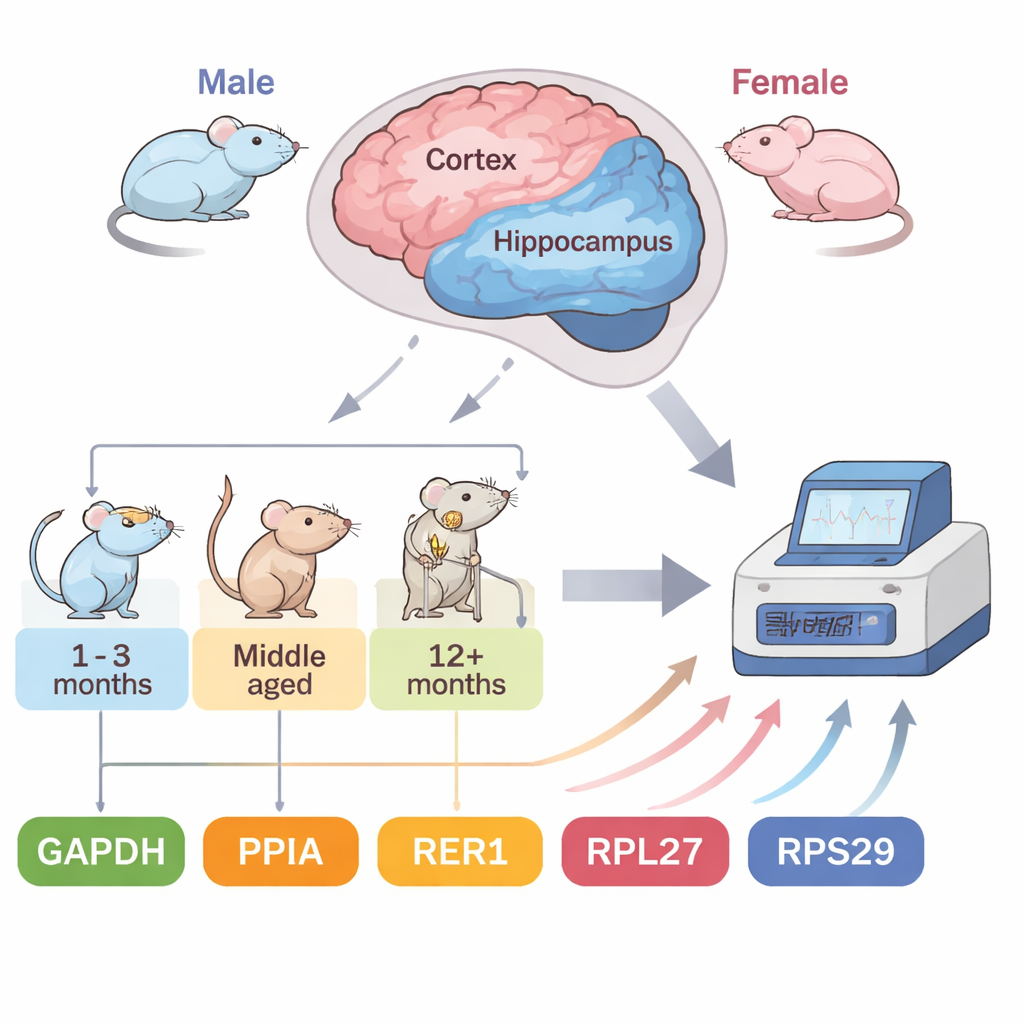
Ein Schnellmodell für Alzheimer
Das Team konzentrierte sich auf 5XFAD-Mäuse, ein weit verbreitetes Modell, das fünf menschliche Mutationen trägt, die mit familiärer Alzheimer-Krankheit verbunden sind. Diese Tiere entwickeln Amyloidplaques — Proteinablagerungen, die für die Krankheit charakteristisch sind — bemerkenswert früh: bereits mit etwa zwei Monaten, und mit starker Plaquebildung nach vier bis fünf Monaten. Dieser beschleunigte Zeitverlauf ermöglicht es Forschern, krankheitsbedingte Veränderungen über Monate statt Jahre zu verfolgen. Die Autoren untersuchten zwei besonders betroffene Hirnregionen, den Cortex und den Hippocampus, bei männlichen und weiblichen Mäusen in vier Stadien: früh (2 Monate), entwickelnd (4 Monate) sowie weiter fortgeschritten (7 und 10 Monate). Sie testeten fünf gängige Referenzgene und nutzten vier unabhängige statistische Werkzeuge, um zu bewerten, wie stabil jedes einzelne unter diesen wechselnden Bedingungen war.
Referenzgene sind keine Einheitslösung
Die Ergebnisse zeigen, dass kein einzelnes Gen überall perfekt stabil blieb. Stattdessen hing die Stabilität davon ab, aus welcher Hirnregion die Probe stammte, ob die Maus männlich oder weiblich war und wie weit die Erkrankung fortgeschritten war. Einige Gene, wie Gapdh — ein klassischer Standard in vielen Studien — schnitten in mehreren Situationen relativ gut ab, insbesondere im Cortex in frühen Stadien, zeigten aber in späteren Phasen oder in bestimmten Hippocampus-Proben größere Variabilität. Andere Kandidaten, etwa Rps29, Ppia, Rpl27 und Rer1, erwiesen sich in bestimmten Kombinationen als bessere Partner, und diese „besten Paare“ änderten sich mit Alter und Geschlecht. Insgesamt zeigte der Cortex tendenziell mehr Variabilität als der Hippocampus, und spätere Krankheitsstadien, besonders bei männlichen Mäusen, störten die angenommene Stabilität mehrerer Referenzgene.
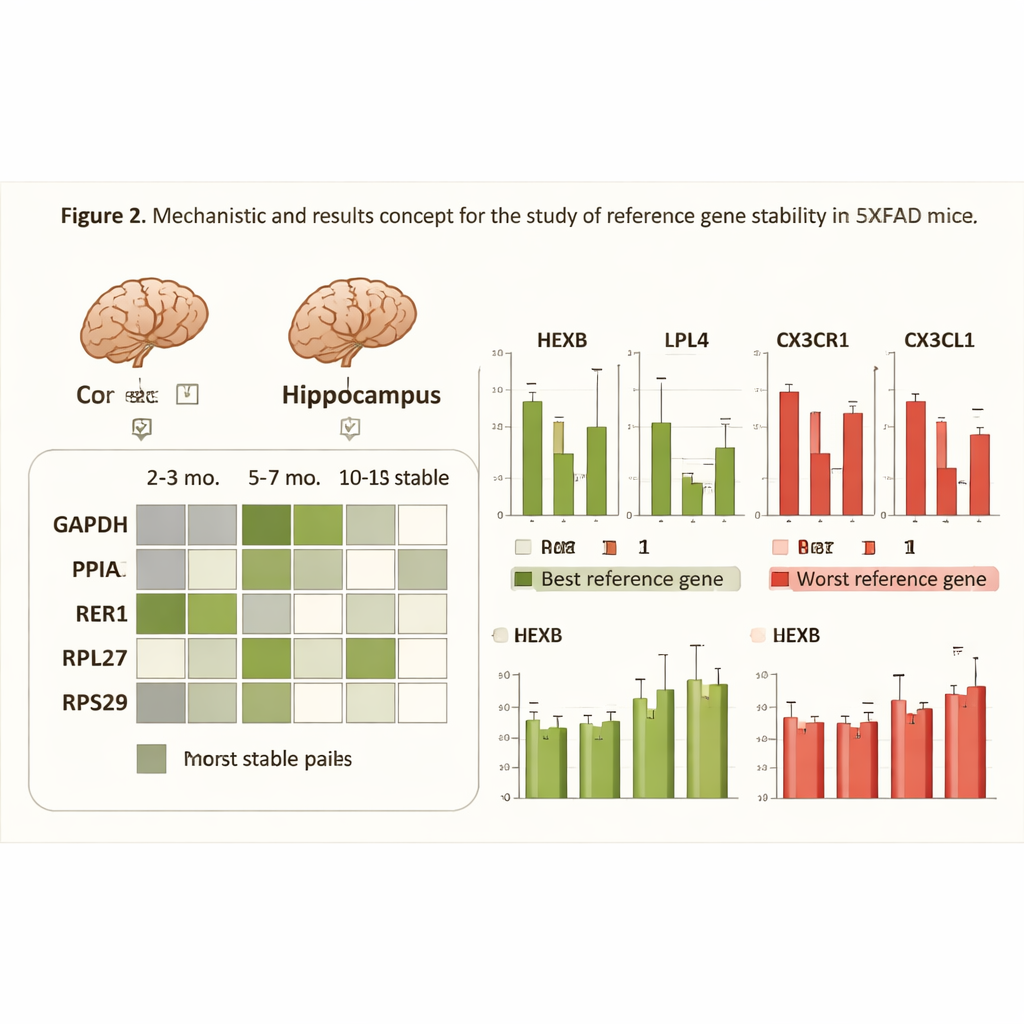
Was passiert, wenn das Maß sich verzieht
Um zu zeigen, warum die sorgfältige Auswahl von Referenzgenen wichtig ist, betrachteten die Forschenden vier Genprodukte im Gehirn, die an Entzündung, Stoffwechsel und Immun‑Signalgebung beteiligt sind — Prozesse, die bei Alzheimer tiefgreifend betroffen sind. Sie verglichen, wie die scheinbaren Veränderungen dieser Zielgene ausfielen, wenn sie entweder mit dem stabilsten Referenzpaar, dem am wenigsten stabilen Einzelgen oder mit allen fünf Genen zusammen normalisiert wurden. Bei Verwendung schlechter Referenzgene wurden die Daten verrauschter und einige biologisch bedeutsame Veränderungen wirkten schwächer oder sogar statistisch nicht signifikant. Im Gegensatz dazu reduzierte die Nutzung des am besten passenden Paars für jede Bedingung die Streuung in den Messwerten und verbesserte die Erkennung echter Unterschiede zwischen gesunden und erkrankten Mäusen, insbesondere in späteren Pathologiestadien.
Deutlichere Signale bei einer komplexen Krankheit
Für nicht Spezialisten ist die Botschaft klar: Selbst die grundlegenden Maßstäbe, die in Genstudien verwendet werden, können unter dem Druck einer sich schnell verändernden Hirnkrankheit wie Alzheimer verzerrt werden. Diese Arbeit liefert einen praktischen Leitfaden zur Auswahl besserer Referenzgene in einem wichtigen Mausmodell und betont, dass Forscher ihre „Maßstäbe“ für jede untersuchte Hirnregion, jedes Alter und jedes Geschlecht validieren müssen. Auf diese Weise erhalten Wissenschaftler klarere, verlässlichere Messwerte darüber, welche Gene sich bei Alzheimer-ähnlicher Degeneration tatsächlich ändern — ein wesentlicher Schritt zum Verständnis der Krankheitsmechanismen und zur Bewertung potenzieller Therapien.
Zitation: Daini, E., Antonioni, K., Piemontese, M. et al. Reference gene variability across age and sex in 5XFAD mice highlights normalization challenges in Alzheimer’s models. Sci Rep 16, 7302 (2026). https://doi.org/10.1038/s41598-026-38346-5
Schlüsselwörter: Alzheimer-Krankheit, Genexpression, 5XFAD-Mäuse, Referenzgene, RT-qPCR