Clear Sky Science · de
Hemmung des Galaninrezeptors 3 verlangsamt die Netzhautdegeneration bei Retinitis pigmentosa durch Modulation von Entzündungs- und oxidativem Stress‑Antworten
Warum der Schutz der schwindenden Nachtsehfähigkeit wichtig ist
Retinitis pigmentosa ist eine Gruppe vererbter Erkrankungen, die nach und nach das Nacht- und Seitensehen rauben und häufig im mittleren Lebensalter zu erheblichen Sehverlusten führen. Es gibt keine allgemein wirksame Behandlung, unter anderem weil viele verschiedene Genmutationen die Krankheit verursachen können. Diese Studie verfolgt einen anderen Ansatz: Statt das defekte Gen zu reparieren, wird untersucht, ob das Herunterregeln schädlicher Entzündungen und „rostähnlicher“ Schäden in der Netzhaut den Verlust lichtempfindlicher Zellen verlangsamen und so das Sehvermögen bewahren kann.
Ein in der Netzhaut verborgener Stress‑Schalter
Die lichtempfindlichen Zellen im hinteren Teil des Auges, die Photorezeptoren, müssen ständig Energieverbrauch, Sauerstoff, Nährstoffe und Abfallbeseitigung ausbalancieren. Bei einer häufigen Form der Retinitis pigmentosa verursacht eine Mutation im Rhodopsinprotein (bekannt als P23H), dass dieses visuelle Pigment falsch gefaltet wird, die zelluläre Maschinerie verstopft und chronischen Stress auslöst. Dieser Stress wiederum löst Entzündungen und oxidative Schäden aus, die beide Photorezeptoren abtöten können. Die Autorinnen und Autoren konzentrierten sich auf ein Signalmolekül namens Galaninrezeptor 3 (GALR3), das in mehreren Netzhautzelltypen vorkommt. Sie fanden heraus, dass bei Mäusen mit der P23H‑Mutation GALR3 und seine natürlichen Partnermoleküle stärker aktiviert waren als in gesunden Augen, was darauf hindeutet, dass GALR3 in degenerierenden Netzhäuten als Stressverstärker wirken könnte.
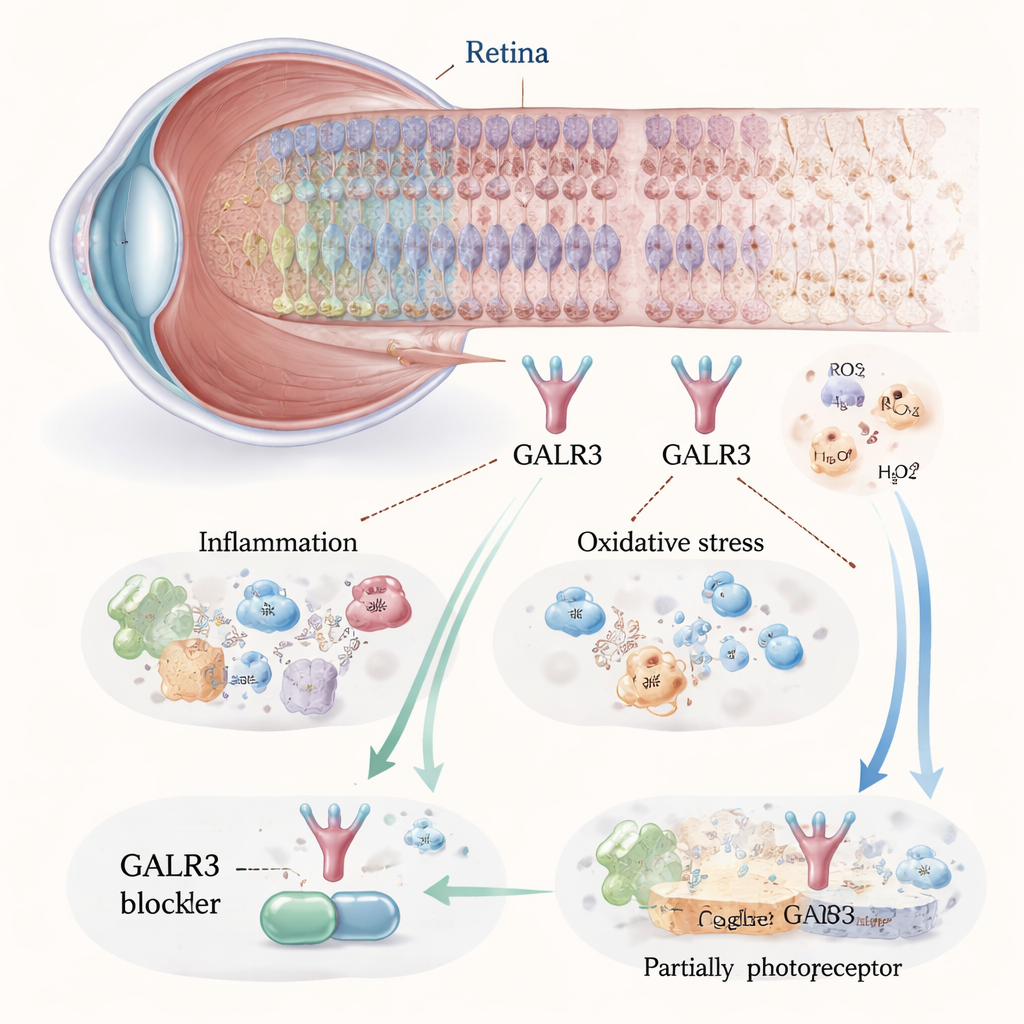
Zellverlust verlangsamen durch Blockade eines schädlichen Signals
Um zu prüfen, ob GALR3 Schäden antreibt oder schützt, verwendeten die Forschenden zwei Strategien in P23H‑Mäusen: Sie züchteten Tiere, denen das Gen Galr3 vollständig fehlte, und behandelten andere mit einem Wirkstoff, der den Rezeptor spezifisch blockiert, namens SNAP‑37,889. Über mehrere Wochen untersuchten sie die Netzhautstruktur mit hochauflösender Bildgebung und maßen elektrische Lichtantworten. Bei unbehandelten P23H‑Mäusen war die Schicht der Zellkerne, die die Photorezeptoren beherbergt, im Alter von einem Monat im Vergleich zu normalen Mäusen etwa halbiert und schrumpfte weiter. Als GALR3 blockiert wurde, war dieses Ausdünnen deutlich geringer, und wichtige visuelle Proteine wie Rhodopsin und Opsine der Zapfen blieben auf einem höheren Niveau. Auch die elektrischen Messungen zeigten stärkere Lichtantworten bei behandelten oder GALR3‑defizienten Mäusen, was bedeutet, dass die überlebenden Zellen besser funktionierten und nicht nur zahlreich vorhanden waren.
Entzündung dämpfen und Abwehrkräfte stärken
Das Team untersuchte dann, warum die GALR3‑Hemmung half. Bei Retinitis pigmentosa verwandeln sich Stützzellen der Netzhaut — Müller‑Glia und Mikroglia — von Betreuern zu überaktiven Antwortgebern, die chronische Entzündungen antreiben. In P23H‑Mäusen waren Marker dieses „Alarmzustands“, darunter GFAP in Gliazellen und IBA‑1 in Mikroglia, stark erhöht, und ein Spektrum entzündlicher Moleküle und Gefahrensensoren, wie NF‑κB und das NLRP3‑Inflammasom, war angehoben. Die Blockade von GALR3 beruhigte diese Reaktion: die Glia‑Aktivierung nahm ab, proinflammatorische Zytokine fielen, und antiinflammatorische Signale, die mit Gewebereparatur verbunden sind, wie IL‑10 und TGF‑β1, stiegen früh in der Krankheitsentwicklung. Parallel dazu stärkte die GALR3‑Hemmung die antioxidativen Abwehrmechanismen der Netzhaut. Sie erhöhte die Aktivität von NRF2, einem zentralen Regulator antioxidativer Gene, und steigerte Enzyme, die reaktive Sauerstoffspezies neutralisieren, wodurch weiterer Schaden durch metabolischen Stress begrenzt wurde.
Schutz der inneren Barriere des Auges
Gesundes Sehen hängt auch von einer intakten Blut‑Retina‑Barriere ab, die unerwünschte Moleküle und Immunzellen davon abhält, ins empfindliche Nervengewebe einzudringen. Bei P23H‑Mäusen begann diese Barriere zu undicht zu werden: Verbindungen zwischen den retinalen Pigmentepithelzellen wurden unregelmäßig, und Blutproteine sickerten in die Netzhaut. Sowohl der genetische Verlust als auch die pharmakologische Blockade von GALR3 reduzierten diese Defekte deutlich, bewahrten das ordentliche, kachelartige Muster der Barriere und begrenzten das Austreten. In Zellkulturversuchen reagierten photorezeptorähnliche Zellen, die Entzündungssignalen aktivierter Mikroglia ausgesetzt waren, mit einer Hochregulierung eigener entzündlicher Gene, doch dieser Effekt wurde abgeschwächt, wenn GALR3 in den Photorezeptorzellen stummgeschaltet wurde. Zusammengenommen zeigen diese Befunde, dass GALR3 an einem Kreuzungspunkt sitzt, der Mikrogliaaktivierung, oxidativen Stress und Barriereversagen mit dem Tod von Photorezeptoren verbindet.
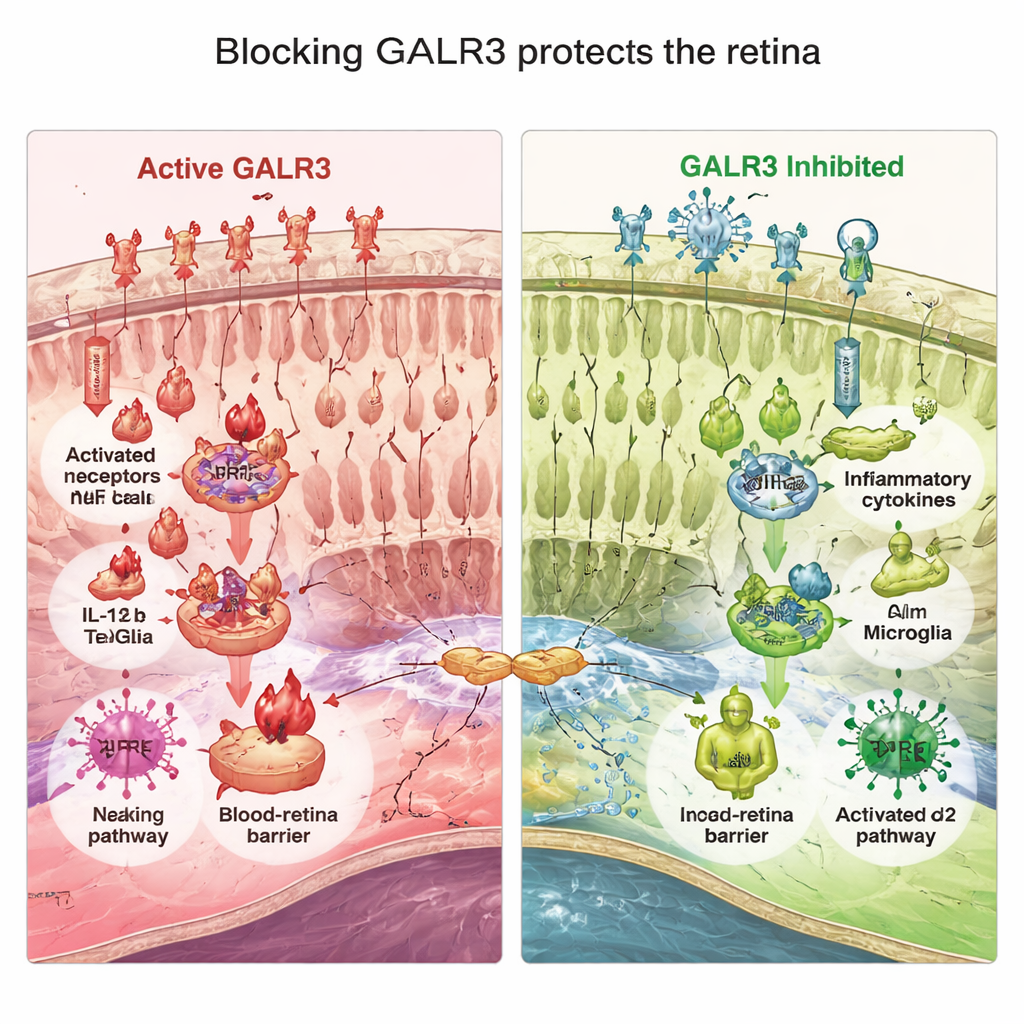
Eine mutationsunabhängige Route zum Erhalt des Sehens
Für Menschen mit Retinitis pigmentosa, insbesondere für jene, die möglicherweise nie gentherapiespezifische Behandlungen erhalten, sind Strategien, die die Netzhautschädigung allgemein verlangsamen, sehr wertvoll. Diese Studie identifiziert GALR3 als einen wichtigen „Lautstärkeregler“ schädlicher Entzündung und oxidativen Stresses in einem weit verbreiteten Mausmodell der Erkrankung. Die Blockade von GALR3 heilte die Retinitis pigmentosa nicht, verlangsamt aber konsistent den Verlust von Photorezeptoren, verbesserte die lichtinduzierten Netzhautantworten, reduzierte toxische Entzündungen, stärkte die natürlichen antioxidativen Abwehrmechanismen und half, die innere Barriere des Auges zu erhalten. Da GALR3 auf Stress‑ und Immunwege wirkt und nicht auf eine einzelne Mutation, könnten Wirkstoffe, die diesen Rezeptor gezielt hemmen, prinzipiell Patientinnen und Patienten mit vielen verschiedenen genetischen Ursachen der Netzhautdegeneration helfen.
Zitation: Azam, M., Pashandi, Z., Liu, M. et al. Inhibition of galanin receptor 3 slows down retina degeneration in retinitis pigmentosa through modulation of inflammatory and oxidative stress response. Sci Rep 16, 7765 (2026). https://doi.org/10.1038/s41598-026-38345-6
Schlüsselwörter: Retinitis pigmentosa, Netzhautentzündung, Photorezeptor‑Überleben, Galaninrezeptor 3, oxidativer Stress