Clear Sky Science · de
DGCR8 reguliert mehrere Prozesse der transkriptionsgekoppelten Nukleotid-Exzisionsreparatur
Wie Sonnenlicht mit unseren Genen spricht
Jedes Mal, wenn wir uns in die Sonne begeben, treffen unsichtbare ultraviolette (UV-)Strahlen auf unsere Haut und schädigen die DNA in unseren Zellen. Meist reparieren die Zellen diese Schäden unbemerkt, bevor sie Probleme verursachen. Diese Studie enthüllt einen überraschenden Akteur in diesem Schutzsystem: ein Protein namens DGCR8, das bisher vor allem dafür bekannt war, der Zelle bei der Herstellung von microRNAs zu helfen. Die Forschenden zeigen, dass DGCR8 nach UV-Exposition die Aufgabe wechseln kann und mehrere Schritte eines wichtigen DNA-Reparaturwegs koordiniert, der Krebs und andere Erkrankungen verhindert.
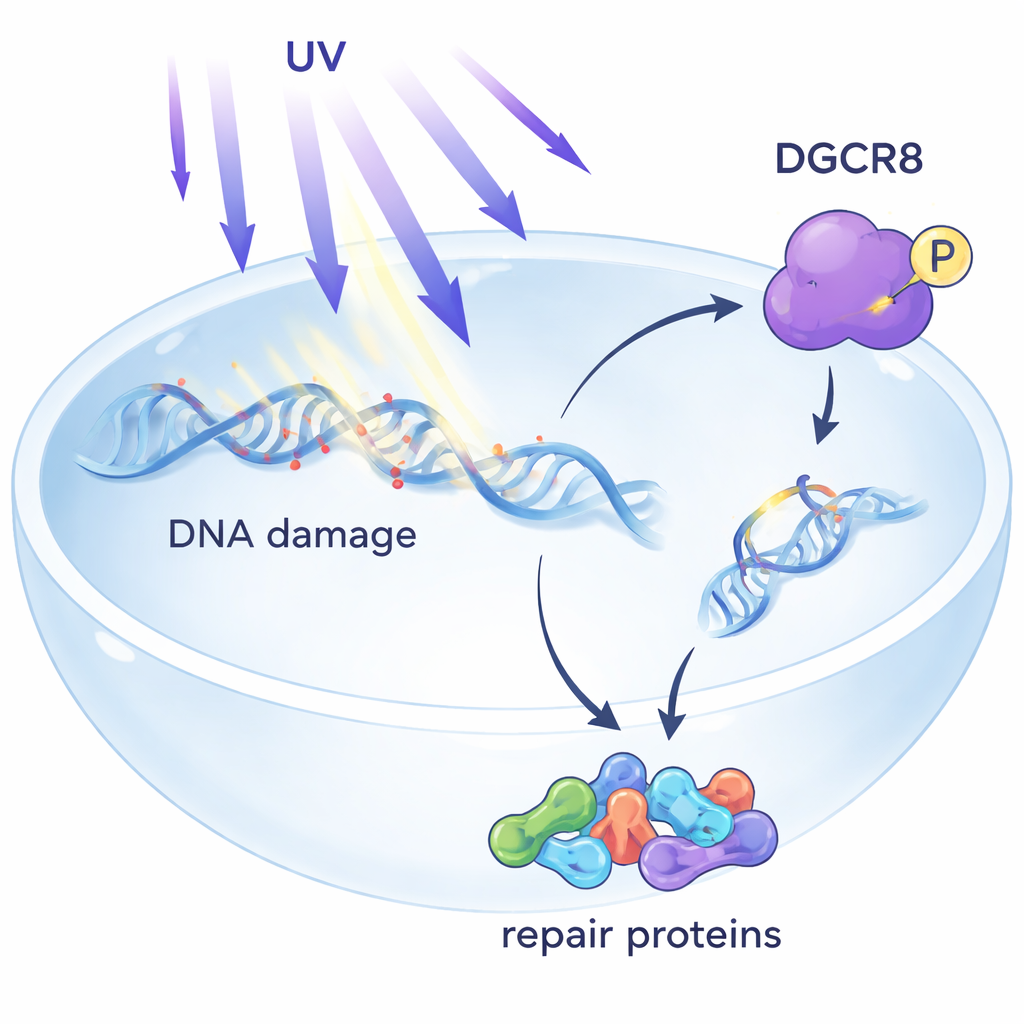
Ein verborgener Wächter in der DNA-Reparatur
UV-Licht erzeugt winzige Läsionen in der DNA, die die molekularen Maschinen, die Gene ablesen, blockieren können. Eine der Hauptabwehrmechanismen des Körpers ist die transkriptionsgekoppelte Nukleotid-Exzisionsreparatur (TC-NER), die sich auf Schäden konzentriert, die die Transkriptionsmaschinerie zum Stillstand bringen. Bisher war DGCR8 hauptsächlich für die Verarbeitung von microRNAs bekannt, kurzen RNA-Molekülen, die die Genaktivität feinjustieren. Frühere Arbeiten deuteten darauf hin, dass DGCR8 Zellen auch vor UV schützt, doch die zugrundeliegenden Mechanismen waren unklar. Dieses Papier zeigt, dass DGCR8 nach UV-Exposition physisch mit zentralen TC-NER-Faktoren assoziiert und als Organisator wirkt, der Reparaturkomponenten genau dorthin bringt, wo das Ablesen der Gene gestoppt wurde.
Ein molekularer Ein-/Ausschalter für DGCR8
Der Schlüssel zu DGCR8s neuer Rolle ist ein einzelner chemischer Marker an einem seiner Bausteine: die Aminosäure Serin an Position 153. Wenn diese Stelle phosphoryliert ist — das heißt eine Phosphatgruppe hinzugefügt wurde — erwirbt DGCR8 die Fähigkeit, an zentrale TC-NER-Komponenten zu binden, darunter die RNA-Polymerase II (das Transkriptionsenzym) sowie die Reparaturfaktoren CSB, CSA und UVSSA. Zellen, die so verändert wurden, dass DGCR8 an dieser Stelle nicht phosphoryliert werden kann (der S153A-Mutant), zeigten schwache oder verlorene Wechselwirkungen zwischen diesen Reparaturproteinen, und die normale UV-getriggerte Assemblierung des Reparaturkomplexes blieb aus. Eine „phosphomimische“ Variante, die sich verhält, als sei sie ständig phosphoryliert, hatte den gegenteiligen Effekt und verstärkte wichtige Interaktionen selbst ohne UV. Diese Ergebnisse deuten darauf hin, dass die Phosphorylierung an Ser153 als Ein-/Ausschalter wirkt, der DGCR8 von seiner üblichen RNA-verarbeitenden Rolle in einen Koordinator der DNA-Reparatur umschaltet.
Gefährliche DNA–RNA-Knoten entwirren
Neben dem Zusammenführen von Reparaturproteinen hilft DGCR8 auch bei der Kontrolle von Strukturen, die R-Loops genannt werden — kurze Abschnitte, in denen neu synthetisierte RNA an die DNA zurückbindet, von der sie stammt, und so ein DNA–RNA-Hybrid entsteht. In kleinen Mengen können R-Loops nützlich sein, aber wenn sie nach UV-Exposition akkumulieren, können sie die DNA-Replikation blockieren und Chromosomen destabilisieren. Mittels spezialisierter Antikörper und fluoreszenter Sonden fanden die Autorinnen und Autoren heraus, dass Zellen ohne DGCR8 oder mit der nicht-phosphorylierbaren S153A-Form nach UV deutlich mehr R-Loops aufbauen. Phosphoryliertes DGCR8 wurde an diesen Hybridstrukturen beobachtet, insbesondere dort, wo sie mit UV-verursachten Läsionen überlappten, was darauf hindeutet, dass es hilft, schädliche R-Loops gezielt an aktiven Genen unter Stress zu verhindern oder zu beseitigen.
Die DNA-Replikation im Griff behalten
Wenn DNA-Schäden oder R-Loops das Kopieren des Genoms stören, verlangsamen Zellen normalerweise die Replikation über eine Schutzschaltung, die als ATR–CHK1-Checkpoint bekannt ist. Faser-Tracking-Experimente zeigten, dass Zellen mit normalem DGCR8 nach UV ihre Replikationsspuren verlangsamten, was einem aktivierten Checkpoint entspricht. Im auffälligen Gegensatz setzten Zellen ohne DGCR8 oder mit der S153A-Mutation die Replikation nahezu mit normaler Geschwindigkeit fort, obwohl sie DNA-Schäden und R-Loops angesammelt hatten. Weitere Tests ergaben, dass zwar ATR selbst aktiviert wurde, sein zentraler Partner CHK1 in diesen Mutanten jedoch nur schwach eingeschaltet war. Das deutet darauf hin, dass phosphoryliertes DGCR8 dazu beiträgt, das Stresssignal von beschädigter DNA und R-Loops an CHK1 weiterzuleiten, sodass die Zelle anhalten und die Replikation stabilisieren kann.
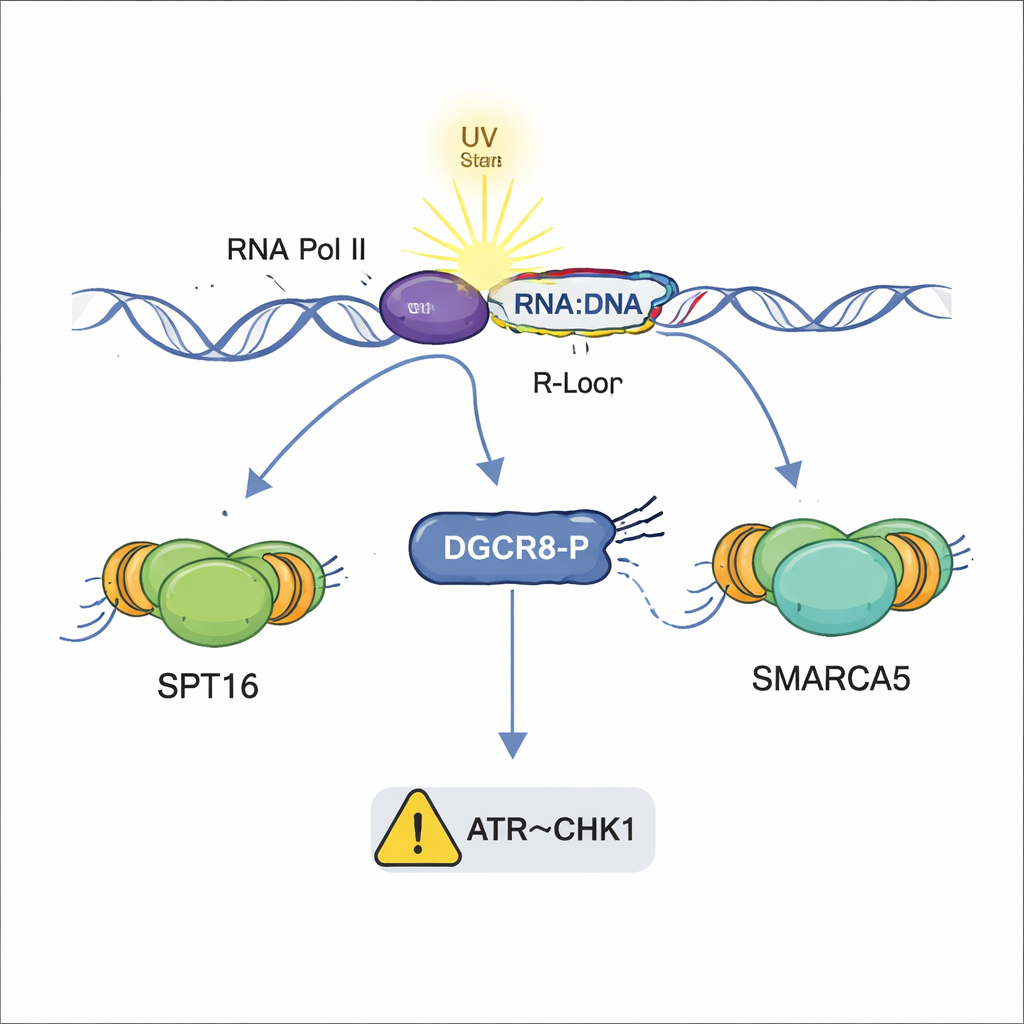
Warum das für Gesundheit und Krankheit wichtig ist
Insgesamt enthüllen die Ergebnisse DGCR8 als vielseitigen Wächter, der mehrere Ebenen der UV-Schadensantwort koordiniert: das Zusammenstellen des TC-NER-Reparaturteams, das Anwerben von Chromatin-Remodellierern, die die DNA öffnen, das Einschränken schädlicher DNA–RNA-Hybride und das Mitauslösen einer Replikationsverlangsamung über den ATR–CHK1-Weg. Entscheidend ist, dass diese Funktionen von DGCR8 getrennt von seiner traditionellen Rolle in der microRNA-Biogenese sind und von der Phosphorylierung einer einzigen Stelle abhängen. Da Fehler in der DNA-Reparatur und der Kontrolle von R-Loops mit Krebs und neurologischen Erkrankungen verknüpft sind und DGCR8-Mutationen in einigen Tumoren gefunden wurden, könnte das Verständnis dieses molekularen Schalters neue Wege für Diagnose oder Therapie von durch UV-Schäden und Genominstabilität verursachten Erkrankungen eröffnen.
Zitation: Watanabe, T., Yoshinami, D., Yamasaki, H. et al. DGCR8 regulates multiple processes of transcription coupled nucleotide excision repair. Sci Rep 16, 7112 (2026). https://doi.org/10.1038/s41598-026-38338-5
Schlüsselwörter: UV-induzierte DNA-Schäden, DGCR8, DNA-Reparatur, R-Loops, Genomstabilität