Clear Sky Science · de
PARP-1 koppelt β-Catenin/TCF4-Signalgebung an den epithelial–mesenchymalen Übergang bei Endometriose
Warum diese Forschung für die Frauengesundheit wichtig ist
Endometriose ist eine schmerzhafte Erkrankung, bei der Gewebe, das dem der Gebärmutterschleimhaut ähnelt, an falschen Stellen wächst, etwa auf den Eierstöcken. Diese fehlplatzierten Herde können benachbarte Strukturen infiltrieren, Narbenbildung verursachen und zur Unfruchtbarkeit beitragen. Die aktuellen Behandlungen sind jedoch oft unvollkommen und die Beschwerden kehren häufig zurück. Diese Studie untersucht einen molekularen „Schalter“ namens PARP‑1 und fragt, ob er dazu beiträgt, dass Endometrioseherde invasiver werden — und ob bereits verfügbare Medikamente, die PARP‑1 blockieren, diesen Schalter abschwächen könnten.
Ein genauerer Blick auf das Verhalten invasiver Herde
Obwohl Endometriose als gutartige Erkrankung eingestuft wird, verhält sich das ektope (fehlplatzierte) Gewebe oft überraschend aggressiv: Es wandert, setzt sich fest und persistiert ähnlich wie ein langsam wachsender Tumor. Ein zentraler Prozess hierfür ist der epithelial–mesenchymale Übergang (EMT), bei dem sich geordnete, blattförmige Zellen lösen und eine mobilere, faserige Identität annehmen. Die Autoren untersuchten Gewebeproben von Frauen mit und ohne Endometriose und stellten fest, dass ovariell gelegene endometriotische Läsionen ein deutliches EMT‑ähnliches Muster zeigten: Das „Klebe“-Protein E‑Cadherin war vermindert, während Marker für beweglichere Zellen, wie N‑Cadherin und Vimentin, erhöht waren. Gleichzeitig waren die Spiegel von PARP‑1 und Komponenten des wachstumssteuernden Wnt/β‑Catenin‑Signalwegs in diesen Läsionen am höchsten, was darauf hindeutet, dass all diese Veränderungen gemeinsam auftreten.
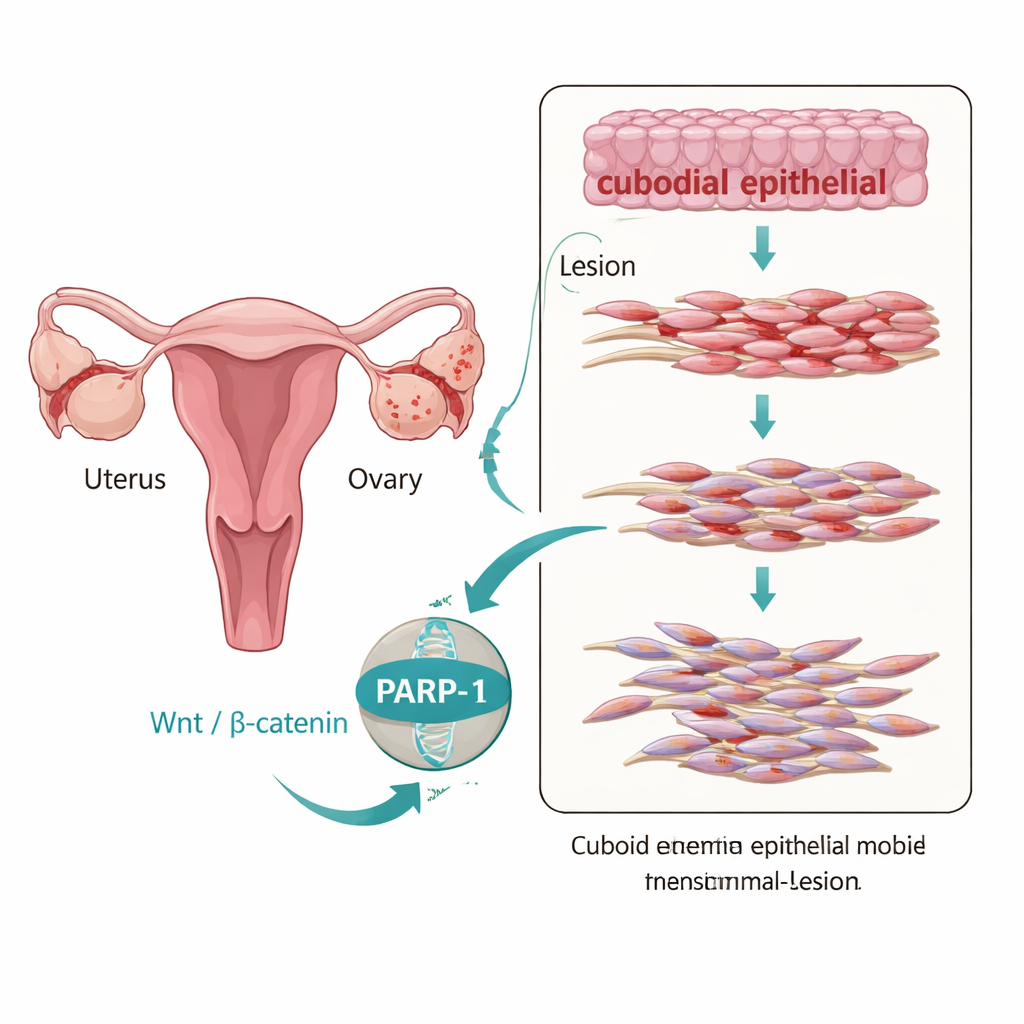
Die molekulare Brücke zwischen Signalen und Zellveränderung
Um herauszufinden, ob PARP‑1 nur präsent ist oder die Veränderungen aktiv vorantreibt, nutzten die Forscher eine immortalisierte endometriotische Epithelzelllinie namens 12Z. Als sie die PARP‑1‑Levels in diesen Zellen künstlich erhöhten, verschoben sich die EMT‑Marker hin zu einem invasiveren Profil, und die Zellen wurden in Labortests, die Wundheilung und Gewebeinvasion nachahmen, mobiler und überlebensfähiger. Bei der Reduktion von PARP‑1 mittels gezielter RNA‑Moleküle kehrte das Muster um: E‑Cadherin stieg, mesenchymale Marker sanken und die Zellen bewegten sich weniger und wuchsen schwächer. Wichtig ist, dass PARP‑1 physisch mit β‑Catenin und TCF4 assoziierte — zwei Schlüsselakteure, die Wnt‑Signale in Genaktivität übersetzen — was PARP‑1 als Brücke nahelegt, die äußere Signale mit dem EMT‑Genprogramm im Zellkern verbindet.
Den Schalter mit einem Krebsmedikament zurückdrehen
Da Wirkstoffe, die die PARP‑Aktivität hemmen, bereits in der Krebsbehandlung eingesetzt werden, prüfte das Team weiter, ob ein solches Medikament, Olaparib, EMT‑ähnliche Eigenschaften abmildern und das Wachstum von Läsionen in einem Mausmodell der Endometriose reduzieren könnte. Mäuse, denen kleine Gewebsfragmente der Gebärmutter implantiert wurden, entwickelten ektope Läsionen im Bauchraum und zeigten damit Aspekte der menschlichen Erkrankung. Bei zweiwöchiger Behandlung mit Olaparib wiesen diese Tiere deutlich geringeres Gesamtvolumen der Läsionen und leichtere Uteri mit haftenden Herden im Vergleich zu unbehandelten Kontrollen auf. Gewebe der behandelten Mäuse zeigte zudem ein stärker „epitheliales“ Markermuster — höhere E‑Cadherin‑Werte und niedrigere N‑Cadherin‑, Vimentin‑, β‑Catenin‑ und TCF4‑Spiegel — was darauf hinweist, dass die PARP‑Hemmung die Zellen vom invasiven EMT‑ähnlichen Zustand wegbewegte.
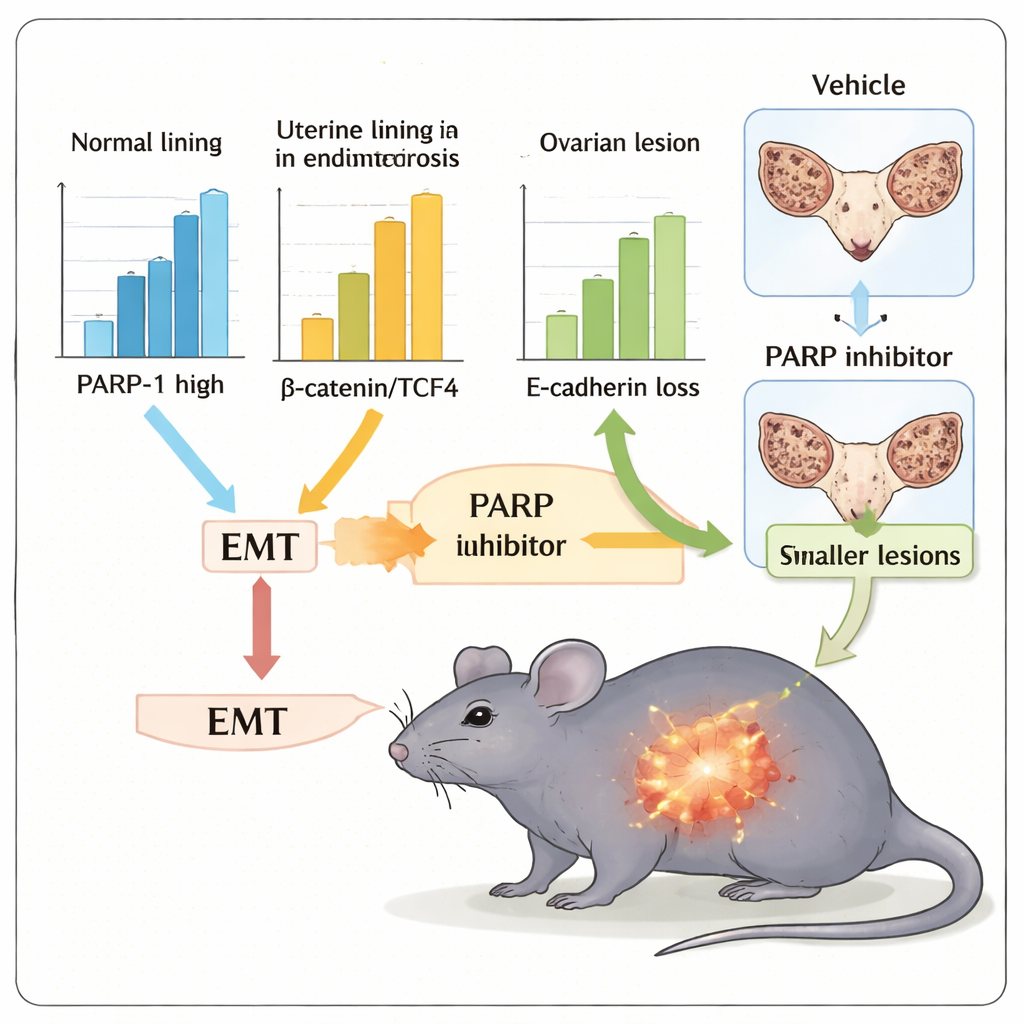
Was das für die zukünftige Versorgung bedeuten könnte
Insgesamt stützen die Befunde aus Patientinnenproben, Zellkultur‑Experimenten und dem Mausmodell eine vereinheitlichende Idee: PARP‑1 fungiert als medikamentenbarer Knotenpunkt, der Wnt/β‑Catenin‑Signalgebung mit EMT‑ähnlichem Verhalten bei Endometriose koppelt. PARP‑1 scheint weniger der einzelne Hauptschalter zu sein, sondern eher ein wichtiger Verbinder in einem größeren Netzwerk aus Entzündung, oxidativem Stress und hormonell gesteuerten Signalen, die das Wachstum und die Invasivität der Läsionen prägen. Da PARP‑Inhibitoren bereits existieren, eröffnet diese Arbeit die Möglichkeit, sie umzunutzen oder anzupassen — vielleicht in Kombination mit anderen Signalwegs‑ oder immunmodulierenden Wirkstoffen — um Läsionslast, Narbenbildung und möglicherweise Auswirkungen auf die Fruchtbarkeit zu verringern. Größere und längerfristige Studien werden nötig sein, doch diese Forschung öffnet einen konkreten Weg hin zu gezielteren, mechanismspezifischen Therapien für eine Erkrankung, die weltweit Millionen von Frauen betrifft.
Zitation: Zhang, L., Li, X., Kong, L. et al. PARP-1 couples β-catenin/TCF4 signaling to epithelial–mesenchymal transition in endometriosis. Sci Rep 16, 6940 (2026). https://doi.org/10.1038/s41598-026-38335-8
Schlüsselwörter: Endometriose, PARP-1, epithelial–mesenchymaler Übergang, Wnt/β-Catenin, PARP-Inhibitor-Therapie