Clear Sky Science · de
Eine neuartige, KI-gekoppelte Flow‑Chamber‑Methode zur Quantifizierung der osmotischen Fragilität von Erythrozyten
Warum die Fragilität roter Blutkörperchen wichtig ist
Sekündlich quetschen sich Millionen Ihrer roten Blutkörperchen durch haarfeine Gefäße, während sie Sauerstoff transportieren. Wie leicht diese Zellen bei Belastung aufspringen — ihre sogenannte „Fragilität“ — kann auf Anämie, Probleme bei der Blutlagerung und Komplikationen schwerer Infektionen wie Sepsis hinweisen. Diese Studie stellt ein modernes, KI‑unterstütztes Mikroskopgerät vor, das misst, wie schnell rote Blutkörperchen in salzigen Lösungen zerfallen, mit dem Ziel, diesen wichtigen Test schneller, präziser und leichter in Forschungslabors und eines Tages auch in Krankenhäusern durchführbar zu machen.
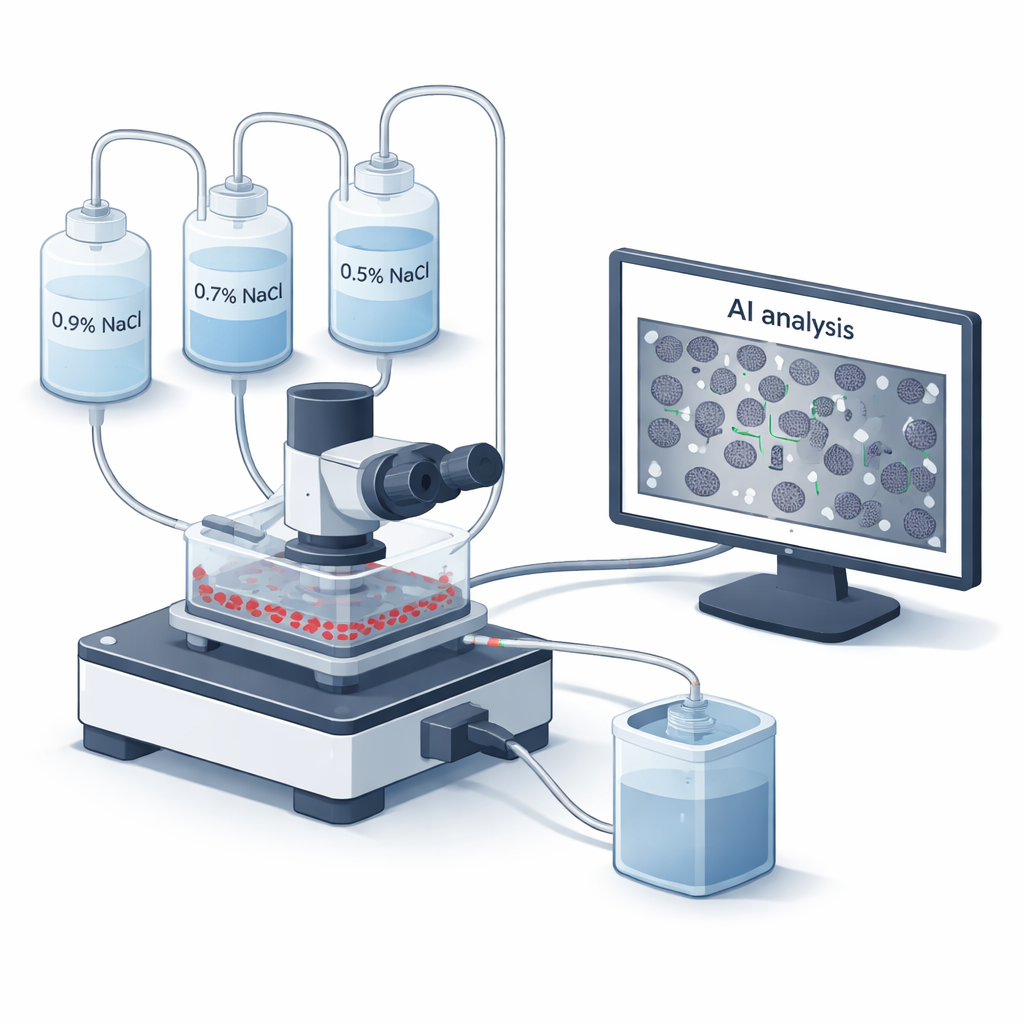
Eine neue Methode, Blutkörperchen unter Stress zu beobachten
Seit den 1940er‑Jahren verwenden Ärzte osmotische Fragilitätstests, um die Stabilität der Membranen roter Blutkörperchen zu beurteilen. Klassisch wird Blut mit einer Reihe von Salzlösungen vermischt und ein Gerät misst, wie viel Hämoglobin beim Aufplatzen der Zellen austritt. Zwar zuverlässig, ist diese klassische Methode langsam, manuell und sieht nicht, wie einzelne Zellen beim Versagen tatsächlich aussehen. Das Team hinter dieser Arbeit entwickelte ein neues mikrofluidisches „Flow‑Chamber“‑System namens BioExP, das rote Blutkörperchen als dünne Einschicht auf einer behandelten Glasfläche ausbreitet. Verschiedene Salzlösungen werden über diese Schicht gepumpt, während ein Mikroskop mit Kamera in Echtzeit aufzeichnet, was geschieht, und integrierte Software mit künstlicher Intelligenz zählt, wie viele Zellen bei jedem Salzkonzentrationsniveau intakt bleiben.
KI und Strömungssteuerung im Praxistest
Um zu beurteilen, ob BioExP zuverlässig ist, verglichen die Forschenden es direkt mit dem klassischen Spektrophotometer‑Assay unter Verwendung von Blutproben von vier gesunden Spendern. Im Mittelpunkt stand eine wichtige Kennzahl, die MCF₅₀: die Salzkonzentration, bei der die Hälfte der roten Zellen lysiert ist. Zunächst mussten sie ihr neues System kalibrieren, indem sie die beste „Sättigungszeit“ ermittelten — wie lange Zellen einer bestimmten niedrig konzentrierten Salzlösung ausgesetzt werden sollen, sodass die verwundbarsten Zellen lysieren, ohne zu überexponieren. Durch Verfolgen, wie viele Zellen bei 0,4 % Salz innerhalb von 15 Minuten verschwanden, stellten sie fest, dass nahezu 80 % der gesamten Hämolyse in den ersten drei Minuten auftraten. Dieses Drei‑Minuten‑Fenster wurde zum Standard‑Expositionszeitraum und bildete einen Kompromiss zwischen Geschwindigkeit und verlässlicher Messung.
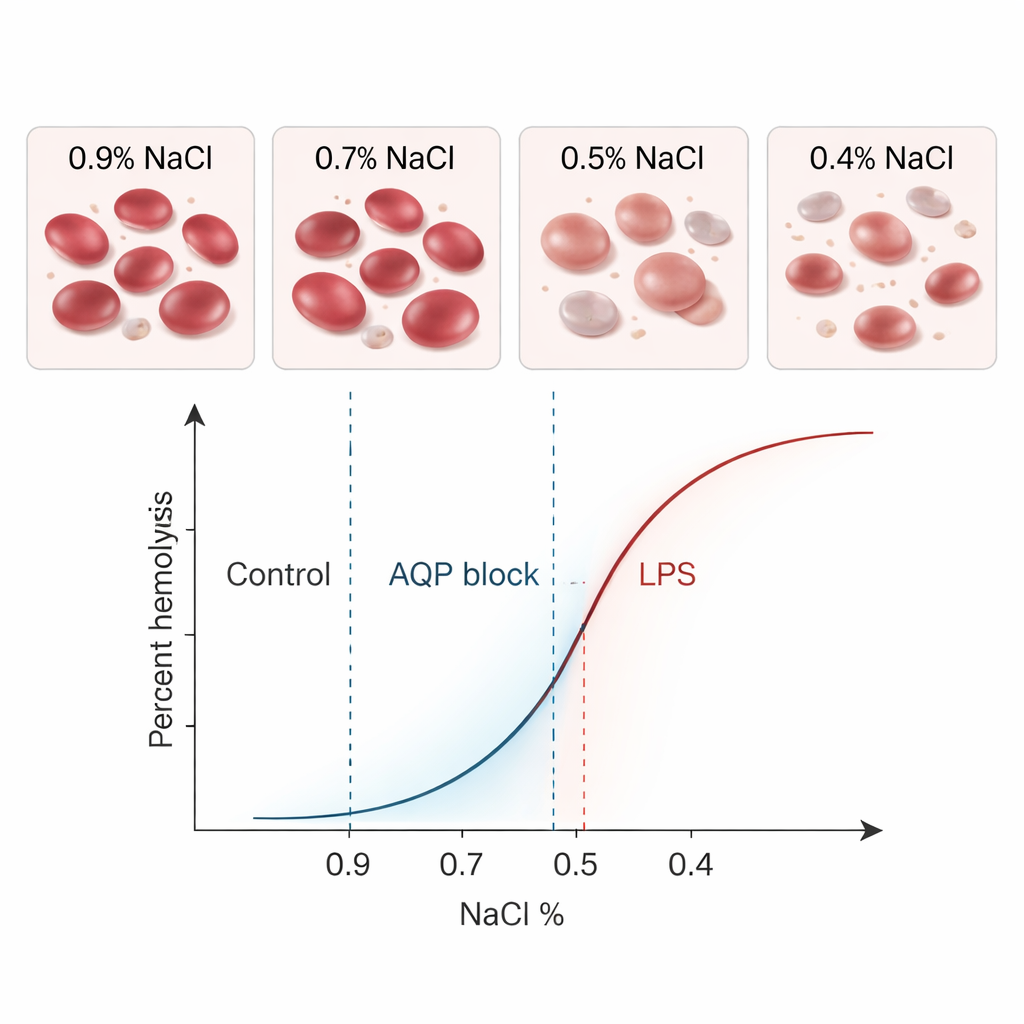
Abgleich mit dem klassischen Test und Untersuchung echter biologischer Effekte
Als sie dieselben gesunden Proben mit beiden Methoden untersuchten, ergaben BioExP und der klassische Test nahezu identische mittlere MCF₅₀‑Werte — 0,41 % Salz — bei ähnlicher Variabilität. Statistische Analysen zeigten keinen relevanten Unterschied zwischen den Methoden, und die meisten gepaarten Ergebnisse lagen innerhalb enger Übereinstimmungsgrenzen. Mit anderen Worten: Das neue Gerät „sprach effektiv die gleiche Sprache“ wie der etablierte Assay. Die eigentliche Stärke von BioExP liegt jedoch in seiner Fähigkeit, zu testen, wie verschiedene Bedingungen die Zellfragilität verändern. Die Forschenden wählten zwei biologisch relevante Modifikatoren: Quecksilberchlorid, das Wasserkanäle (Aquaporine) in der Zellmembran blockiert, und bakterielles Lipopolysaccharid (LPS), ein mit Sepsis assoziiertes Toxin.
Wie Toxine und Wasserkanäle die Widerstandskraft der Zellen verändern
Das Blockieren von Aquaporinen machte rote Blutkörperchen widerstandsfähiger gegen Aufplatzen: Die MCF₅₀ verschob sich zu niedrigeren Salzkonzentrationen, was bedeutet, dass die Zellen stärkere Verdünnung tolerierten, bevor sie zerbrachen. Sowohl BioExP als auch die klassische Methode erfassten diese Linksverschiebung deutlich. LPS zeigte den gegenteiligen Effekt. Wurden rote Zellen in Abwesenheit von Plasma mit einer hohen Dosis LPS inkubiert, wurden sie fragiler und lysierten bei höheren Salzkonzentrationen. Unter dem Mikroskop veränderten viele Zellen ihre Form und wurden kugeliger oder stacheliger — sichtbare Anzeichen einer gestörten Membran. Auch hier registrierten beide Methoden eine starke, statistisch signifikante Rechtsverschiebung der Fragilitätskurven. Insgesamt verfolgte das neue Flow‑Chamber‑System in all diesen Tests konsistent dieselben biologischen Trends wie der ältere Assay, wenn auch mit leicht niedrigeren absoluten Werten, die klein und systematisch waren.
Was das für Patienten und Labore bedeutet
Die BioExP‑Plattform reduziert die Assay‑Zeit von mehreren Stunden auf unter eine Stunde, benötigt nur winzige Blutmengen (möglicherweise nur einen Fingerstich) und automatisiert Zählung und Kurvenanpassung mit KI statt vieler manueller Schritte. Weil sie dieselben Zellen über die Zeit abbildet, kann sie das Aussehen der Zellen mit ihrer Aufplatzzusammenhang bringen und viele Salzkonzentrationen oder Wirkstoffbedingungen in einem Lauf testen. Die Studie zeigt, dass dieser moderne Ansatz die Genauigkeit des klassischen osmotischen Fragilitätstests erreichen kann und zusätzlich Geschwindigkeit, Flexibilität und reichhaltige visuelle Informationen liefert. Nach weiterer Validierung in größeren und heterogeneren Spendergruppen könnten solche Systeme wertvolle Werkzeuge zur Diagnose hämolytischer Anämien, zur Überwachung gelagerten Bluts in Blutbanken und zur Untersuchung, wie Infektionen oder neue Medikamente unsere roten Blutkörperchen schwächen oder schützen, werden.
Zitation: Fırat, I.S., Alaçayır, Ö., Creutz, T. et al. A novel AI-coupled flow chamber method quantifying erythrocyte osmotic fragility. Sci Rep 16, 7175 (2026). https://doi.org/10.1038/s41598-026-38322-z
Schlüsselwörter: rote Blutkörperchen, osmotische Fragilität, Microfluidik, Sepsis, künstliche Intelligenz