Clear Sky Science · de
Räumlich‑zeitliche Expression von Endosporen‑Anhängen und Kryo‑EM‑Einblicke in Ena1C‑vermittelte S‑ENA‑Verankerung bei Bacillus paranthracis
Warum hartnäckige bakterielle Sporen wichtig sind
Bakterien aus der Bacillus cereus‑Gruppe können zu widerstandsfähigen Sporen werden, die Hitze, Chemikalien und Reinigungsmittel überstehen. Diese Sporen haften oft an Geräten in der Lebensmittelverarbeitung und an anderen Oberflächen, wo sie über lange Zeit Lebensmittelvergiftungen verursachen oder Produkte kontaminieren können. Die vorliegende Studie untersucht winzige, haarähnliche Fasern auf diesen Sporen, sogenannte Endosporen‑Anhänge, und zeigt auf, wann sie gebildet werden und wie ein Schlüsselmolekül, Ena1C, sie an der Sporoberfläche verankert. Das Verständnis dieses Prozesses könnte der Industrie helfen, bessere Reinigungsstrategien zu entwickeln, und zudem neue Ansätze inspirieren, Sporen für Landwirtschaft oder Biotechnologie gezielt zu gestalten.
Steife Haare auf ruhenden Bakterien
Unter dem Mikroskop sind Sporen vieler Bacillus‑cereus‑Gruppen‑Bakterien von feinen Fasern bedeckt, die Borsten oder Pili ähneln. Diese Endosporen‑Anhänge sind extrem robust und widerstehen sowohl Enzymen als auch aggressiven Chemikalien, was ihre Erforschung erschwert hat. Frühere Arbeiten mit hochauflösender Kryo‑Elektronenmikroskopie zeigten, dass Bacillus paranthracis zwei Haupttypen von Fasern herstellt: dicke, versetzte S‑ENAs, die etwa 90 % der Haare ausmachen, und dünnere, leiterartige L‑ENAs, die den Rest bilden. Genetische Analysen hatten bereits spezifische ena‑Gene mit jedem Fasertyp verknüpft, doch wann und wo diese Proteine während der Sporulation erscheinen und wie S‑ENAs tatsächlich an der Spore verankert werden, waren weiterhin offene Fragen.
Die Aktivierung der Fasern in Echtzeit beobachten
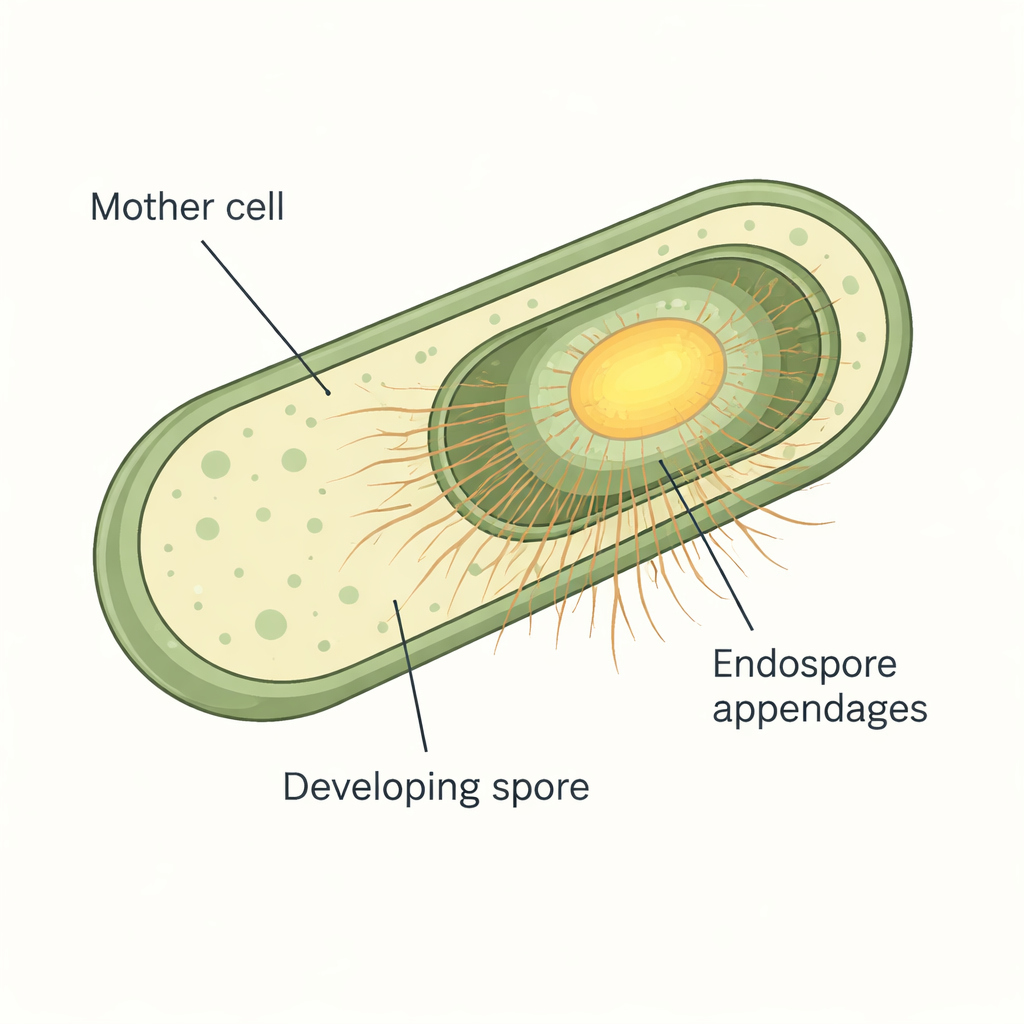
Um diesen Bausteinen beim Aufbau zuzusehen, fusionierten die Forscher die ENA‑Proteine mit hellen Fluoreszenzmarkern, sodass sie jedes Protein in lebenden Zellen per Zeitraffer‑Mikroskopie verfolgen konnten. Sie kultivierten Bacillus paranthracis auf speziell präparierten Agarplatten unter dem Mikroskop und fertigten alle 10 bis 12 Minuten Aufnahmen an, während die Zellen die Sporulation durchliefen. Das Team fand heraus, dass keine der ENA‑Proteine während des normalen Wachstums produziert wurden. Stattdessen begann die Produktion erst, nachdem sich die sich entwickelnden Sporen „phasenglänzend“ zeigten — ein visuelles Zeichen dafür, dass der Sporenkern und die Schutzschichten ausgereift sind. Die ENA‑Fluoreszenz stieg dann spät in der Sporulation stark an und konzentrierte sich um die Spore, besonders an der Schnittstelle zwischen Mutterzelle und entstehender Spore, was zeigt, dass diese Fasern wirklich sporenpezifische Dekorationen sind, die gegen Ende des Prozesses hinzugefügt werden.
Zwei Faser‑Typen mit unterschiedlichem Zeitplan
Das Team verglich außerdem die zeitliche Abfolge der S‑ENA‑ und L‑ENA‑Produktion, indem es zwei Proteine gleichzeitig in denselben Zellen verfolgte. Wenn S‑ENA‑Untereinheiten (Ena1A oder Ena1C) grün markiert zusammen mit der L‑ENA‑Untereinheit Ena3A in Rot exprimiert wurden, erschien das grüne Signal konstant etwa eine Stunde vor dem roten. Dieser versetzte Zeitplan stimmt mit dem bekannten Aufbau der Spore überein: S‑ENAs treten aus der Sporenhülle hervor, die früher gebildet wird, während L‑ENAs an das Exosporium verankert sind, eine äußere Hülle, die später hinzugefügt wird. Die Ergebnisse legen nahe, dass die Zelle spätzeitliche genetische Schalter nutzt, um ENA‑Gene in strikter Reihenfolge einzuschalten, sodass jeder Fasertyp zur richtigen Zeit in die passende Sporenschicht eingebaut wird.
Ein molekulares „Dock“, das Fasern an Ort und Stelle hält
Einer der rätselhaftesten Akteure war Ena1C, ein Protein, das für das Auftreten von S‑ENA‑Fasern auf Sporen erforderlich ist, aber nicht Teil des Faserstiels selbst ist. Bei der Untersuchung von Sporen aus Bakterien ohne das ena1C‑Gen stellten die Wissenschaftler fest, dass S‑ENA‑Fasern weiterhin gebildet wurden, jedoch frei in der umgebenden Flüssigkeit schwebten, statt an den Sporen befestigt zu sein. Bei Überproduktion von Ena1C trugen Sporen deutlich mehr S‑ENAs, doch jede Faser war kürzer, als würde ein begrenzter Vorrat an Bausteinen über zusätzliche Anknüpfungspunkte verteilt. Dies deutet darauf hin, dass Ena1C als dedizierter Anker fungiert, der S‑ENA‑Fasern an der Sporenhülle befestigt und sowohl die Anzahl der angehefteten Fasern als auch deren Länge kontrolliert.
Ringförmige Anker, sichtbar durch Kryo‑EM
Um zu sehen, wie Ena1C die Fasern greifen könnte, reinigten die Forscher das Protein und bildeten es mit hochauflösender Kryo‑Elektronenmikroskopie ab. Sie entdeckten, dass Ena1C keine langen Filamente bildet. Stattdessen verbinden sich neun Kopien des Proteins zu einem stabilen Ring mit einer zentralen Öffnung, der durch multiple Disulfidbrücken — starke chemische Bindungen zwischen schwefelhaltigen Aminosäuren — verstärkt wird. Computermodelle und strukturelle Vergleiche mit bekannten Faserproteinen deuten darauf hin, dass S‑ENA‑Stiele wahrscheinlich in den positiv geladenen Trichter in der Mitte dieses Rings einschieben, wo Schlüssel‑Cysteinreste von Ena1C Disulfidbindungen mit passenden Stellen an den Faseruntereinheiten eingehen können. Auf diese Weise scheint jeder Ena1C‑Ring als molekulares Dock zu dienen, das ein oder wenige S‑ENA‑Fasern an der äußeren Hülle der Spore festklemmt.
Was das für die Kontrolle hartnäckiger Sporen bedeutet
In der Summe zeigt die Studie, dass Sporenhaare bei Bacillus paranthracis erst nach der Reifung der Spore produziert werden, wobei S‑ENA‑Fasern gebaut und an der Hülle verankert werden, bevor L‑ENAs dem Exosporium hinzugefügt werden. Sie identifiziert zudem Ena1C als ringförmigen Anker, der S‑ENA‑Fasern kovalent mit der Sporoberfläche verbindet. Für Nicht‑Spezialisten lautet die Kernbotschaft: Dass Sporen an Oberflächen haften, ist kein Zufall — es ist das Ergebnis eines sorgfältig zeitlich abgestimmten Bauprojekts, das robuste, faserbasierte „Velcro“-Verbindungen außen an der Spore anbringt. Durch gezieltes Angreifen dieses Verankerungssystems — etwa durch Störung von Ena1C oder Veränderung der ENA‑Bildung — könnten künftige Strategien die Adhäsion von Sporen schwächen und die industrielle Reinigung verbessern oder umgekehrt Ingenieuren erlauben, Sporen so zu gestalten, dass sie gezielt an Pflanzen oder Materialien binden und dadurch nützliche Anwendungen ermöglichen.
Zitation: Zegeye, E.D., Sleutel, M., Jonsmoen, U.L. et al. Spatiotemporal expression of endospore appendages and cryo-EM insights into Ena1C-mediated S-ENA anchoring in Bacillus paranthracis. Sci Rep 16, 7122 (2026). https://doi.org/10.1038/s41598-026-38321-0
Schlüsselwörter: bakterielle Sporen, Oberflächenadhäsion, Kryo‑Elektronenmikroskopie, Proteinassemblierung, Lebensmittelsicherheit