Clear Sky Science · de
Selektive Inaktivierung von Lis1 stört Migration und Positionierung kortikaler Somatostatin‑Interneurone
Warum winzige Gehirnzellen und ein einziges Gen wichtig sind
In unseren Gehirnen müssen Milliarden von Nervenzellen genau an den richtigen Ort gelangen, damit Denken, Gefühle und Erinnerungen korrekt funktionieren. Diese Studie betrachtet eine kleine, aber einflussreiche Gruppe von Gehirnzellen, die Somatostatin‑Interneurone, und ein Gen namens Lis1, das bereits dafür bekannt ist, bei Mutationen eine schwere „glatte Hirn“-Erkrankung zu verursachen. Indem die Forschenden untersuchen, was passiert, wenn Lis1 nur in dieser winzigen Zellpopulation abgeschaltet wird, zeigen sie, wie subtile Fehler in der Zellmigration während der Entwicklung Schlüsselregionen des Gehirns verändern können, die an Stimmung, Gedächtnis und psychischen Erkrankungen beteiligt sind.
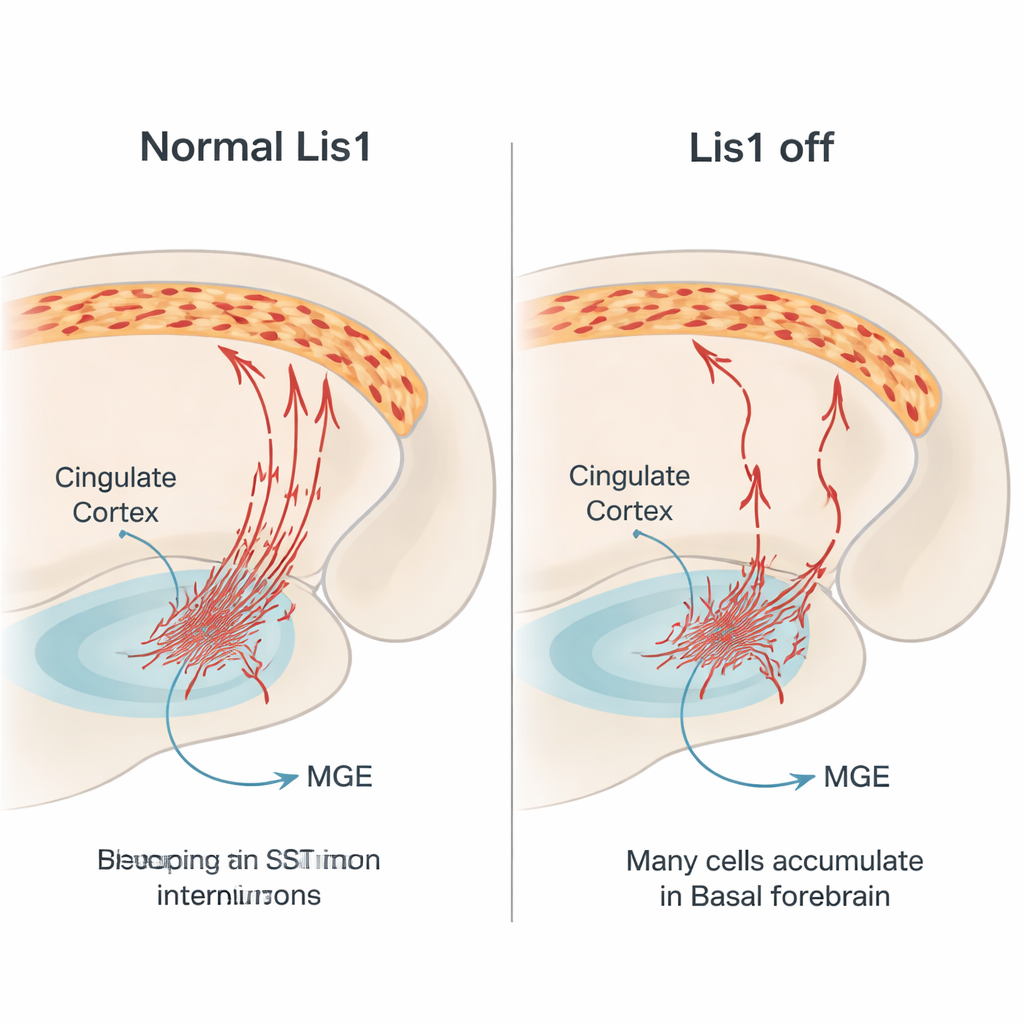
Hauptakteure im Bremssystem des Gehirns
Somatostatin‑Interneurone wirken als Teil des Bremssystems des Gehirns. Sie geben das inhibitorische Signal GABA und das Peptid Somatostatin frei und zielen dabei hauptsächlich auf die Dendriten von exzitatorischen Pyramidenneuronen. Das trägt dazu bei, die Gehirnaktivität im Gleichgewicht zu halten, was für normale Wahrnehmung, Entscheidungsfindung und emotionale Kontrolle unerlässlich ist. Viele dieser Interneurone entstehen in einer tiefen Region des embryonalen Gehirns, der medialen ganglionären Eminenz. Von dort aus wandern sie seitlich über weite Strecken in den Kortex, einschließlich des cingulären Kortex, einem Knotenpunkt für Emotion, Schmerz und Gedächtnis. Da diese Reise komplex und streng zeitlich gesteuert ist, sind Gene, die die Zellbewegung lenken, von entscheidender Bedeutung. Lis1 ist ein solches Gen und bekannt dafür, das innere Gerüst und die motorische Maschinerie der Zelle zu regulieren, die den Zellkern verschieben und die Zellform während der Migration bestimmen.
Ein gezieltes genetisches „Abschalt“‑Experiment
Um herauszufinden, welche Rolle Lis1 speziell in Somatostatin‑Interneuronen spielt, entwickelten die Autorinnen und Autoren Mäuse, in denen Lis1 nur in Zellen gelöscht wird, die das Somatostatin‑Gen aktivieren. Sie nutzten außerdem ein fluoreszierendes rotes Protein, um diese Zellen dauerhaft zu markieren und ihre Entwicklung zu verfolgen. Dieses Design erlaubte dem Team, Effekte innerhalb der Somatostatin‑Zellen selbst von Veränderungen im übrigen Gehirn zu unterscheiden. Ungefähr einen Monat nach der Geburt, einer Phase, in der kortikale Schaltkreise relativ reif, aber noch plastisch sind, untersuchten sie zwei cinguläre Regionen — den anterioren cingulären Kortex und den retrosplenialen Kortex. Mithilfe sorgfältiger Zählmethoden schätzten sie sowohl die absolute Zahl als auch die Dichte der Somatostatin‑Interneurone in jeder kortikalen Schicht.
Weniger Interneurone und ein verschobenes Schichtmuster
Bei jungen erwachsenen Mäusen, denen Lis1 in Somatostatin‑Interneuronen fehlte, enthielten sowohl der anteriore cinguläre als auch der retrospleniale Kortex deutlich weniger dieser Zellen als bei Kontrolltieren. Die Reduktion war groß und über alle untersuchten Schichten hinweg konsistent, was auf einen tatsächlichen Verlust statt auf eine bloße Umverteilung hindeutet. Bei genauerer Betrachtung der Anordnung der verbliebenen Zellen zeigte sich eine Veränderung des üblichen Schichtmusters. Bei gesunden Mäusen konzentrieren sich Somatostatin‑Interneurone tendenziell stärker in den tieferen Kortexschichten. Bei den Mutanten war dieses Gefälle umgekehrt: Relativ mehr Zellen fanden sich in den oberen Schichten und weniger in der tiefsten Schicht. Wichtig ist, dass die Gesamtgröße der cingulären Regionen nicht geschrumpft war, sodass die geringere Dichte tatsächlich fehlende Interneurone und nicht ein komprimiertes Gewebevolumen widerspiegelt.
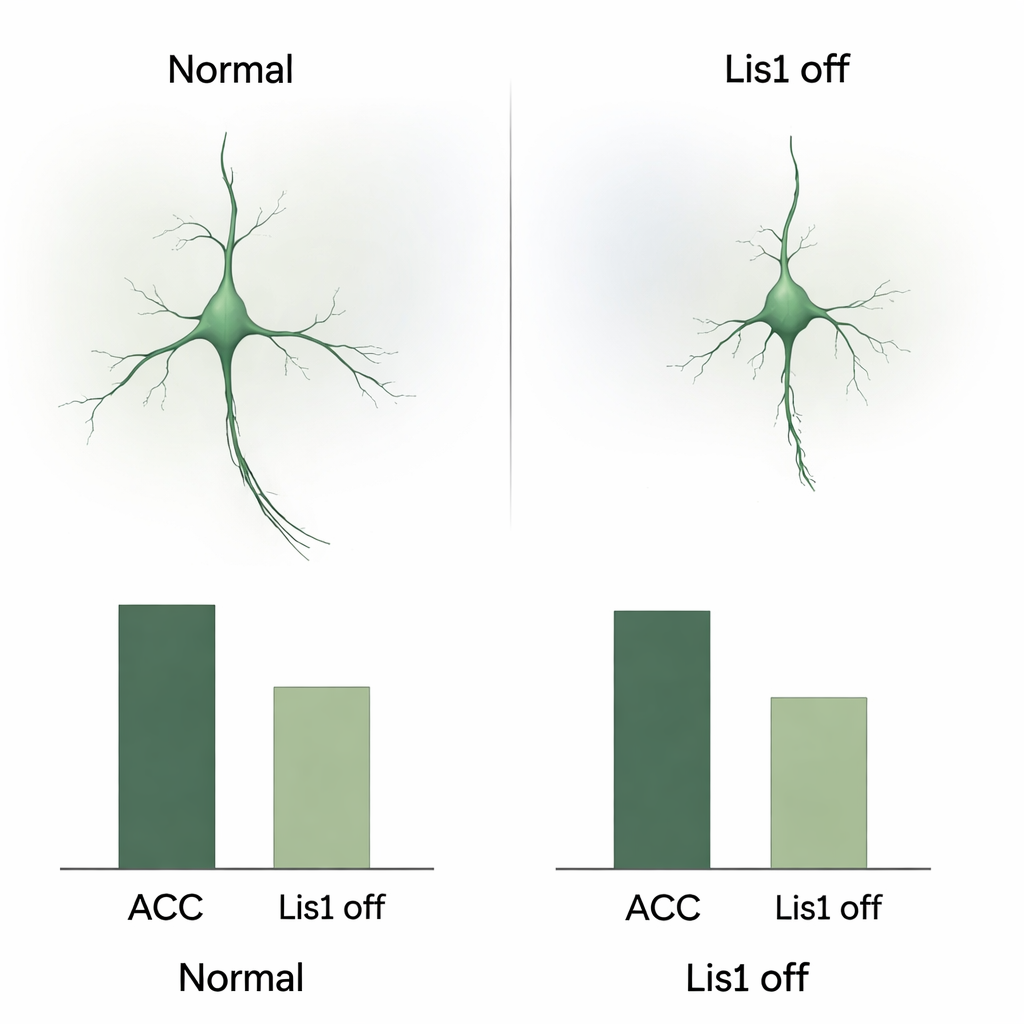
Eine fehlgeschlagene Entwicklungsreise
Um zu verstehen, wie dieser Verlust entsteht, verfolgte das Team die rot markierten Somatostatin‑Zellen in Embryonen. Sie bestätigten, dass die Lis1‑Löschung erst einsetzt, nachdem diese Zellen die Zellteilung eingestellt haben, wodurch ein direkter Effekt auf ihre Entstehung ausgeschlossen wurde. Stattdessen zeigte sich das Problem während ihrer langen Migration. In mittleren Gestationsstadien wurden deutlich weniger markierte Zellen auf den normalen Bahnverläufen in Richtung Kortex gefunden, und viele schienen im basalen Vorderhirn, einer ventralen Region, die sie passieren müssen, stecken zu bleiben. Die migrierenden Zellen, die sich bewegten, zeigten veränderte Formen: kürzere führende Fortsätze, weniger Verzweigungen und kleinere, rundere Zellkörper — alles Anzeichen dafür, dass ihre interne Transportmaschinerie beeinträchtigt ist. In späteren Stadien enthielt die ventrale Region der Mutanten mehr Zellen mit Merkmalen programmierter Zellsterblichkeit, was darauf hindeutet, dass viele feststeckende Interneurone sterben, bevor sie den Kortex erreichen.
Was das für die Gehirngesundheit bedeutet
Kurz gesagt: Wenn Lis1 nur in Somatostatin‑Interneuronen abgeschaltet wird, beginnen viele dieser Zellen ihre Reise normal, erreichen aber ihre Zielorte im cingulären Kortex nicht. Einige reichern sich an und sterben unterwegs; diejenigen, die ankommen, sind zahlenmäßig reduziert und ungleichmäßig über die Kortikalschichten verteilt. Da Systeme mit Somatostatin wiederholt mit Depression, Schizophrenie, Epilepsie und neurodegenerativen Erkrankungen in Verbindung gebracht wurden, hebt diese Arbeit einen direkten, zellspezifischen Weg hervor, über den Lis1‑Fehlfunktionen gestörte Gehirnrhythmen und psychiatrische Symptome begünstigen könnten. Die Studie zeigt, dass selbst eine vergleichsweise kleine Neuronengruppe, gesteuert von einem einzelnen Gen, entscheidend dafür sein kann, die ausgewogenen Schaltkreise aufzubauen, die gesundes Denken und Verhalten ermöglichen.
Zitation: Pombero, A., García-López, R., Geijo-Barrientos, E. et al. Selective Lis1 inactivation disrupts migration and positioning of cortical somatostatin interneurons. Sci Rep 16, 7330 (2026). https://doi.org/10.1038/s41598-026-38316-x
Schlüsselwörter: Somatostatin‑Interneurone, Lis1‑Gen, neurale Migration, cingulärer Kortex, neuroentwicklungsstörungen