Clear Sky Science · de
Entwicklung und Charakterisierung immortaliserter Maus‑Darmepithelzelllinien
Warum neue Darmzellmodelle wichtig sind
Die Auskleidung des Darms ist eine stark frequentierte Grenze, an der Nahrung, nützliche Mikroben und gefährliche Keime auf unseren Körper treffen. Um zu untersuchen, wie diese Barriere entsteht, heilt und Infektionen abwehrt, benötigen Forschende verlässliche Zellen, die sie im Labor kultivieren können. Die heutigen dreidimensionalen „Mini‑Darm“‑Kulturen sind zwar leistungsfähig, aber teuer, empfindlich und technisch anspruchsvoll, was ihre Verbreitung und regelmäßige Nutzung einschränkt. Diese Studie stellt eine praktischere Reihe von Maus‑Darmzelllinien vor, die leicht zu züchten, genetisch anpassbar und dennoch nah genug am echten Gewebe sind, um viele wichtige biologische und krankheitsrelevante Fragen zu beantworten.
Von der Maus‑Darmwand zu labortauglichen Zellen
Die Forschenden begannen mit kleinen Abschnitten des Maus‑Dünn‑ und Dickdarms und isolierten winzige Zellcluster, die auch Darmstammzellen enthalten. Diese Cluster, Spheroide genannt, benötigen normalerweise einen reichen Cocktail aus Wachstumsfaktoren und ein gelartiges Stützmaterial zum Überleben. Das Team nutzte ein virales Übertragungssystem, um ein Gen namens SV40 large T antigen einzuführen, das Zellen erlaubt, sich unbegrenzt weiter zu teilen, und schuf so „immortalisierte“ Linien. Anschließend entwöhnte man die Zellen schrittweise von ihrem komplexen Medium und dem Gelträger und passte sie daran an, als einfache, flache Schichten auf Standard‑Plastikgefäßen in üblichen Nährlösungen zu wachsen. Klone wurden nach ihrem Erscheinungsbild ausgewählt — entweder stärker schuppen‑/blattförmig und epithelial oder eher fibroblastär — und auf frei von gängigen Kontaminationen wie Mykoplasmen geprüft. 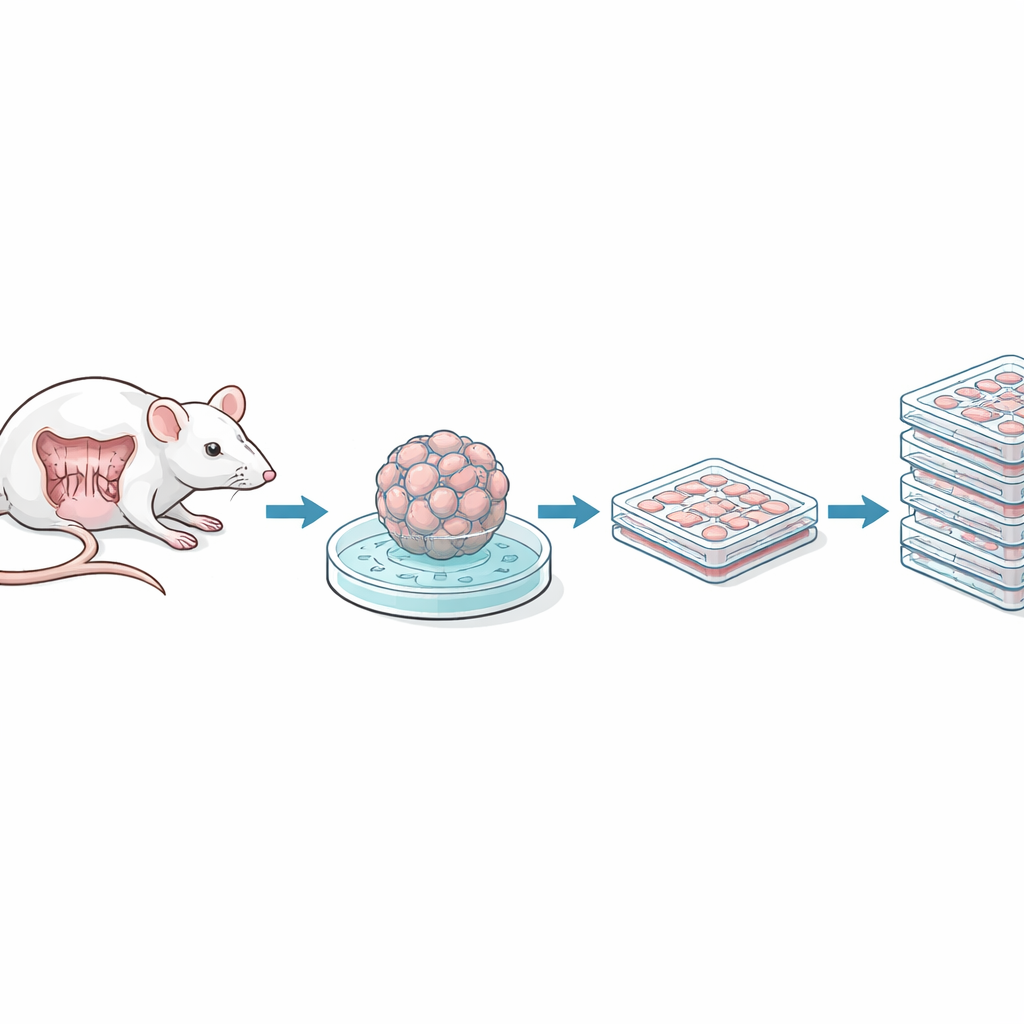
Überprüfung der Identität und genetischen Stabilität
Die Immortalisierung kann unerwünschte genetische Veränderungen einführen, daher überprüfte das Team sorgfältig, was entstanden war. Mit DNA‑Fingerprinting‑Methoden zeigten sie, dass die neuen Zelllinien weiterhin eng dem ursprünglichen C57BL/6‑Maussgewebe entsprachen und dass keine menschliche DNA eingeschleppt worden war. Chromosomenanalysen enthüllten einige zusätzliche oder umgelagerte Chromosomen, wie sie bei langkultivierten Zelllinien häufig vorkommen, doch insgesamt waren die neuen Linien weniger stark verändert als weitverbreitete Maus‑Kolonkarzinom‑Linien. In einer anspruchsvolleren Air–Liquid‑Interface‑Kultur, die normalerweise zur vollen Differenzierung des Darmepithels anregt, bildeten die immortalisierten Zellen eine einfache einschichtige Lage mit einer bürstensaumähnlichen Oberfläche, reiften jedoch nicht vollständig zu allen spezialisierten Zelltypen des nativen Darms heran. Das spricht dafür, dass sie eher aktiv teilenden Vorläuferzellen ähneln als vollständig differenzierten Zellen.
Molekulare Persönlichkeit: zwischen Epithel und Reparaturmodus
Um diese Zellen auf Genexpressions‑Ebene zu verstehen, verglich das Team deren RNA‑Profile mit denen der ursprünglichen Spheroide und mit normalen Darmzelltypen. Die immortalisierten Zellen zeigten eine Abschwächung klassischer epithelialer Marker und eine Hochregulation von Genen, die mit dem epithelial–mesenchymalen Übergang (EMT) assoziiert sind — einem Prozess, bei dem Zellen ihre Verbindungen lockern und mobiler werden, ein Zustand, der oft bei Wundheilung und in Tumoren beobachtet wird. Dennoch exprimierten sie weiterhin viele junctionale Proteine und behielten deutliche Signaturen der Herkunft aus Dünn‑ oder Dickdarm. Insgesamt ähnelten die Linien „transit amplifying“‑Vorläuferzellen — schnell teilenden Zwischenstufen zwischen Stammzellen und ausgereiften Darmzellen — und modellieren damit ein regeneratives, reparaturorientiertes Epithel.
Leicht umprogrammierbar und angreifbar durch Krankheitserreger
Ein großer Vorteil dieser neuen Linien ist ihre Bereitschaft für genetische und Umweltmanipulationen. Die Forschenden konnten DNA mit Standard‑Transfektionsreagenzien sowie mit lentiviralen Vektoren in die Zellen einbringen und starke fluoreszente Reportersignale erzeugen. Sie testeten anschließend, wie gut die Zellen Wirt–Mikroben‑Begegnungen modellieren. Bei Infektion mit Vesicular stomatitis virus unterstützten die Zellen die Virusreplikation, ließen sich aber durch eine vorbehandelnde Interferon‑Gabe dosisabhängig schützen — ein Schlüsselsignal der antiviralen Abwehr. Dieselben Zellen schalteten schnell klassische interferon‑stimulierte Gene an, was eine intakte antivirale Reaktion bestätigt. In getrennten Experimenten erlaubten die Zellen das Eindringen und Überleben von Salmonella‑Bakterien und reagierten auf bakterielle Komponenten mit Aktivierung des NF‑κB‑Wegs sowie der Sekretion einer Reihe entzündlicher Zytokine und Chemokine — Verhalten, das von einer alarmbereiten Darmbarriere zu erwarten ist. 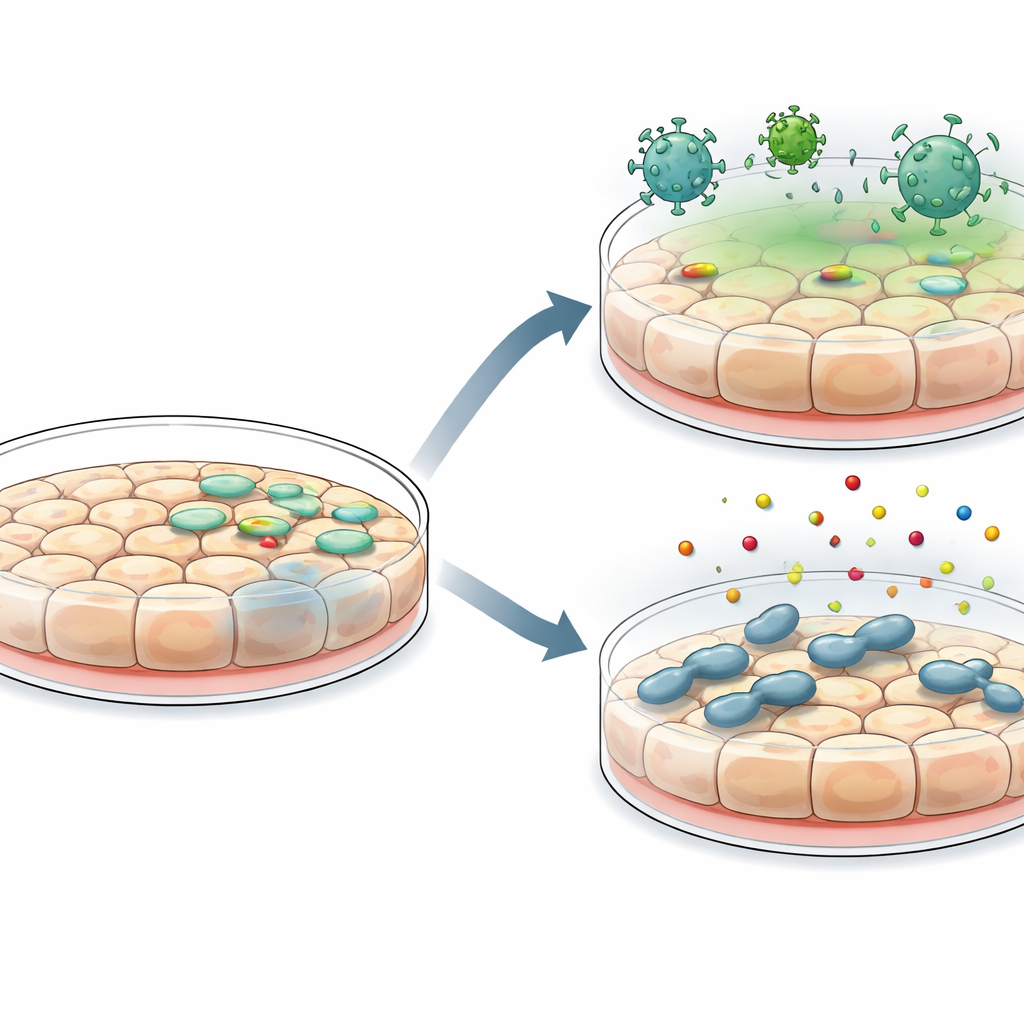
Kostensenkung und neue Möglichkeiten
Da diese immortaliserten Linien auf Standard‑Plastik in einfachem Medium wachsen, sind sie deutlich günstiger und leichter zu handhaben als dreidimensionale Mini‑Därme. Die Autorinnen und Autoren schätzen, dass ein Screening von 10.000 Verbindungen mit ihrem System um ein Vielfaches günstiger wäre als mit primären Spheroid‑ oder Organoidkulturen und zudem weniger Zeit und spezialisiertes Können erfordern würde. Zwar ahmen die Zellen nicht die volle Diversität und Struktur des nativen Darms perfekt nach und zeigen einige Merkmale teilweiser Transformation, doch sie füllen eine wichtige Lücke: eine mausbasierte, genetisch gut manipulierbare und physiologisch informierte Plattform für Hochdurchsatz‑Entdeckungen. Praktisch können diese Linien als erste, skalierbare Testumgebung dienen, wobei vielversprechende Befunde später in komplexeren Mini‑Darm‑Kulturen oder in Tiermodellen bestätigt werden sollten.
Was das für die Darmforschung bedeutet
Kurz gesagt liefert die Studie eine neue Reihe von Maus‑Darmzelllinien, die leicht zu kultivieren, einfach zu gentechnisch zu verändern und gegenüber Viren, Bakterien und Immun‑Signalen reaktionsfähig sind — auf eine Weise, die echtes Darmgewebe widerspiegelt. Sie liegen zwischen einfachen, aber schlecht definierten Krebszelllinien und anspruchsvollen, aber sehr realistischen Organoid‑Systemen. Indem sie technische und finanzielle Hürden senken, könnten diese immortalisierten Darmepithelzellen die Forschung zu Darmentwicklung, Infektion, Entzündung und Arzneimittelantworten beschleunigen und Forschenden ermöglichen, schneller von Grundlagenfragen zu Ergebnissen zu gelangen, die in höher‑aufgelösten Modellen und schließlich in lebenden Organismen getestet werden können.
Zitation: Zhou, J.Y., Espenschied, S.T., Lu, Q. et al. Development and characterization of immortalized mouse intestinal epithelial cell lines. Sci Rep 16, 8297 (2026). https://doi.org/10.1038/s41598-026-38295-z
Schlüsselwörter: Darmepithelzellen, immortalisierte Zelllinien, Maus‑Darm‑Modelle, Wirt–Pathogen‑Interaktionen, angeborene Immunität