Clear Sky Science · de
Genomanalyse von ST117, 155, 1011, 167, 744 und 17391 in multiresistenten, mit Geflügel assoziierten Escherichia-coli-Isolaten aus Indien
Warum Geflügelfarmen Ihre Gesundheit betreffen
Huhn ist eines der weltweit beliebtesten Fleischprodukte, und die Geflügelindustrie in Indien wächst schnell, um die Nachfrage zu decken. Neben günstigem Protein gibt es jedoch ein stilles Problem: Einige Bakterien auf Geflügelfarmen werden gegen viele der Antibiotika resistent, auf die Ärztinnen und Ärzte zur Behandlung von Infektionen beim Menschen angewiesen sind. Diese Studie untersucht multiresistente Escherichia coli (E. coli) von Geflügelfarmen im Süden Indiens eingehend, um zu verstehen, wie verbreitet sie sind, welche Faktoren sie gefährlich machen und wie sie von Ställen und Einstreu in die weitere Umwelt und schließlich in menschliche Gemeinschaften gelangen könnten.
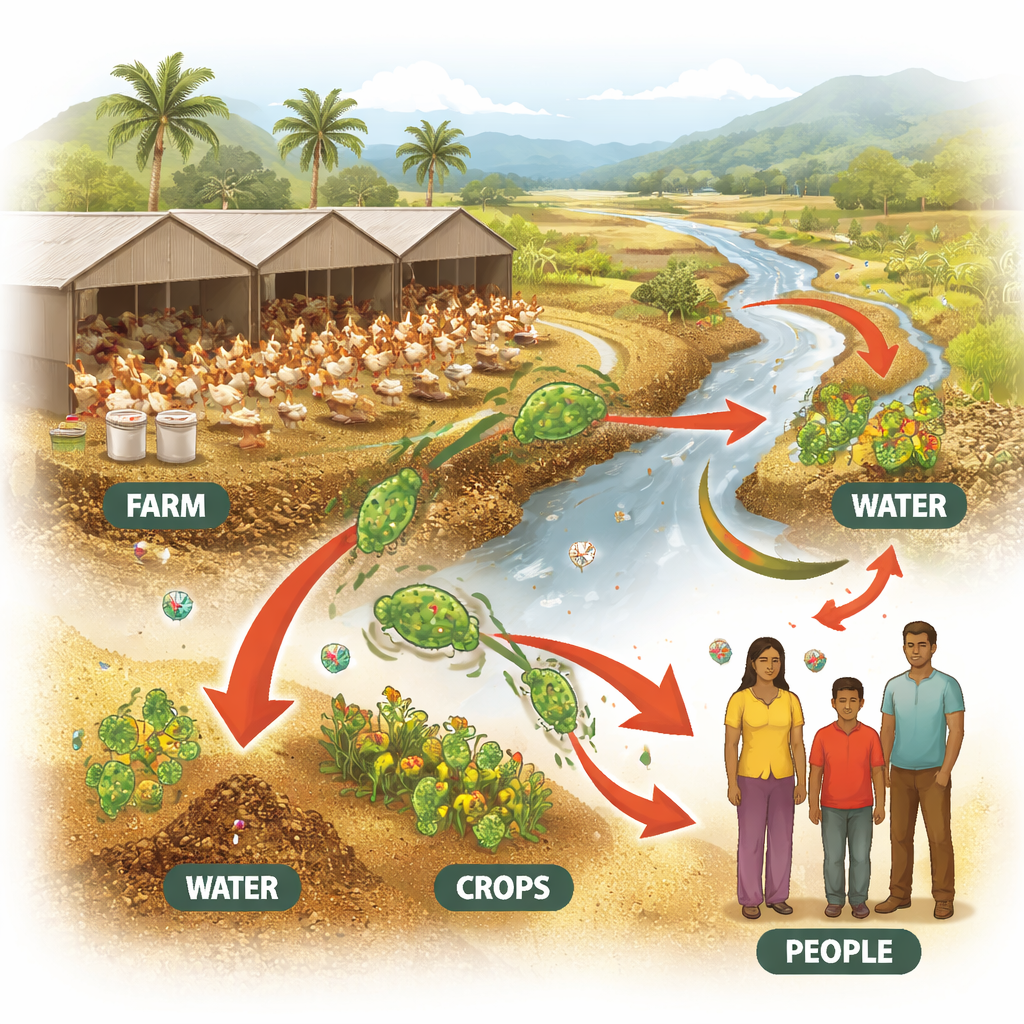
Untersuchung von verschmutzter Einstreu und Farmwasser
Die Forscher sammelten 38 Proben von Einstreu und Trinkwasser auf sieben Geflügelfarmen in Tamil Nadu. Dort vermischen sich Vogelkot, Futterreste und verschüttetes Wasser – ideale Bedingungen für Bakterien, um zu wachsen und genetisches Material auszutauschen. Labortests zeigten, dass viele E. coli aus diesen Proben mehreren gängigen Antibiotikaklassen widerstehen konnten, darunter Penicilline, Cephalosporine, Fluorchinolone und Tetracyclin. Im Durchschnitt war jeder Stamm gegen mehr als die Hälfte der getesteten Wirkstoffe resistent, ein Warnsignal dafür, dass in diesen Beständen Antibiotika intensiv und wiederholt eingesetzt werden.
Lesen der Bedienungsanleitungen der Bakterien
Um zu verstehen, warum diese Bakterien so schwer zu töten sind, sequenzierten die Forschenden die gesamten DNA-Sequenzen von sieben der resistentesten E.-coli-Stämme – eine Art komplettes Handbuch für jedes Mikrobenexemplar. Sie entdeckten viele bekannte Resistenzgene, unter anderem solche, die gegen Tetracyclin, Fluorchinolone und mehrere andere Antibiotikafamilien schützen. Einige Stämme trugen potente Beta-Laktamasen-Gene wie CTX-M und TEM-1B, die eine große Gruppe penicillinähnlicher Wirkstoffe neutralisieren können, die Ärztinnen und Ärzte häufig bei schweren Infektionen einsetzen. Die Bakterien trugen außerdem kleine zusätzliche DNAstrukturen, sogenannte Plasmide, die zwischen Bakterien wandern können und die rasche Verbreitung von Resistenzmerkmalen auf einer Farm begünstigen.
Globale Störenfriede in indischen Hühnerställen
Beim Vergleich dieser E. coli mit weltweit berichteten Stämmen gehörten mehrere zu sogenannten „pandemischen“ Linien – genetischen Familien, die sowohl bei Tieren als auch beim Menschen mit Krankheiten in Verbindung gebracht werden. Dazu zählten ST117, ST167 und ST744, die in Nutz- und Klinikpatienten sowie in Umweltproben aus vielen Ländern nachgewiesen wurden. Noch besorgniserregender war der Nachweis eines bisher neuen genetischen Typs, ST17391, in der Einstreu einer Farm. Dieser Stamm trug Gene, die ihm Mehrfachresistenzen verleihen und möglicherweise seine Besiedlungsfähigkeit in Tieren oder Menschen verbessern. Solche Hochrisikolinien bereits in Routinematerial von Farmen zu finden, legt nahe, dass Geflügelbetriebe als stille Knotenpunkte für Bakterien dienen können, die bereits für schwer behandelbare Krankenhausinfektionen bekannt sind.
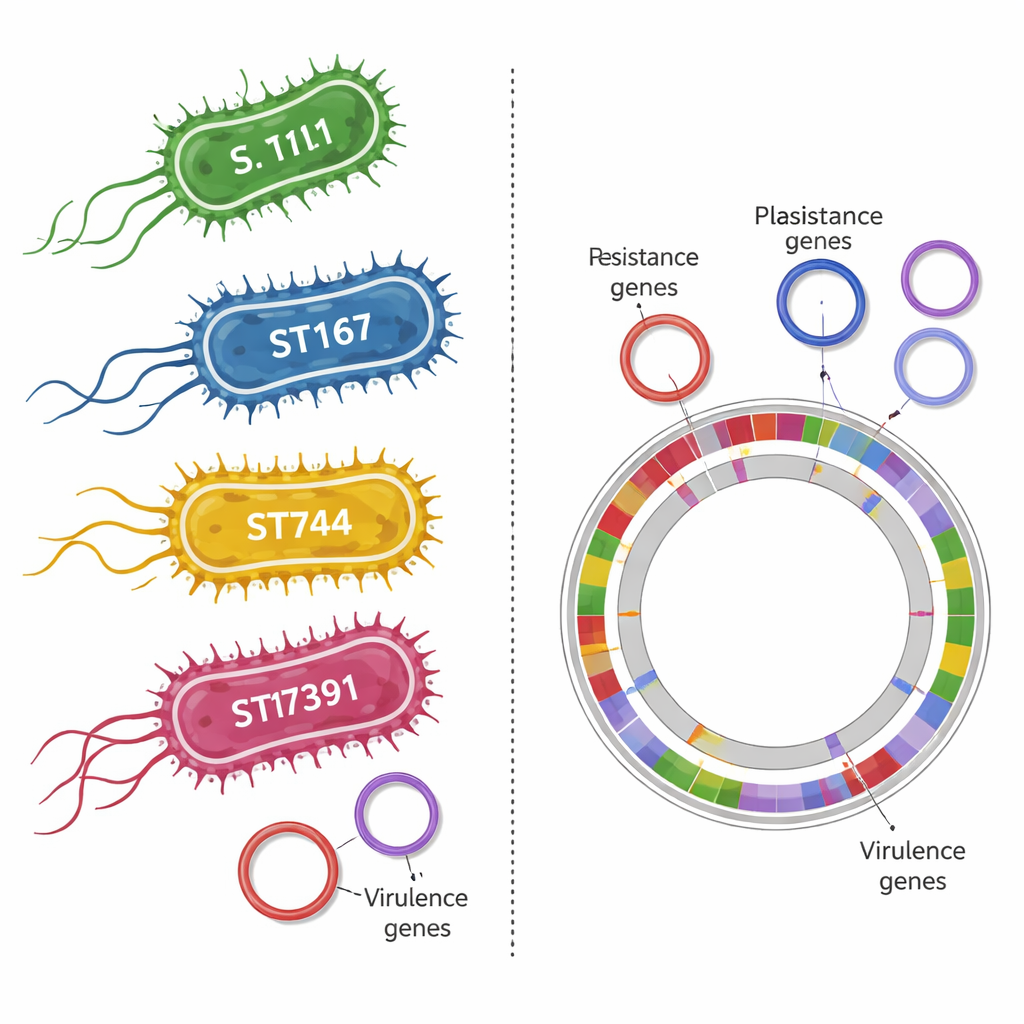
Verborgene Helfer, die Bakterien schädlicher machen
Die DNA-Analysen zeigten nicht nur Resistenzgene, sondern auch Virulenzgene – Merkmale, die E. coli helfen, an Geweben zu haften, dem Wirt Eisen zu entziehen und Angriffen des Immunsystems zu trotzen. Viele Stämme trugen Kombinationen dieser Faktoren, was darauf hindeutet, dass sie keine harmlosen Begleiter sind. In einem Fall gingen die Wissenschaftler über Einzestämme hinaus und sequenzierten alle DNA-Komponenten einer Einstreuprobe von einer Farm mit einem besonders bedenklichen E.-coli-Typ. Dieses metagenomische Abbild zeigte eine dichte Gemeinschaft von Mikroben, die Gene gegen mehrere Antibiotikaklassen tragen. Effektiv fungierte die Einstreu als genetischer Marktplatz, auf dem Resistenzmerkmale gespeichert und zwischen vielen Arten geteilt werden.
Was das für Farmen, Lebensmittel und Familien bedeutet
Für Nichtfachleute ist die Botschaft klar: Wie wir Hühner halten, kann die Wirksamkeit von Antibiotika in der Humanmedizin beeinflussen. Der routinemäßige Einsatz dieser Wirkstoffe in der Geflügelhaltung begünstigt die Selektion von E. coli, die potente Resistenzgene und Virulenzfaktoren tragen, und diese können auf kontaminierter Einstreu, in Abwässern oder entlang der Lebensmittelkette von der Farm gelangen. Die Autorinnen und Autoren der Studie plädieren für einen One-Health-Ansatz, der menschliche, tierische und ökologische Gesundheit als eng verknüpft betrachtet. Sie fordern bessere Abfallwirtschaft, strengere Regeln für den Antibiotikaeinsatz in der Tierhaltung und breitere, DNA-basierte Überwachung zur Verfolgung gefährlicher bakterieller Linien. Diese Maßnahmen seien notwendig, um alltägliche Infektionen behandelbar zu halten und Antibiotika für künftige Generationen zu schützen.
Zitation: P, R., Srijith, L., G, K. et al. Genomic analysis of ST117, 155, 1011, 167, 744, and 17391 in poultry-associated multidrug resistant Escherichia coli isolates from India. Sci Rep 16, 7438 (2026). https://doi.org/10.1038/s41598-026-38232-0
Schlüsselwörter: antimikrobielle Resistenz, Geflügelhaltung, Escherichia coli, One Health, Ganzgenomsequenzierung