Clear Sky Science · de
PERK-Inhibition dämpft multiplen programmierten Zelltod durch Aktivierung von Nrf2/HO-1 bei diabetischer Retinopathie mit integrierter Proteomik und funktionaler Validierung in HRECs
Warum der Schutz des Sehvermögens bei Diabetes wichtig ist
Für Millionen von Menschen mit Diabetes ist eine der gefürchtetsten Komplikationen der schrittweise Verlust des Sehvermögens, bekannt als diabetische Retinopathie. Diese Schädigung des lichtempfindlichen Gewebes im hinteren Teil des Auges beginnt oft unauffällig, lange bevor Symptome auftreten. Die Studie hinter diesem Artikel untersucht, was genau die winzigen Blutgefäßzellen tötet, die die Netzhaut gesund halten — und testet eine neue Möglichkeit, sie zu schützen. Indem Forscher die durch hohen Blutzucker ausgelösten zellulären „Stressreaktionen“ besser verstehen und dämpfen, hoffen sie, die Erblindung bei Menschen mit Diabetes zu verlangsamen oder sogar zu verhindern.
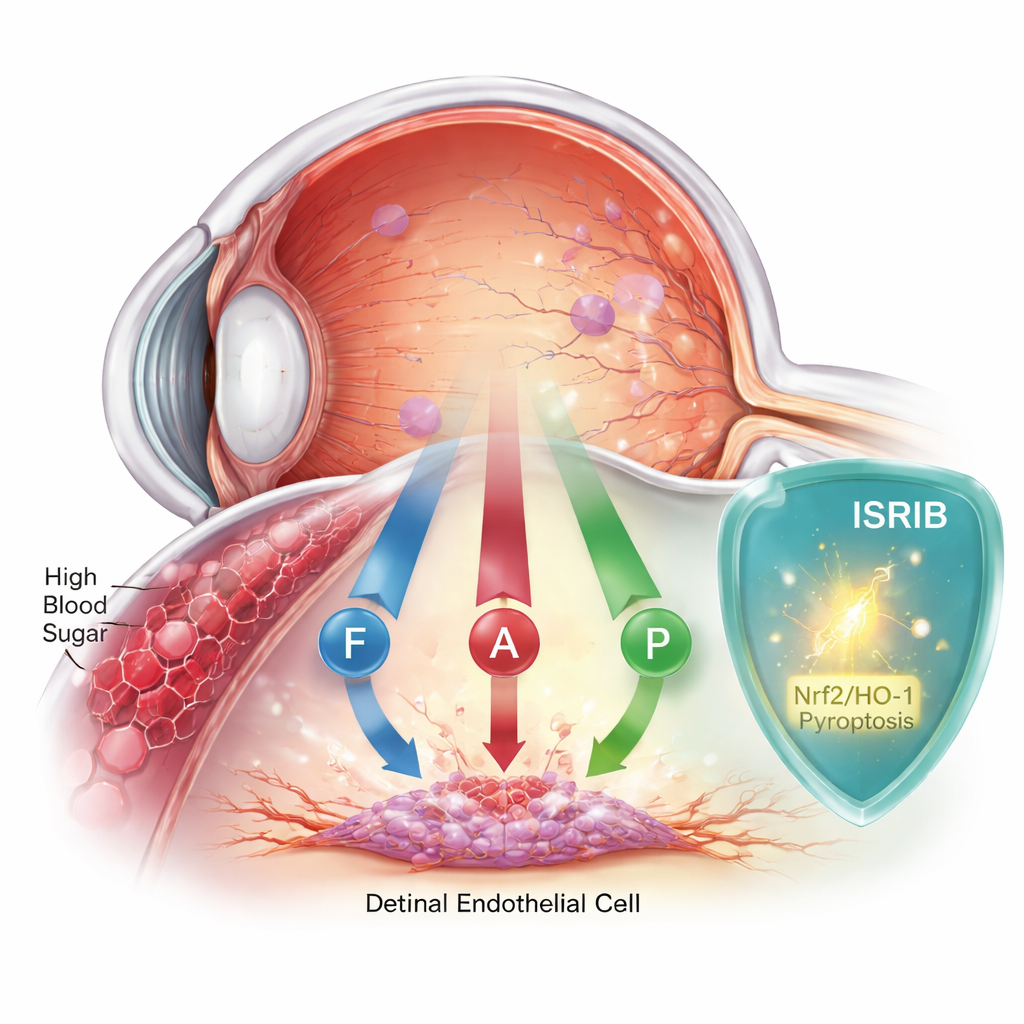
Wenn Blutzucker das Auge still verletzt
Die diabetische Retinopathie beginnt, wenn hoher Blutzucker die empfindliche innere Auskleidung der retinalen Blutgefäße schädigt. Diese Zellen bilden eine Barriere, die die Netzhaut ernährt und schützt. Jahrelang gingen Wissenschaftler davon aus, dass vor allem eine Form des Zelltods, die Apoptose, verantwortlich sei. Zunehmende Hinweise deuten jedoch darauf hin, dass die Lage komplizierter ist. Das Team konzentrierte sich auf humanen retinalen Endothelzellen, die im Labor gezüchtet und Zuckerspiegeln ausgesetzt wurden, wie sie bei schlecht eingestelltem Diabetes vorkommen, und beobachtete, wie die Zellen über zwei Tage reagierten.
Drei Wege, auf denen Zellen gleichzeitig sterben können
Mit einer leistungsfähigen Proteinmessmethode, der Proteomik, fanden die Forschenden heraus, dass hohe Zuckerspiegel Hunderte von Proteinen störten, insbesondere solche, die an Stressreaktionen, Stoffwechsel und Eisenhaushalt beteiligt sind. Folgeuntersuchungen zeigten, dass die Zellen nicht nur auf einem Weg starben, sondern auf dreien: klassischer programmierter Zelltod (Apoptose), einer feurigen, entzündungsassoziierten Form (Pyroptose) und einer neueren, eisengetriebenen Form namens Ferroptose. Marker oxidativer Schäden, Eisenüberladung und erschöpfter Antioxidantien stiegen alle an, während schützende Enzyme sanken. Zusammen ergab das Bild von Zellen, die von Stress, Entzündung und toxischer Anhäufung reaktiver Moleküle überwältigt waren.
Ein Stressschalter im Zentrum des Problems
Das Team richtete den Blick dann auf einen wichtigen Stresssensor in den Zellen namens PERK, der an der Membran des endoplasmatischen Retikulums sitzt, einer Struktur, die beim Falten und Verarbeiten von Proteinen hilft. Unter hohen Zuckerkonditionen wurde PERK überaktiv — wie ein klemmender Notfallalarm, der weiter schrillt. Dies schien in alle drei Todesprogramme hinein zu wirken. Gleichzeitig war ein natürlicher Abwehrmechanismus, der normalerweise Zellen vor oxidativen Schäden schützt — der Nrf2/HO-1-Antioxidansweg — geschwächt. Einfach gesagt: Die Gefahrensignale waren hochgedreht, während die inneren Feuerlöscher heruntergeregelt waren.
Stress dämpfen, Schutz hochfahren
Um zu prüfen, ob sie diesen zerstörerischen Kreislauf durchbrechen konnten, behandelten die Forschenden die Hochzucker-Zellen mit ISRIB, einem kleinen Molekül, das PERKs Stresssignalisierung effektiv abschwächt. Die Ergebnisse waren eindrücklich. ISRIB verbesserte das Überleben der Zellen, reduzierte Marker eisengetriebener Schäden und oxidativen Stresses und senkte chemische Hinweise sowohl auf Apoptose als auch auf Pyroptose. Gleichzeitig stärkte es den Nrf2/HO-1-Abwehrweg und half den Zellen, ihre antioxidative Kapazität wiederherzustellen. Ein weiteres Medikament, das gezielt Ferroptose blockiert, war ebenfalls hilfreich, doch ISRIB stach hervor, weil es alle drei Todeswege zugleich beruhigte, statt nur einen einzelnen.
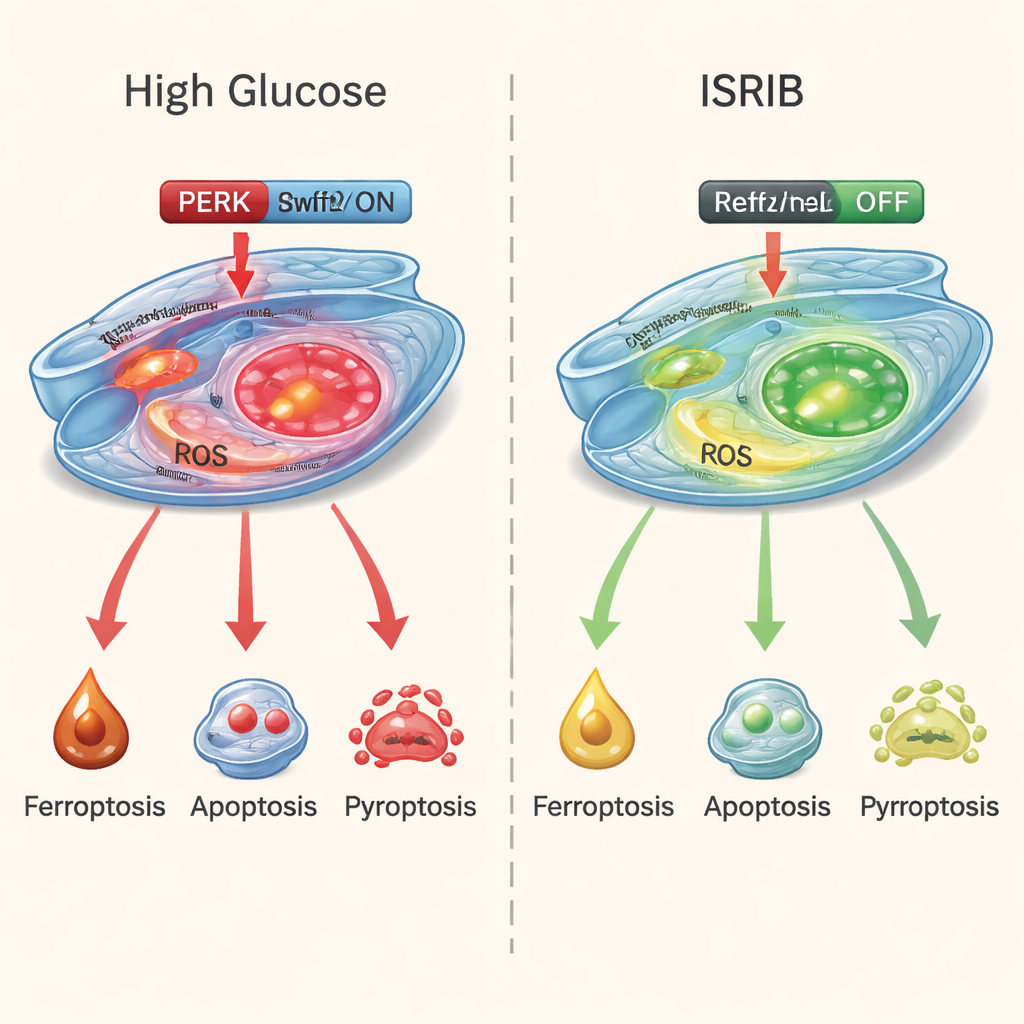
Was das für Menschen mit Diabetes bedeuten könnte
Diese Arbeit legt nahe, dass frühe Schäden bei der diabetischen Retinopathie nicht durch einen einzelnen „Bösewicht“ verursacht werden, sondern durch das Zusammenwirken mehrerer sich selbst verstärkender Todesprogramme, die durch chronischen zellulären Stress angetrieben werden. Indem man den PERK-Stressschalter herunterregelt und die eigenen Schutzmechanismen der Zelle reaktiviert, könnten Medikamente wie ISRIB einen einheitlicheren Weg bieten, die retinalen Blutgefäße am Leben zu erhalten. Obwohl diese Experimente an Zellen und noch nicht am Menschen durchgeführt wurden, weisen sie auf künftige Behandlungen hin, die Stressreaktionen im Auge gezielt adressieren — potenziell als zusätzliche Schutzschicht neben Blutzuckerkontrolle und den derzeitigen Injektionen ins Auge, um das Sehvermögen bei Diabetes zu erhalten.
Zitation: Xie, L., Zhang, X., Tian, M. et al. PERK inhibition attenuates multi-program cell death through Nrf2/HO-1 activation in diabetic retinopathy with integrated proteomics and functional validation in HRECs. Sci Rep 16, 7225 (2026). https://doi.org/10.1038/s41598-026-38213-3
Schlüsselwörter: diabetische Retinopathie, retinaler Zelltod, oxidativer Stress, PERK-Signalweg, Nrf2 HO-1