Clear Sky Science · de
Hemmung des SHH-Signalwegs und Ko-Kultur mit Astrozyten rufen unterschiedliche Reaktionen in Glioblastom- und Krebsstammzellen hervor
Warum Hirntumoren so schwer zu behandeln sind
Das Glioblastom gehört zu den tödlichsten Hirntumoren, und selbst mit Operation, Bestrahlung und Chemotherapie überleben nur wenige Patienten mehr als fünf Jahre. Ein Grund dafür ist, dass diese Tumoren nicht aus nur einer Zellart bestehen. Sie enthalten eine kleine Gruppe besonders hartnäckiger „Krebsstamm“zellen, die Behandlungen überdauern und dem Tumor helfen können, wieder nachzuwachsen. Diese Studie stellt eine zentrale Frage: Wie reagieren diese unterschiedlichen Tumorzellen, wenn ein wachstumsförderndes Signal blockiert wird, und wie verändert die Anwesenheit normaler Gehirnstützzellen, der Astrozyten, diese Reaktion?
Ein genauerer Blick auf die härtesten Tumorzellen
Die Forschenden arbeiteten mit zwei Hauptzelltypen aus einem gängigen Glioblastom-Modell: den Massen–Tumorzellen und einer winzigen Unterpopulation, die durch das Protein CD133 markiert ist und sich wie Krebsstammzellen verhält. Diese stammähnlichen Zellen teilten sich weniger, erschienen kleiner und runder und bildeten dichtere Cluster als die Massen–Zellen. Das Team kultivierte die Tumorzellen außerdem zusammen mit Astrozyten, den sternförmigen Zellen, die das gesunde Hirngewebe unterstützen. Diese Mischkultur bildet die tatsächliche Tumorumgebung besser nach, in der Krebszellen ständig mit ihren Nachbarn „kommunizieren“. 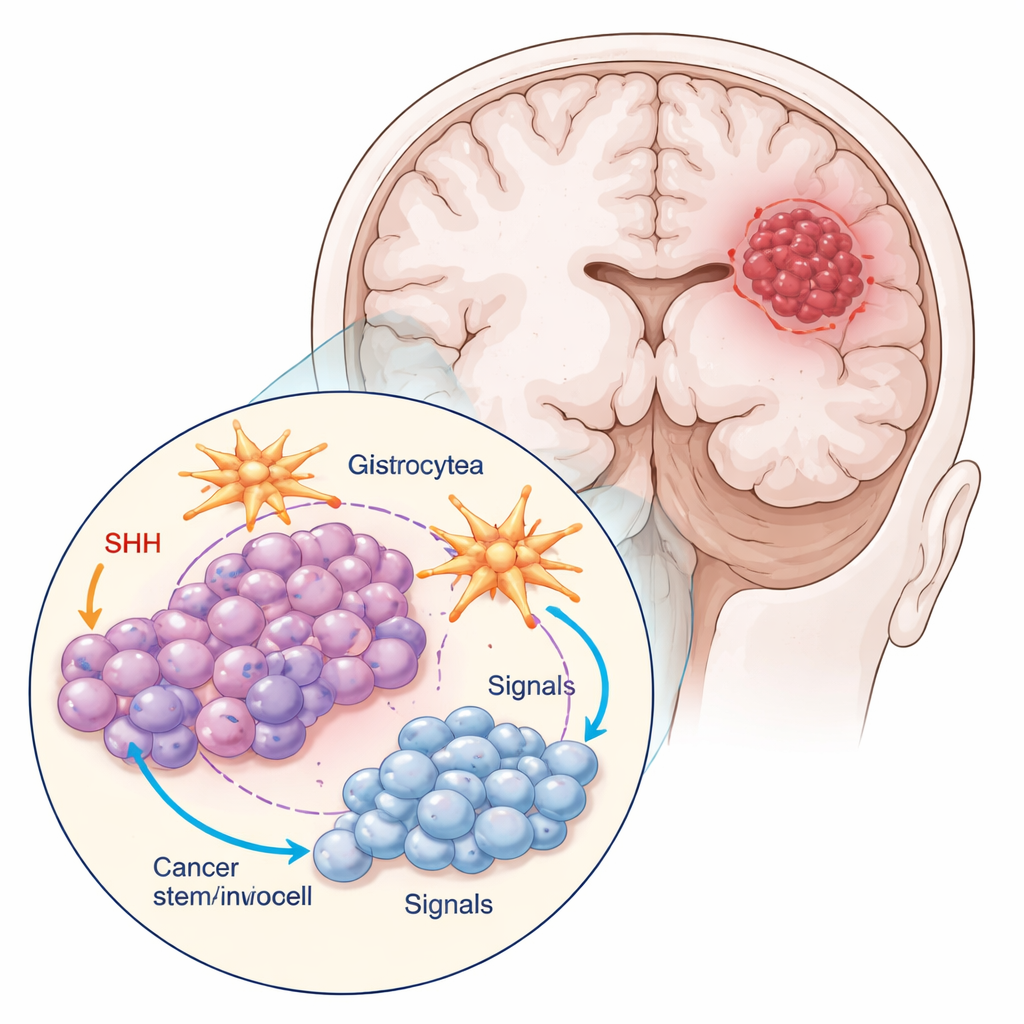
Blockade eines Entwicklungs‑Signals, das Tumoren wiederverwenden
Viele Glioblastome, insbesondere ihre stammähnlichen Zellen, kapern eine molekulare Kommunikationsstrecke namens Sonic‑Hedgehog (SHH), die normalerweise während der Gehirnentwicklung aktiv ist. Das Team setzte Cyclopamin ein, eine Verbindung, die eine Schlüsselkomponente des SHH‑Weges blockiert, um zu untersuchen, wie sowohl Massen‑Tumorzellen als auch Krebsstammzellen reagieren. Sie maßen die Aktivität SHH‑bezogener Gene und Proteine, die Geschwindigkeit des Zellzyklusfortschritts und die Häufigkeit programmierten Zelltods (Apoptose). Cyclopamin veränderte die SHH‑Signalgebung auf eine Weise, die stark vom Zelltyp und davon abhängte, ob Astrozyten vorhanden waren. Krebsstammzellen produzierten am meisten SHH, wenn sie allein kultiviert wurden, doch diese Ausschüttung sank, wenn sie zusammen mit Astrozyten und unter Behandlung mit dem Wirkstoff wuchsen — ein Hinweis darauf, dass die umgebenden Gehirnzellen die chemische „Selbstunterstützung“ des Tumors dämpfen können.
Wie die Nachbarschaft Wachstum und Tod verschiebt
Über SHH hinaus verfolgte das Team andere Gen-Netzwerke, die bestimmen, ob Zellen weiter teilen, pausieren oder zu spezialisierteren Zuständen übergehen. In einfachen, nur aus Tumorzellen bestehenden Kulturen drängte die SHH‑Blockade die Massen‑Zellen eher in einen Stillstand in der späten Teilungsphase (G2/M), während sich die stammähnlichen Zellen tendenziell früher ansammelten, in der Ruhe‑ oder Eintrittsphase (G0/G1). Mit hinzugefügten Astrozyten änderten sich diese Muster: Krebsstammzellen, die zuvor ruhiger waren, verschoben sich hin zu einer G2/M‑Arretierung, was auf ein anderes Set von „Bremsen“ in der gemischten Umgebung hindeutet. Die Forschenden beobachteten außerdem, dass Signale, die Zellschicksal und Gewebeformung steuern — etwa WNT-, BMP‑ und TGF‑β‑Wege — in Massen‑ und stammähnlichen Zellen unterschiedlich reguliert wurden, wenn Astrozyten anwesend waren. Das bedeutet, die Mikroumgebung kann Zellen eher zu weiterem Stamm‑ähnlichen Verhalten oder zu einem differenzierteren, weniger aggressiven Zustand neigen lassen.
Den Zelltod in den widerstandsfähigsten Zellen auslösen
Die Studie untersuchte außerdem, wie leicht Zellen in die Apoptose gehen. Genetische Auslese und ein DNA‑Schadens‑Test (TUNEL‑Assay) zeigten, dass Cyclopamin eine „extrinsische“ Todesroute begünstigte, die von einem Protein namens CASP8 getrieben wird, besonders in der Population der Krebsstammzellen. Interessanterweise nahm in allein kultivierten Tumorzellen der Gesamttod nach SHH‑Blockade manchmal ab, was darauf hindeutet, dass diese Zellen alternative Überlebensstrategien aktivieren können. Im Gegensatz dazu erhöhte Cyclopamin bei stammähnlichen Zellen in Ko‑Kultur mit Astrozyten die Apoptosemarker, was darauf hinweist, dass die umgebenden Gehirnzellen diese ansonsten hartnäckigen Zellen verletzlicher machen, sobald SHH‑Signalgebung blockiert ist. 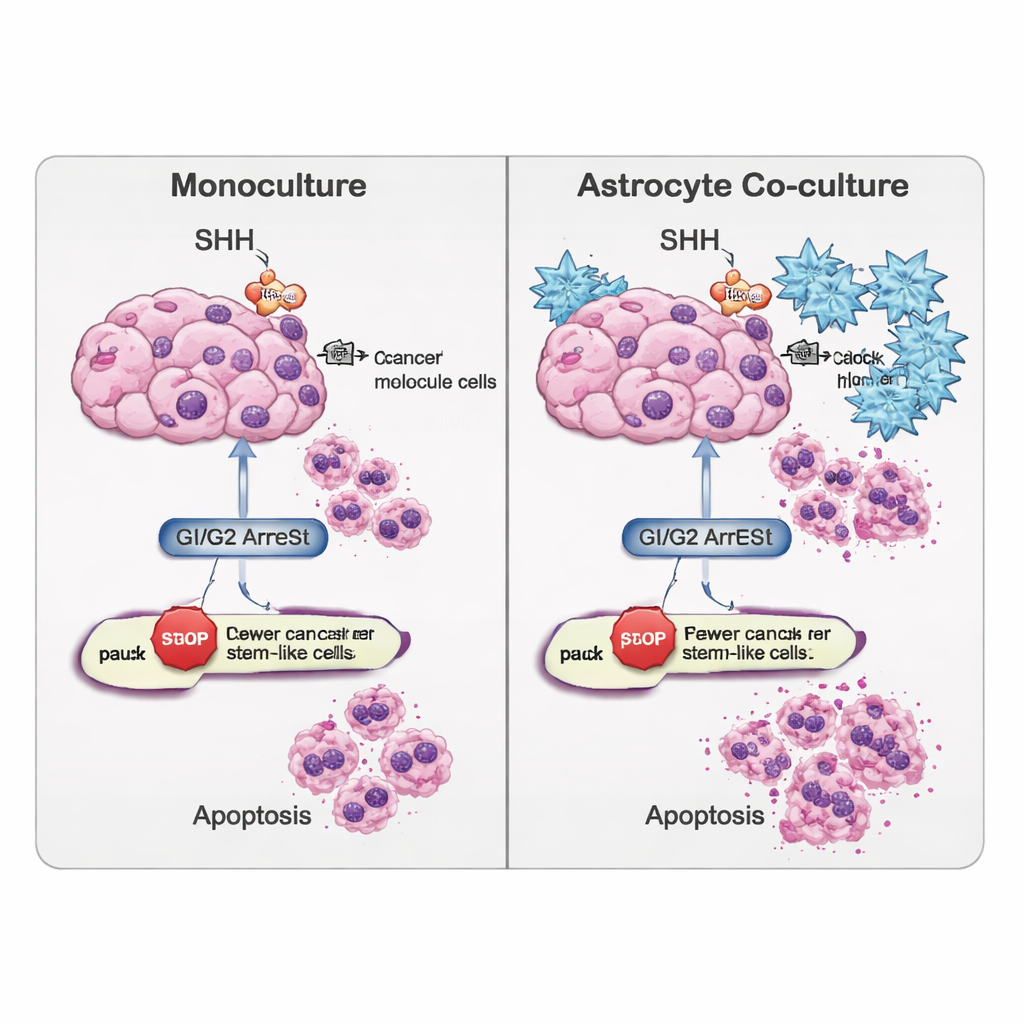
Was das für künftige Hirnkrebsbehandlungen bedeutet
Für Nicht‑Fachleute ist die Kernbotschaft: Auf ein einzelnes Wachstumssignal im Glioblastom zu zielen, reicht nicht aus, wenn wir die Tumornachbarschaft ignorieren. Diese Arbeit zeigt, dass Astrozyten — die normalen Zellen, die den Raum mit dem Tumor teilen — die Reaktion von sowohl Massen‑Krebszellen als auch Krebsstammzellen auf die Blockade des SHH‑Weges grundlegend verändern können. Insbesondere wurden Krebsstammzellen in Anwesenheit von Astrozyten eher zu Zellzyklusarrest und zu einer Form des Zelltods geneigt. Die Autoren schließen daraus, dass Wirkstoffe, die auf SHH und verwandte Wege abzielen, eher funktionieren, wenn sie in Modellen getestet und später angewendet werden, die die reale Gehirnumgebung besser widerspiegeln — möglicherweise in Kombination mit anderen Therapien, die die Backup‑Überlebenswege des Tumors angreifen. Kurz: Das Verstehen und Ausnutzen der „Kommunikation“ zwischen Tumorzellen und ihren Nachbarn könnte präzisere und dauerhaftere Strategien gegen diesen sonst unerbittlichen Krebs eröffnen.
Zitation: Kocaturk, D.C., Ozdil, B., Adali, Y. et al. SHH pathway inhibition and astrocyte co-culture induce distinct responses in glioblastoma and cancer stem cells. Sci Rep 16, 7712 (2026). https://doi.org/10.1038/s41598-026-38199-y
Schlüsselwörter: Glioblastom, Krebsstammzellen, Sonic-Hedgehog-Signalweg, Tumormikroumgebung, Astrozyten