Clear Sky Science · de
Identifizierung und Validierung einer neuartigen ferroptosebezogenen Gen-Signatur, die mit erblich bedingter Netzhautdegeneration bei Rd10-Mäusen assoziiert ist
Warum sterbende Augen-Zellen uns alle betreffen
Retinitis pigmentosa ist eine Gruppe erblicher Augenkrankheiten, die den Sehsinn allmählich rauben — häufig beginnend mit Nachtblindheit und endend im vollständigen Sehverlust. Es gibt keine Heilung, und bestehende Gentherapien helfen nur einem kleinen Teil der Patienten. Diese Studie verfolgt einen anderen Ansatz: eine spezielle Form des Zelltods namens Ferroptose, angetrieben von Eisen und oxidativem Stress, zu untersuchen, um neue Genziele zu finden, die eines Tages die lichtempfindlichen Zellen der Netzhaut schützen könnten — unabhängig davon, mit welcher Mutation eine Person geboren wurde.
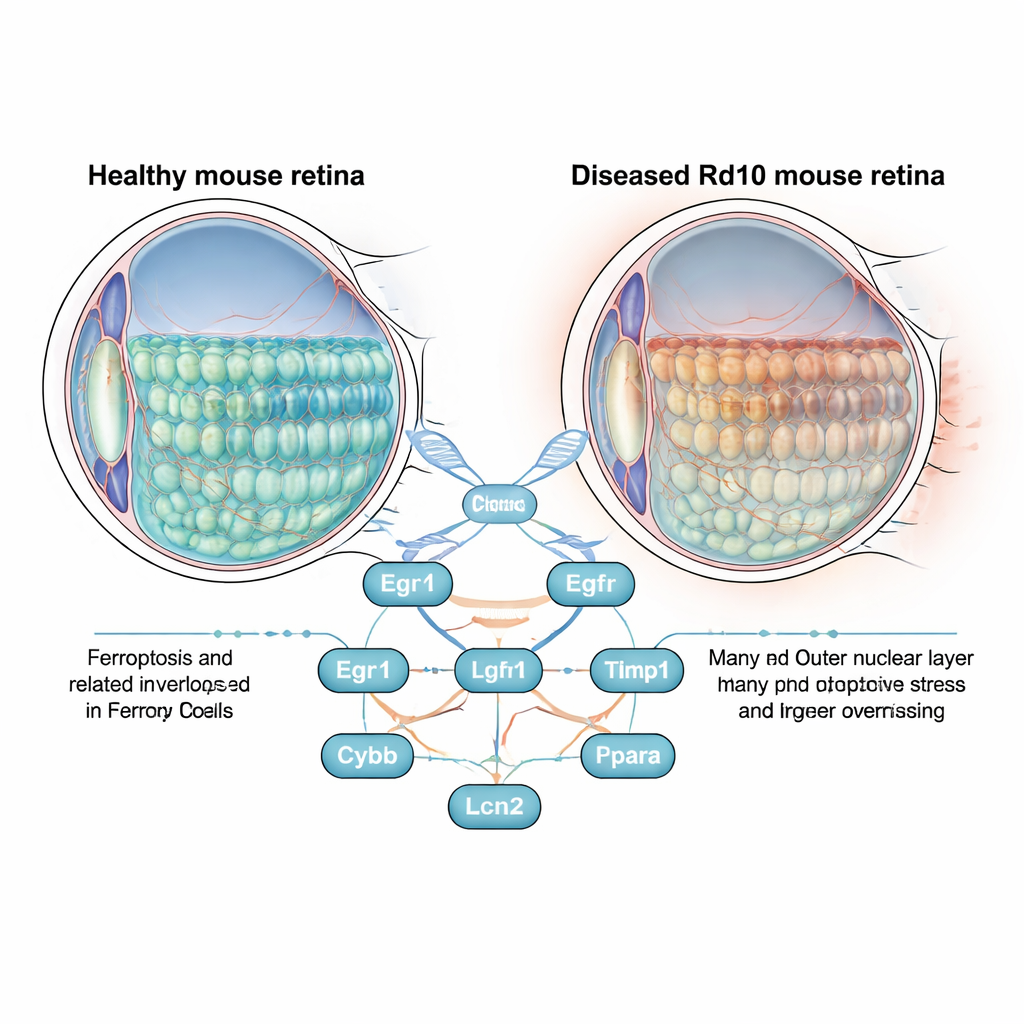
Ein genauerer Blick auf eine erblindende Erkrankung
Die Netzhaut ist eine dünne Gewebeschicht im Augenhintergrund, die Stäbchen- und Zapfenphotorezeptoren beherbergt — die Zellen, die Licht in elektrische Signale umwandeln. Bei Retinitis pigmentosa sterben diese Zellen langsam ab, wodurch zunächst Nacht- und Seitenblick verloren gehen und später das zentrale Sehen. Wissenschaftler untersuchen diesen Prozess oft in Rd10-Mäusen, die eine Mutation tragen, die der menschlichen Krankheit nahekommt. Anstatt sich nur auf das fehlerhafte Gen zu konzentrieren, stellten die Autoren eine breitere Frage: Wenn die Netzhaut degeneriert, welche mit Ferroptose verknüpften Gene werden an- oder abgeschaltet, und könnten sie den Zelltod antreiben?
Die Schlüsselgene in einem Meer von Daten finden
Das Team analysierte große öffentliche Genexpressionsdatensätze aus gesunden und Rd10-Mausnetzhauten und erstellte gewissermaßen einen globalen »Schnappschuss« darüber, welche Gene stärker oder schwächer aktiv sind. Sie identifizierten über 2.000 veränderte Gene und kreuzprüften diese dann mit einer kuratierten Liste ferroptosebezogener Gene. Das reduzierte das Feld auf 37 Kandidaten, die mit eisengetriebenem, oxidativem Zelltod in Verbindung stehen. Computergestützte Analysen zeigten, dass diese Gene in Prozessen wie Reaktion auf oxidativen Stress, Regulation des neuronalen Zelltods und Lipidstoffwechselwegen gehäuft auftreten — Kennzeichen der Ferroptose und bekannte Stressreaktionen in degenerierenden Nerven.
Acht Gene, die herausragen
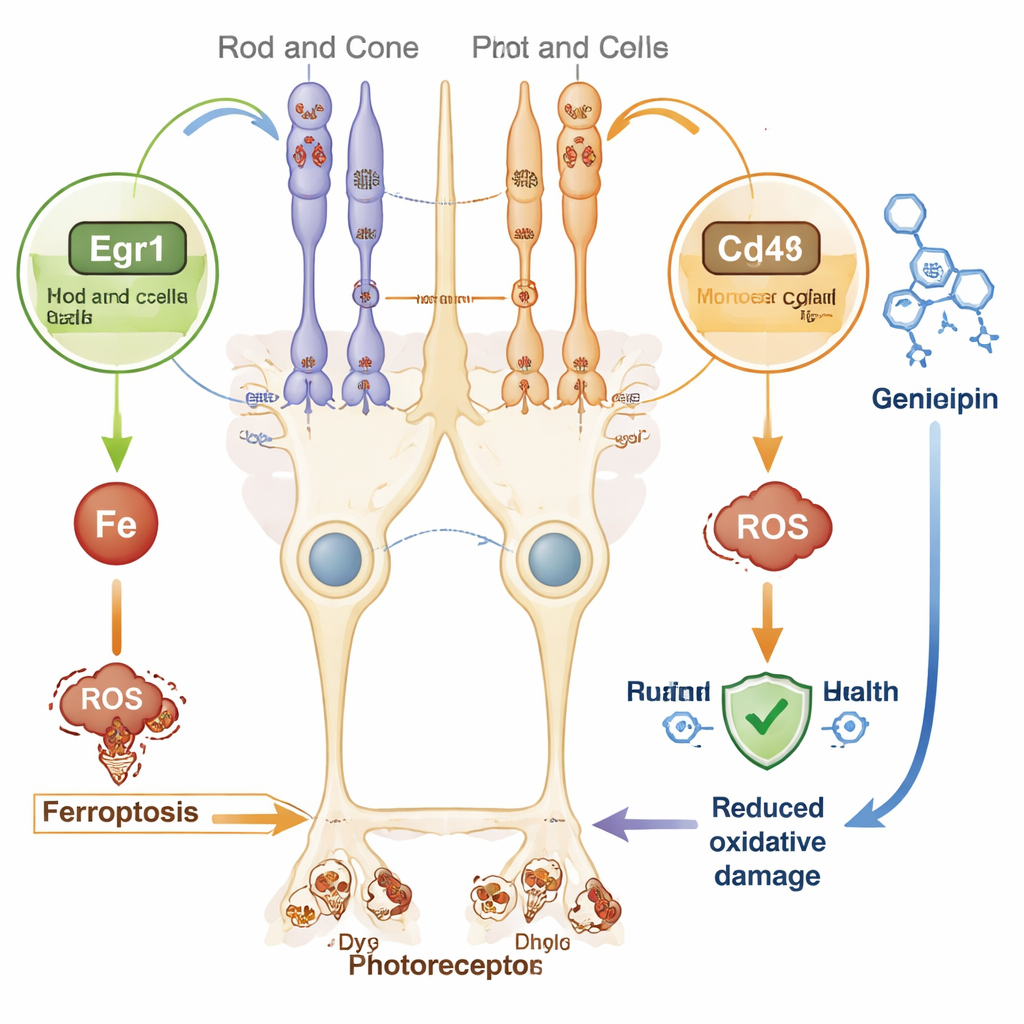
Um die einflussreichsten Akteure zu bestimmen, bauten die Forscher ein Protein-Interaktionsnetzwerk auf und wandten mehrere Rangfolgealgorithmen an. Acht »Hub«-Gene traten zutage: Egr1, Cd44, Egfr, Tlr4, Timp1, Cybb, Lcn2 und Ppara. Sieben davon waren in erkrankten Netzhauten stärker aktiv, während Ppara weniger aktiv war. Die Gruppe bestätigte diese Muster in einem unabhängigen Datensatz und untersuchte dann genauer, wo die Top-Gene im Auge vorkommen. Mit fluoreszierender Färbung und Einzelzell-RNA-Sequenzierung zeigten sie, dass Egr1 in Stäbchen- und Zapfenphotorezeptoren stark erhöht ist, während Cd44 in Müller-Zellen, den stützenden Gliazellen der Netzhaut, deutlich ansteigt. Das deutet darauf hin, dass gestresste Photorezeptoren und ihre Stütz-Zellen möglicherweise über ferroptose-verbundene Wege zusammenwirken — vielleicht zum Nachteil der Zellen.
Was das für zukünftige Behandlungen bedeutet
Da gentherapeutische Ansätze, die auf jedes fehlerhafte Gen zugeschnitten sind, komplex und teuer sind, erscheinen breit wirkende Strategien attraktiv. Die neu identifizierte Gen-Signatur deutet auf mehrere solche Wege hin. Beispielsweise ist Egr1 ein schnell reagierender Schalter, der auf oxidativen Stress anspricht und in anderen Organen Ferroptose fördern kann. Cd44, ein Oberflächenmolekül auf Müller-Zellen, wurde in verschiedenen Geweben mit verschlechterter Eisenüberladung und Zelltod in Verbindung gebracht. Gleichzeitig könnte das verringerte Ppara, ein Regulator des Lipidstoffwechsels und des Energiehaushalts, Netzhautzellen anfälliger für Schäden machen. Durch das Anvisieren dieser gemeinsamen Stresswege könnte es möglich sein, die Netzhautdegeneration über viele genetische Formen der Retinitis pigmentosa hinweg zu verlangsamen.
Medikamente, die das Sehen schützen könnten
Mithilfe einer Datenbank für Wirkstoff–Gen-Interaktionen suchten die Autoren nach Verbindungen, die Egr1 oder Cd44 beeinflussen könnten. Mehrere existierende Moleküle tauchten auf, darunter der natürliche Stoff Genipin, der in Modellen von Parkinson, Nervendegeneration und diabetischer Retinopathie schützende Effekte gezeigt hat, indem er oxidativen Stress und Entzündung dämpft. Obwohl keines dieser Kandidaten bisher in genau diesem Mausmodell der Retinitis pigmentosa getestet wurde, bieten sie vielversprechende Ansatzpunkte für künftige Labor- und Tierstudien, die darauf abzielen, Photorezeptoren vor Ferroptose zu schützen.
Kernaussage für Nichtfachleute
Diese Arbeit zeigt, dass eisengetriebener, oxidativer Zelltod eng mit den Genaktivitätsänderungen in einem klassischen Modell erblicher Erblindung verknüpft ist. Indem acht Schlüsselgene herausgearbeitet wurden — besonders das stressantwortende Egr1 in Photorezeptoren und Cd44 in Müller-Zellen — zeichnet die Studie neues Terrain für potenzielle Therapien, die nicht auf die Reparatur eines einzelnen mutierten Gens angewiesen sind. Bestätigen künftige Experimente, dass das Dämpfen der Ferroptose über diese Ziele Netzhautzellen am Leben erhalten kann, eröffnet das die Möglichkeit von Behandlungen, die einer breiten Palette von Patienten mit fortschreitendem Sehverlust zugutekommen könnten.
Zitation: Qiu, X., Fu, XW., Lei, XL. et al. Identification and validation of a novel ferroptosis-related gene signature associated with inherited retinal degeneration in Rd10 mice. Sci Rep 16, 6992 (2026). https://doi.org/10.1038/s41598-026-38193-4
Schlüsselwörter: retinitis pigmentosa, Ferroptose, Photorezeptoren, Netzhautdegeneration, Egr1 Cd44