Clear Sky Science · de
Integrierte Metabolomik und 16S-rRNA-Sequenzierung enthüllen den Wirkmechanismus der Gesamtflavone von Abelmoschus manihot (L.) Medic gegen Leberfibrose
Blütenkraft für eine vernarbte Leber
Leberverhärtung oder Fibrose ist eine stille Gefahr, die langsam zu Zirrhose und Leberversagen führen kann. In der modernen Medizin fehlen noch sichere, breit wirksame Arzneien, die diesen Prozess stoppen oder umkehren. Diese Studie untersucht, ob natürliche Verbindungen aus den leuchtend gelben Blüten von Abelmoschus manihot – einer in der traditionellen chinesischen Medizin bereits bei Nierenerkrankungen eingesetzten Pflanze – die Leber vor langfristigen toxischen Schäden schützen können und wie sie dies möglicherweise tun, indem sie sowohl die Körperchemie als auch die Darmmikroben beeinflussen.
Ein weltweit wachsendes Leberproblem
Hunderte Millionen Menschen leben weltweit mit chronischen Lebererkrankungen, verursacht durch Viren, Alkohol, Fettablagerungen oder Toxine. Wiederholte Leberverletzungen führen dazu, dass das Organ Narbengewebe bildet – ähnlich einer Wunde, die nie vollständig heilt. Mit der Zeit kann diese Fibrose die Leber versteifen, den Blutfluss behindern und sich zur Zirrhose entwickeln, einer der führenden Ursachen für leberbedingte Todesfälle. Da viele verschiedene Auslöser gleichzeitig Schaden anrichten können, interessieren sich Forscher besonders für pflanzliche Mischungen, die mehrere Ziele gleichzeitig ansprechen, statt einzelner Wirkstoffe, die nur einen Signalweg treffen.
Erprobung eines traditionellen Mittels an Mäusen
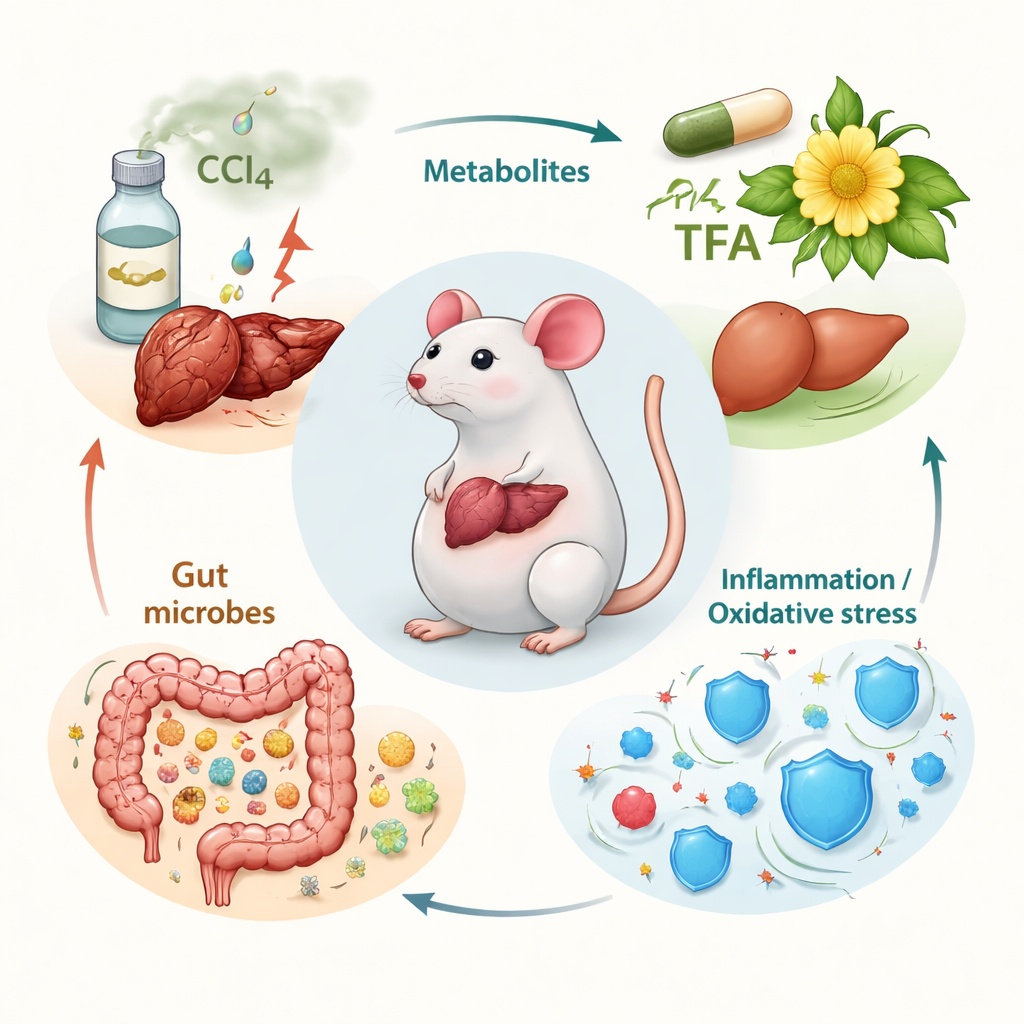
Das Team konzentrierte sich auf die „Gesamtflavone“ von Abelmoschus manihot (TFA) – eine konzentrierte Mischung aus sieben verwandten Pflanzenverbindungen, die zuvor entzündungshemmende und antioxidative Wirkungen gezeigt hatten. Sie verwendeten ein etabliertes Mausmodell, bei dem wiederholte Exposition gegenüber dem Industriechemikal CCl4 (Tetrachlorkohlenstoff) chronische Leberschädigung und Narbenbildung ähnlich der menschlichen Fibrose verursacht. Männliche Mäuse wurden in Gruppen eingeteilt: gesunde Kontrollen, CCl4‑geschädigte „Modell“-Mäuse, eine Standardmedikamenten‑Gruppe und drei TFA‑Dosisgruppen. Nach Wochen der CCl4‑Exposition behandelten die Forscher die Tiere oral mit TFA und untersuchten anschließend Blut, Lebergewebe und Darminhalt.
Bessere Blutwerte und gesünderes Lebergewebe
TFA zeigte klare Schutzwirkungen. Die Blutwerte der Leberenzyme ALT und AST – klinische Indikatoren für Leberschädigung – stiegen in CCl4‑exponierten Mäusen stark an, sanken jedoch in den TFA‑behandelten Tieren um etwa die Hälfte. Die mikroskopische Untersuchung bestätigte dies: Unbehandelte fibrotische Lebern zeigten verzerrte Architektur, abgestorbene Zellen, ausgeprägte Kollagenablagerungen und entzündliche Zellansammlungen. Bei TFA‑behandelten Lebern gab es weniger Narben‑„Pseudolobuli“, geringere Kollagenfärbung und reduzierte Zeichen von Zelluntergang. Marker des oxidativen Stresses verbesserten sich ebenfalls: Antioxidative Abwehrsysteme (SOD und GSH‑Px) stiegen, während schädliche Stoffwechselprodukte (MDA) sanken. Wichtige Entzündungsbotenstoffe, darunter TNF‑α, IL‑6 und TGF‑β1, waren ebenfalls reduziert, ebenso wie chemische Fibrosemarker wie Hydroxyprolin, Kollagen IV und Hyaluronsäure.
Wiederherstellung der Körperchemie und der Darmmikroben
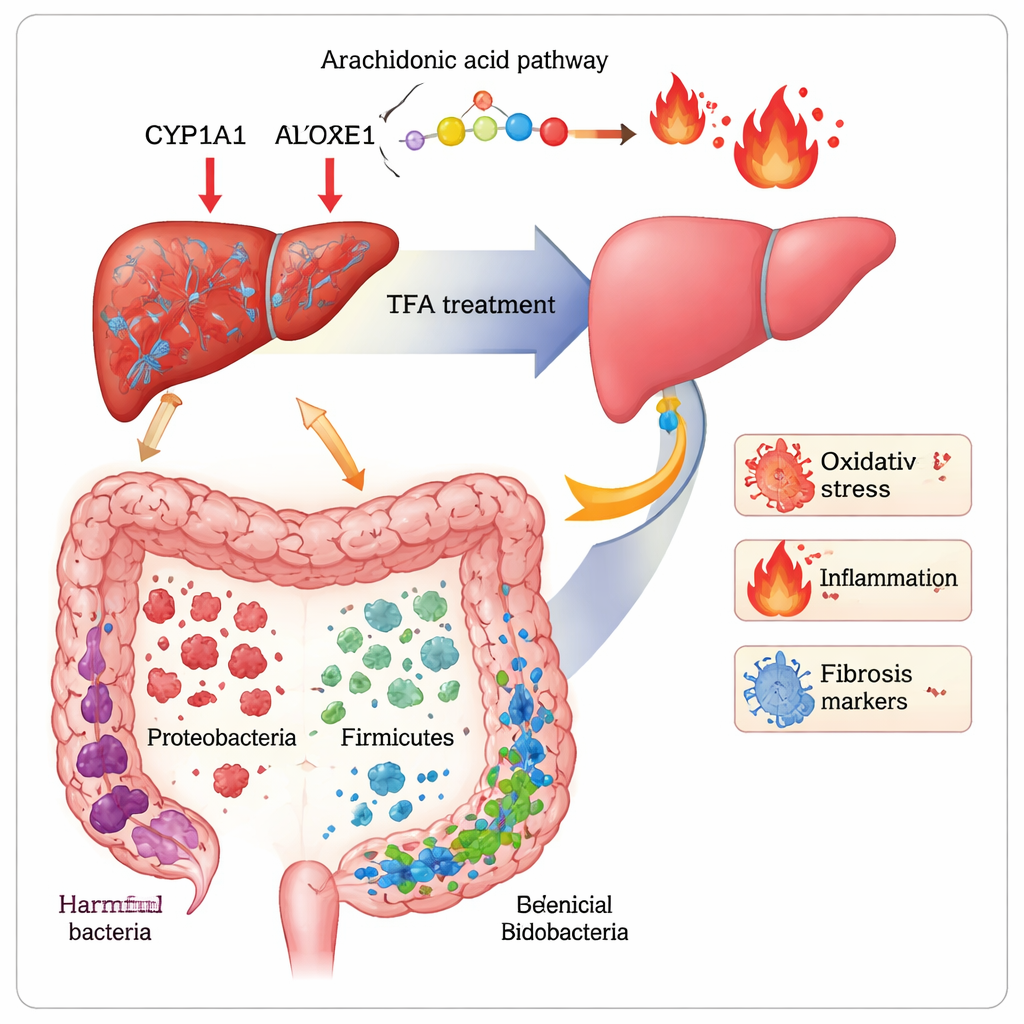
Um aufzudecken, wie TFA diese Vorteile vermittelt, kombinierten die Forscher zwei leistungsfähige Werkzeuge: Metabolomik, die Hunderte kleiner Moleküle im Blut profilieren kann, und 16S‑rRNA‑Sequenzierung, die die Bakterientypen im Darm kartiert. Bei fibrotischen Mäusen waren Dutzende von Metaboliten, die an Fettstoffwechsel und Aminosäureabbau beteiligt sind, gestört. TFA stellte teilweise das Gleichgewicht in Signalwegen wieder her, die mit Zellmembranen (Glycerophospholipide), der stimmungsrelevanten Aminosäure Tryptophan und einer Fettsäure namens Arachidonsäure verbunden sind, die Entzündungssignale nährt. Die Spiegel zweier Arachidonsäure‑Produkte, 20‑HETE und 16(R)‑HETE – beide mit oxidativem Stress und Fibrose in Verbindung gebracht – wurden wieder in Richtung Normalwerte verschoben. In der Leber senkte TFA die Menge dreier Enzyme (CYP1A1, CYP2E1, ALOX15), die an der Bildung dieser schädlichen Moleküle beteiligt sind. Gleichzeitig störte CCl4 die Darmmikrobiota, reduzierte nützliche Gruppen wie Firmicutes, Lactobacillus und Bifidobacterium und ließ potenziell schädliche Proteobacteria aufblühen. TFA kehrte einen Großteil dieser Verschiebung um, erhöhte die Diversität und stellte „freundliche“ Bakterien wieder her, die mit besserer Barrierfunktion und geringerer Entzündung assoziiert sind.
Eine Multi‑Ziel‑Strategie auf der Darm‑Leber‑Achse
Indem bakterielle Veränderungen mit Blutchemie und Krankheitsmarkern verknüpft wurden, legt die Studie nahe, dass TFA entlang der „Darm‑Leber‑Achse“ wirkt – der vielbefahrenen Verbindung von Signalen, Nährstoffen und Toxinen vom Darm zur Leber. Schädliche Bakterien und deren Produkte scheinen mit höherer Entzündung und Narbenbildung zu korrelieren, während nützliche Mikroben mit gesünderen Stoffwechselprofilen und weniger Fibrose einhergehen. TFA scheint dieses gesamte System zurück ins Gleichgewicht zu schieben: Es stärkt antioxidative Abwehrmechanismen, dämpft entzündliche Wege, die durch Arachidonsäure angetrieben werden, formt die mikrobielle Gemeinschaft im Darm um und mildert letztlich die Narbenbildung in der Leber.
Was das für zukünftige Behandlungen bedeuten könnte
Für nicht‑Fachleute ist die Kernbotschaft, dass ein seit Langem in der Tradition verwendeter Blütenextrakt in einem modernen, strengen Test chronischer Lebernarbenbildung vielversprechende Ergebnisse zeigte. Bei Mäusen schützte TFA nicht nur Leberzellen – es reduzierte gleichzeitig toxische Chemikalien und schädliche Darmmikroben. Obwohl diese Ergebnisse noch keinen Nutzen beim Menschen beweisen und nur an männlichen Tieren unter einer Form der Leberschädigung gewonnen wurden, heben sie eine potenzielle Multi‑Ziel‑Therapie hervor, die mit den eigenen Netzwerken des Körpers arbeitet statt gegen ein einzelnes Molekül. Mit weiteren Untersuchungen könnten solche pflanzenbasierten Flavone eines Tages Teil eines breiteren Werkzeugsatzes werden, um Leberfibrose zu verlangsamen oder sogar umzukehren.
Zitation: Li, D., Ge, H., Zhang, Y. et al. Integrated metabolomics and 16S rRNA sequencing reveal the mechanism of total flavones of Abelmoschus manihot (L.) Medic against liver fibrosis. Sci Rep 16, 7342 (2026). https://doi.org/10.1038/s41598-026-38192-5
Schlüsselwörter: Leberfibrose, Darmmikrobiota, Metabolomik, Flavonoide, Traditionelle chinesische Medizin