Clear Sky Science · de
Biokompatible 3D-hierarchische, blumenförmige eisendotierte Silbernanostrukturen als Plattform für in vitro- und in vivo-Wirkstofffreisetzung
Warum winzige Metallblumen für die Krebstherapie wichtig sind
Chemotherapeutika können starke Verbündete gegen Krebs sein, verhalten sich aber oft wie Flächenbombardements: Sie verteilen sich im ganzen Körper und schädigen gesunde Gewebe ebenso wie Tumore. Diese Studie untersucht einen ganz anderen Ansatz: winzige, blumenförmige Partikel aus Silber und Eisen zu bauen, die das bewährte Krebsmedikament Methotrexat tragen und es gezielter dort freisetzen können, wo es gebraucht wird. Durch Feinabstimmung von Form, Oberflächenchemie und Säureempfindlichkeit wollen die Forschenden die Behandlung sowohl wirksamer als auch verträglicher für den Rest des Körpers machen.
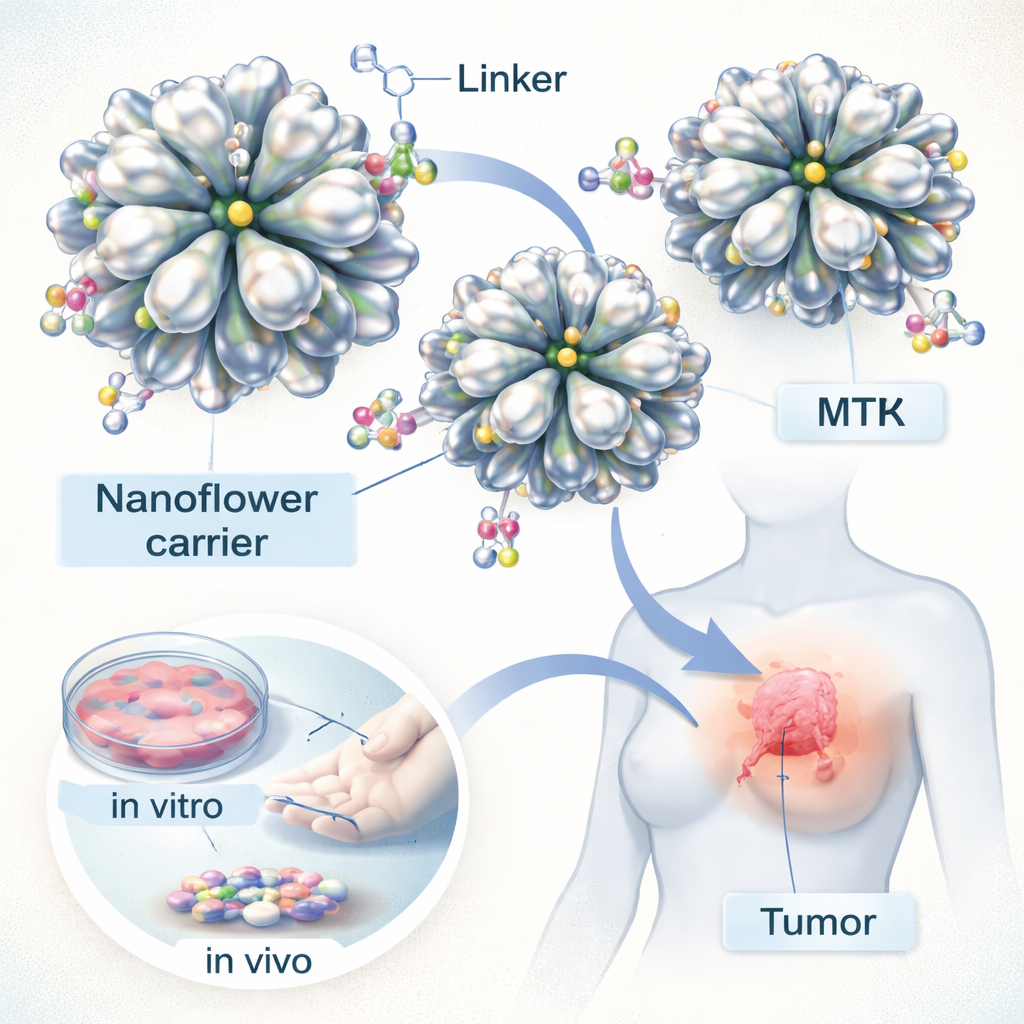
Winzige Blumen aus Metallen
Das Team entwarf dreidimensionale „Nanoblumen“ aus Silber, das leicht mit Eisen legiert ist. Unter dem Mikroskop ähneln diese Partikel tatsächlich Blumen mit vielen dünnen, überlappenden Blütenblättern. Diese komplexe Form verleiht ihnen eine sehr große Oberfläche, ideal zum Aufnehmen von Wirkstoffmolekülen. Die Forschenden stellten die Nanoblumen mittels einer einfachen wässrigen chemischen Reaktion her und passten Zutaten wie Bernsteinsäure (malonsäure) und Eisensalze so an, dass die Metallatome in verzweigten, blattähnlichen Strukturen statt zu kompakten Kugeln heranwachsen. Untersuchungen mit bildgebenden und strukturellen Methoden bestätigten, dass die Partikel die gewünschte raue, geschichtete Oberfläche besitzen und dass Eisen gleichmäßig im Silber verteilt ist.
Metallblumen als Wirkstoffträger
Um diese Metallblumen in Wirkstoffshuttles zu verwandeln, beschichteten die Wissenschaftler zunächst ihre Oberfläche mit einem kleinen organischen Molekül, das wie ein zweiköpfiger Haken wirkt. Ein Ende bindet natürlich an Silber, das andere Ende kann Methotrexat einhaken. Mittels gängiger Kupplungschemie stellten sie stabile Verbindungen zwischen dem Wirkstoff und der Nanoblütenoberfläche her. Diese Strategie erzielte eine hohe Beladungskapazität—der Großteil des zugeführten Methotrexats ließ sich an den Träger binden. Entscheidend ist, dass die Bindung zwischen Wirkstoff und Träger säureempfindlich ist. Unter den leicht sauren Bedingungen, wie sie häufig in Tumoren und zellulären Kompartimenten vorkommen, löst sich die Bindung schneller, während sie im nahezu neutralen pH-Wert gesunden Bluts stabiler bleibt.
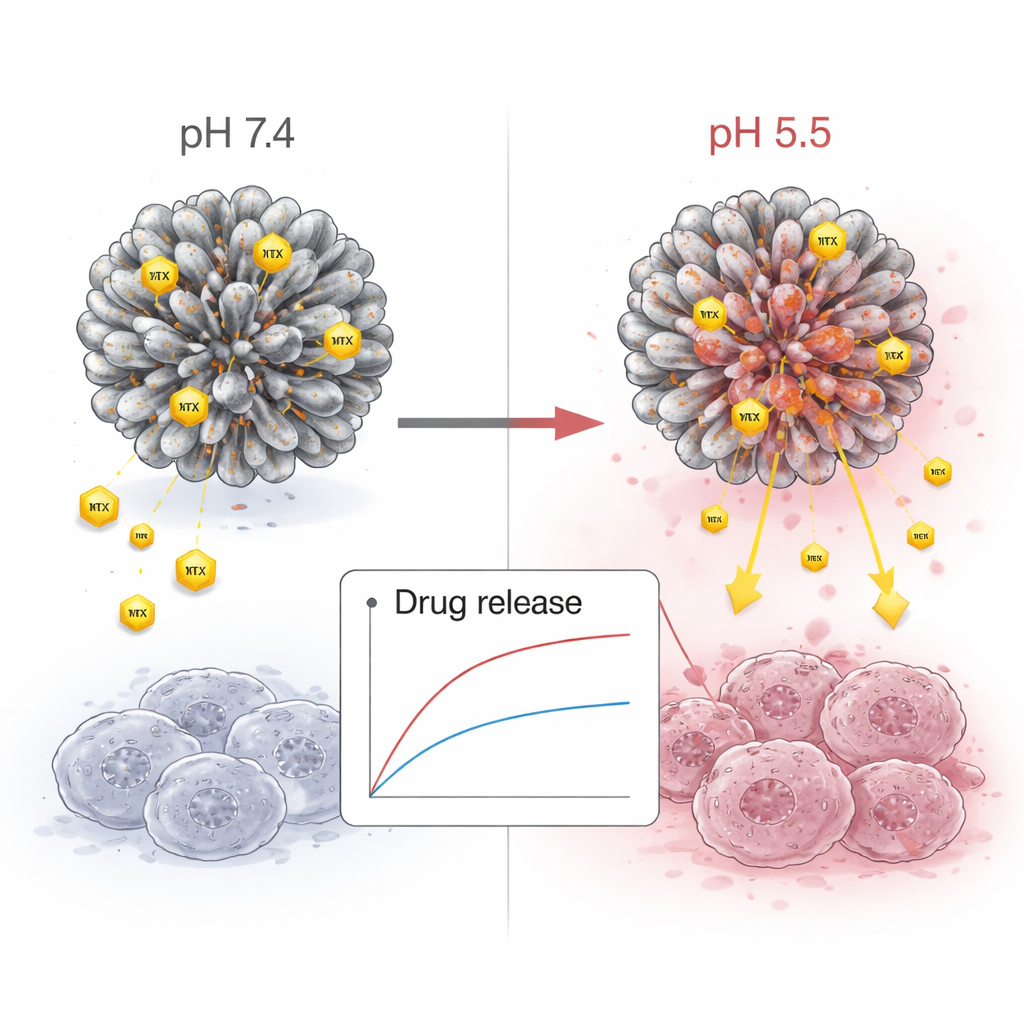
Gezielte Freisetzung in sauren Tumoren
Das Team testete anschließend, wie viel Wirkstoff über die Zeit bei verschiedenen Säuregraden freigesetzt wird. Im normalen Blut-pH geben die Nanoblumen Methotrexat nur langsam frei, was dazu beitragen könnte, Schäden an gesundem Gewebe zu begrenzen. In saurerem Milieu, ähnlich dem Inneren von Brustkrebszellen, beschleunigte sich die Freisetzung deutlich, und über ein bis zwei Tage wurde deutlich mehr Wirkstoff freigesetzt. Das bedeutet, dass dasselbe Partikel im Kreislauf „ruhig“ bleiben, aber im raueren chemischen Umfeld des Tumors „aktiv“ wird. Dieses pH-reaktive Verhalten ist eines der Hauptziele moderner „intelligenter“ Wirkstofftransportsysteme.
Wirkungen auf Zellen, Blut und Tumore
Im Zellkulturversuch erwiesen sich die mit Methotrexat beladenen Nanoblumen als schonend gegenüber normalen Fibroblasten, während sie für Brustkrebszellen schädlicher waren—ein Hinweis auf eine gewisse Selektivität. Krebszellen, die den Nanoblüten ausgesetzt wurden, zeigten Anzeichen programmierter Zellsterblichkeit und wurden überwiegend in der DNA-Replikationsphase ihres Zellzyklus aufgehalten, was mit der bekannten Wirkungsweise von Methotrexat übereinstimmt. Fluoreszenzbildgebung zeigte, dass die Partikel in Zellen eindringen und sich dem genetischen Material nähern können. Die Nanoblumen schnitten auch in Bluttests gut ab: Sie verursachten bei den meisten Konzentrationen nur geringe Schädigung roter Blutkörperchen, und die wirkstoffbeladenen Varianten waren besonders sicher. In Mausmodellen des Brustkrebses zeigten Mikro-CT-Aufnahmen und Gewebsuntersuchungen, dass die Partikel dazu neigen, sich in Tumoren anzureichern, wo sie das Tumorvolumen über einen Zeitraum von zwei Wochen verkleinerten, bei gleichzeitig begrenzter Anreicherung in anderen Organen.
Was das für künftige Therapien bedeuten könnte
Insgesamt legt die Studie nahe, dass diese eisendotierten Silbernanoblumen eine vielversprechende Plattform für die gezielte und schonendere Verabreichung von Methotrexat darstellen können. Durch die Kombination aus hoher Wirkstoffbeladung, säuregetriebener Freisetzung und vertretbarer Sicherheit in Blut und Geweben sprechen sie mehrere langjährige Probleme der Chemotherapie an: mangelnde Selektivität, starke Nebenwirkungen und rasches Auswaschen des Wirkstoffs. Zwar sind noch weitere Untersuchungen nötig, um ihr Langzeitverhalten im Körper vollständig zu verstehen und sie für den Einsatz beim Menschen anzupassen, doch deuten diese winzigen Metallblumen auf eine Zukunft hin, in der Krebsmedikamente direkt zu Tumoren transportiert und kontrollierter freigesetzt werden—möglicherweise machen sie etablierte Wirkstoffe sowohl sicherer als auch wirksamer.
Zitation: Almosawy, W., Landarani-Isfahani, A., Moghadam, M. et al. Biocompatible 3D hierarchical flower-like iron-doped silver nanostructures as a platform for in vitro and in vivo drug delivery. Sci Rep 16, 7044 (2026). https://doi.org/10.1038/s41598-026-38175-6
Schlüsselwörter: Nanomedizin, Wirkstofffreisetzung, Methotrexat, Brustkrebs, Silbernanopartikel