Clear Sky Science · de
Das hypoxische Tight‑Skin-Mausmodell der Gruppe‑3‑Pulmonalhypertension
Warum diese Forschung wichtig ist
Pulmonale Hypertonie ist ein schwerwiegender, oft tödlicher Anstieg des Blutdrucks in der Lunge. Eine der häufigsten Formen, die als Gruppe‑3‑Pulmonalhypertension bezeichnet wird, entwickelt sich bei Menschen mit chronischen Lungenerkrankungen wie Emphysem oder Lungenfibrose oder bei Personen mit langfristiger Sauerstoffunterversorgung. Dennoch fehlen Ärzten gezielte Medikamente für diese Erkrankung, unter anderem weil Wissenschaftlern bisher ein Tiermodell fehlte, das das Geschehen in menschlichen Lungen realistisch nachbildet. Diese Studie stellt ein neues Mausmodell vor, das der Gruppe‑3‑Erkrankung sehr ähnlich ist, und deckt eine schädliche Signalkette auf, die in Zukunft therapeutisch angegriffen werden könnte.
Eine Maus, die geschädigte Lungen nachahmt
Die Forscher konzentrierten sich auf einen Mäusestamm, der als „tight‑skin“ (Tsk) bekannt ist. Diese Tiere tragen eine Mutation in einem Strukturprotein namens Fibrillin‑1. Aufgrund dieses Defekts entwickeln sie von Natur aus emphysemähnliche Veränderungen und Vernarbungen in ihren Lungen, ähnlich wie Menschen mit schwerer chronischer Lungenerkrankung. Das Team verglich diese Mäuse mit normalen Wurfgeschwistern, wobei die Tiere entweder normaler Luft oder über vier Wochen niedrigen Sauerstoffbedingungen ausgesetzt wurden, um den chronischen Sauerstoffmangel zu simulieren, den viele Patientinnen und Patienten erleben. 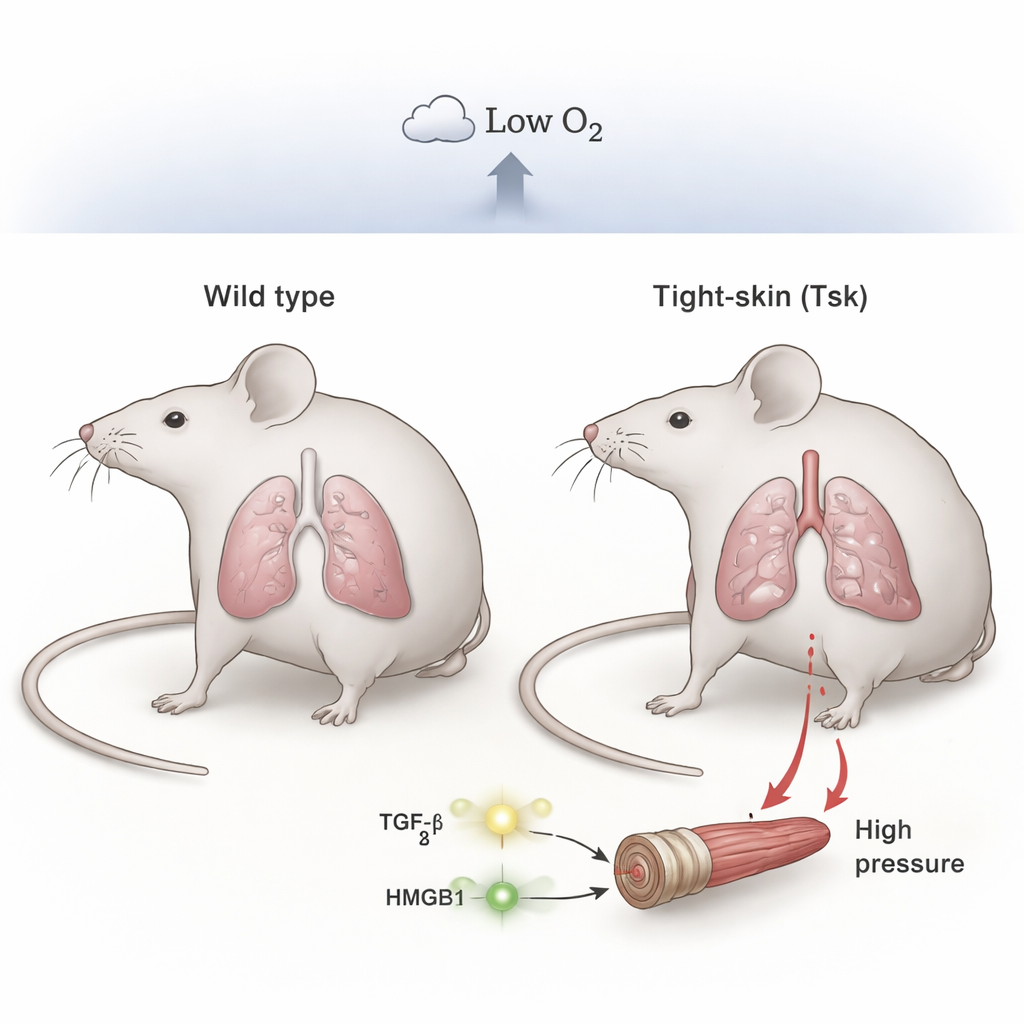
Niedriger Sauerstoff verwandelt eine verletzliche Lunge in Hochdrucklungen
Wenn sowohl normale als auch tight‑skin‑Mäuse an Raumluft gehalten wurden, waren ihre Lungenblutdrücke ähnlich und im normalen Bereich. Unter chronischer Hypoxie waren die Unterschiede jedoch deutlich. Normale Mäuse entwickelten nur moderate Druckanstiege, während tight‑skin‑Mäuse eine schwere pulmonale Hypertonie entwickelten, mit deutlich erhöhten Drücken auf der rechten Herzseite und offensichtlicher Verdickung der kleinen Lungenarterien. Die Mikroskopie zeigte vergrößerte Lufträume (Emphysem) und ausgeprägte Muskelbildung in winzigen Gefäßen der tight‑skin‑Tiere, was die strukturellen Schäden bei Patientinnen und Patienten mit Gruppe‑3‑Erkrankung eng widerspiegelt. Dies deutet darauf hin, dass vorbestehende Lungenschädigung plus Hypoxie gemeinsam das System in einen weitaus gefährlicheren Zustand treiben als Hypoxie allein.
Ein Gefahrensignal im Blut
Das Team fragte dann, warum tight‑skin‑Mäuse so stark auf niedrigen Sauerstoff reagieren. Sie konzentrierten sich auf ein Molekül namens HMGB1, ein „Gefahrensignal“-Protein, das von gestressten oder geschädigten Zellen freigesetzt wird. Tight‑skin‑Mäuse hatten bereits im Baseline‑Zustand höhere HMGB1‑Spiegel im Blut, und diese Werte stiegen unter Hypoxie weiter an. Die Verabreichung eines kleinen Peptidarzneimittels, P5779, das die Interaktion von HMGB1 mit einem seiner wichtigen Rezeptoren (TLR4) blockiert, verhinderte weitgehend die Entwicklung der schweren pulmonalen Hypertonie bei tight‑skin‑Mäusen. Die behandelten Tiere zeigten niedrigere Lungenwerte, weniger Verdickung ihrer Lungengefäße und eine geringere Vergrößerung der rechten Herzhälfte. Diese schützenden Effekte waren bei tight‑skin‑Mäusen deutlich ausgeprägter als bei normalen Mäusen und machen HMGB1 in diesem Modell zu einem zentralen Verstärker der Erkrankung.
Wie ein Wachstumssignal das Gefahrensignal nährt
Ein weiterer Akteur in dieser Geschichte ist TGF‑β, ein Wachstumsfaktor, der seit langem mit Vernarbung und Umbau in erkrankten Lungen in Verbindung gebracht wird. Die Forscher fanden, dass tight‑skin‑Mäuse eine höhere basale TGF‑β‑Aktivität in ihren Lungen aufwiesen, erkennbar an einer erhöhten Aktivierung seines nachgeschalteten Botenstoffs SMAD‑3 um Blutgefäße. In Experimenten mit humanen adventitiellen Fibroblasten aus Lungenarterien — Zellen, die die äußere Schicht von Blutgefäßen auskleiden — erhöhte die Zugabe von TGF‑β die Produktion von HMGB1. Im Gegenzug bewirkte HMGB1 sowohl bei diesen Fibroblasten als auch bei benachbarten glatten Muskelzellen eine Proliferation. Wichtig ist, dass dieser Wachstumseffekt vom TLR4‑Rezeptor abhängt und durch P5779 blockiert wurde, nicht jedoch durch Blockade eines anderen HMGB1‑Rezeptors namens RAGE. Zusammengenommen skizzieren diese Befunde eine Schleife, in der mutiertes Fibrillin‑1 die TGF‑β‑Aktivierung fördert, TGF‑β die HMGB1‑Spiegel erhöht und HMGB1 das Überwachsen von Gefäßwandzellen antreibt, das Lungenarterien verengt. 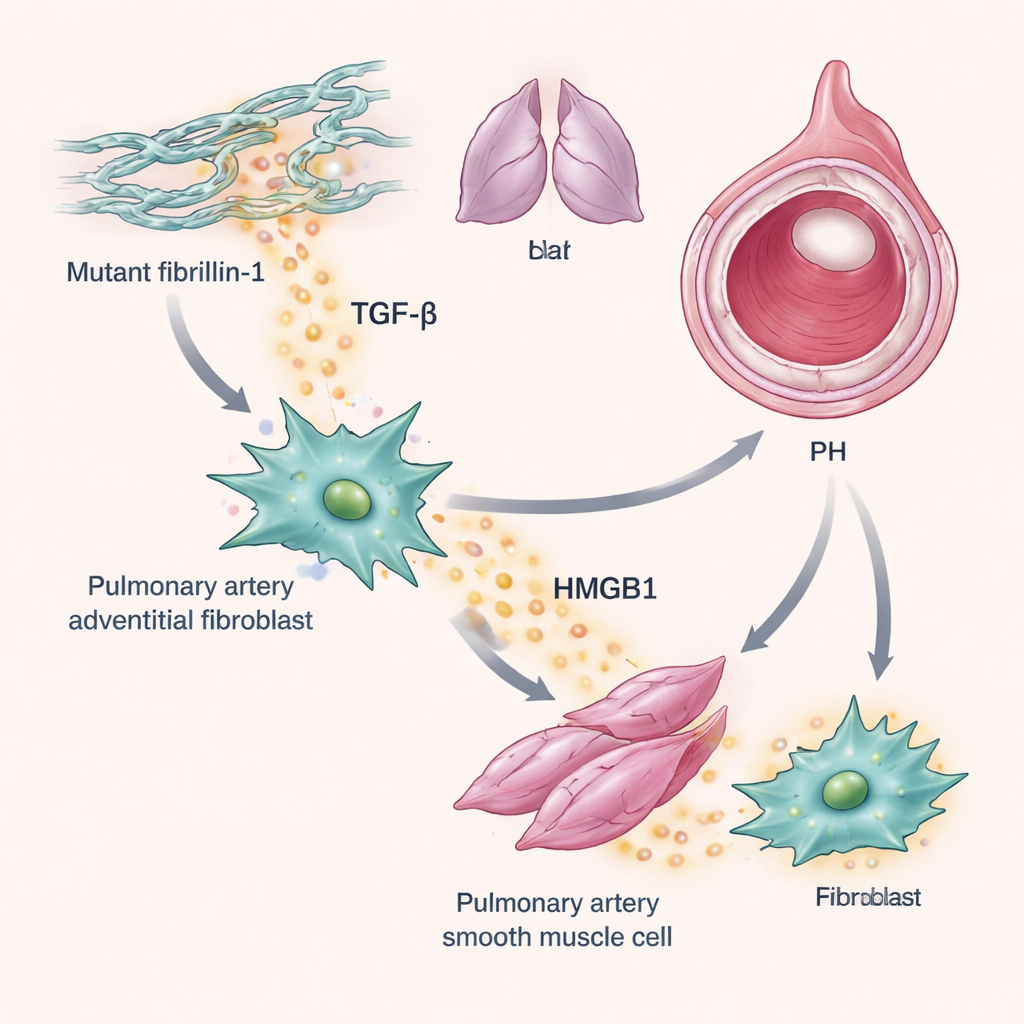
Folgen für Patientinnen und Patienten
Durch die Kombination einer emphysemähnlichen Lungenstruktur mit chronischer Hypoxie reproduziert das tight‑skin‑Mausmodell viele Schlüsselmerkmale der Gruppe‑3‑pulmonalen Hypertonie, die einfachere Modelle mit nur Hypoxie nicht abbilden. Die Arbeit hebt einen TGF‑β–HMGB1–TLR4‑Weg hervor, der verletzte, sauerstoffarme Lungen in Hochdrucklungen verwandelt. Für Menschen mit chronischen Lungenerkrankungen deutet diese Forschung auf neue Therapieansätze hin: Medikamente, die das TGF‑β‑Signaling dämpfen, oder solche, die HMGB1–TLR4‑Interaktionen wie P5779 blockieren, könnten eines Tages helfen, den Anstieg des Lungenblutdrucks zu verhindern oder zu verlangsamen. Das Modell selbst bietet außerdem eine leistungsfähige neue Plattform, um solche Behandlungen zu testen, bevor sie in die Klinik gelangen.
Zitation: Chi, L., Foley, A.E., Goodarzi, G. et al. The hypoxic tight-skin mouse model of Group 3 pulmonary hypertension. Sci Rep 16, 6968 (2026). https://doi.org/10.1038/s41598-026-38174-7
Schlüsselwörter: pulmonale Hypertonie, chronische Lungenerkrankung, Hypoxie, HMGB1, TGF-beta