Clear Sky Science · de
Die potenzielle Wirkung von Albuminersatz auf Immunmodulation und Sphingosin‑1‑phosphat‑Dynamik
Warum das für Intensivpatienten wichtig ist
Patienten auf Intensivstationen haben oft sehr niedrige Werte eines Blutproteins namens Albumin. Ärztinnen und Ärzte verabreichen gelegentlich Albumin‑Infusionen in der Hoffnung, den Blutdruck zu stabilisieren und das Überleben zu verbessern, doch größere Studien haben keinen eindeutigen Vorteil gezeigt. Diese Studie stellt eine andere Frage: Statt nur das Flüssigkeitsgleichgewicht zu betrachten, könnte Albumin das Immunsystem beeinflussen, indem es ein kleines fettähnliches Botenmolekül im Blut transportiert — und könnte das erklären, warum manche Patienten scheinbar mehr Nutzen haben als andere?
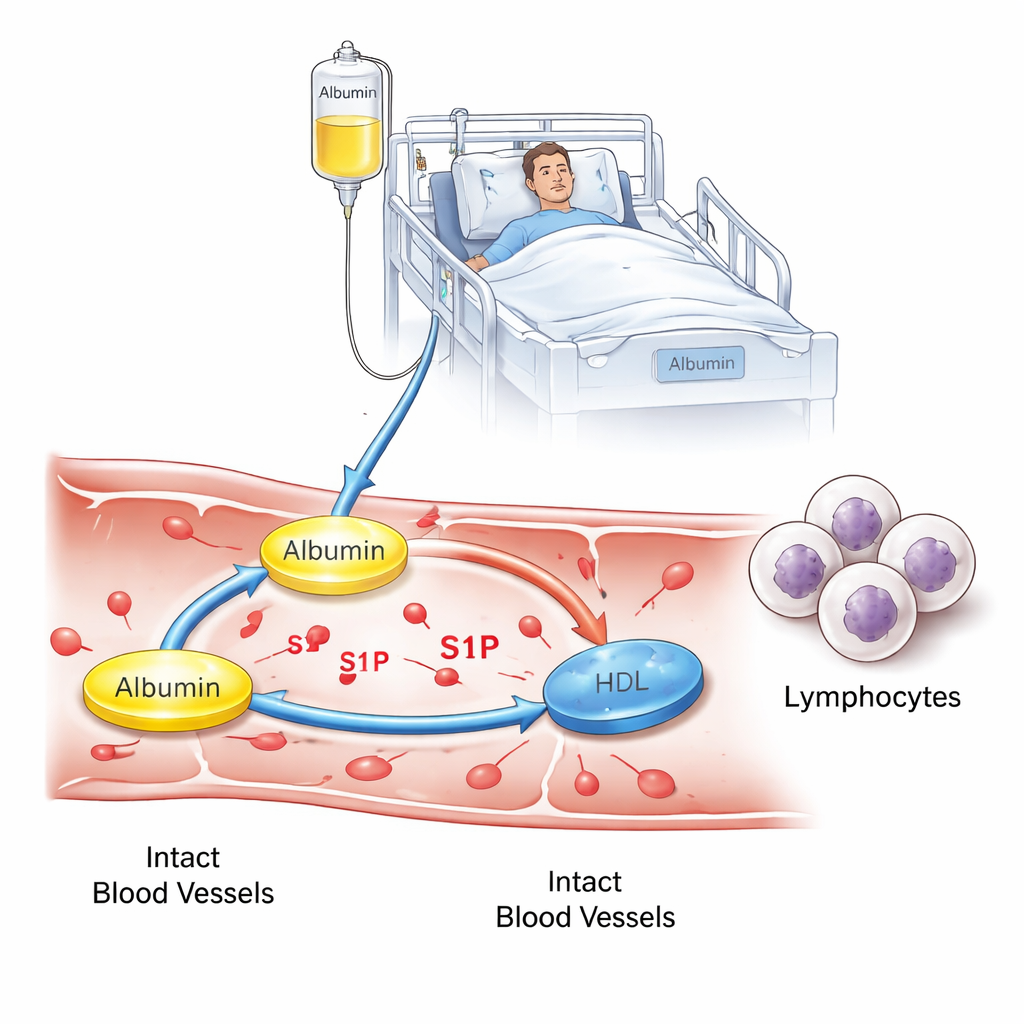
Ein genauerer Blick auf Albumin und einen winzigen Botenstoff
Albumin erfüllt mehr Aufgaben, als nur Wasser in unseren Blutgefäßen zu halten. Es transportiert auch zahlreiche kleine Moleküle, darunter Sphingosin‑1‑phosphat (S1P), das steuert, wie sich weiße Blutkörperchen im Körper bewegen und wie „leck“ Blutgefäße während schwerer Erkrankungen werden. Bei gesunden Menschen zirkuliert S1P hauptsächlich an zwei Trägern: Albumin und High‑Density‑Lipoprotein (HDL, oft als „gutes Cholesterin“ bezeichnet). Wenn Menschen kritisch erkranken — insbesondere bei Sepsis — können sowohl Albumin‑ als auch HDL‑Werte sinken, und frühere Arbeiten zeigten, dass auch S1P‑Werte abfallen, was mit schlechteren Ergebnissen verbunden ist. Die Autorinnen und Autoren wollten prüfen, ob die Gabe von humanem Albumin an Intensivpatienten mit niedrigem Albumin das Verteilungsverhältnis von S1P zwischen Albumin und HDL verändern könnte und ob sich diese Verschiebung in Veränderungen der Immunzellen oder der Gefäßstabilität niederschlägt.
Wie die Studie am Krankenbett durchgeführt wurde
Das Team begleitete 47 Erwachsene auf einer einzigen Intensivstation über rund ein Jahr. Alle hatten niedrige Albuminwerte, doch die behandelnden Ärzte — nicht die Forschenden — entschieden, wer Albumininfusionen erhielt. Daraus ergaben sich drei Gruppen: eine kleine Kontrollgruppe mit normalem Albumin, eine größere Gruppe mit niedrigem Albumin, die kein Albumin erhielt, und eine Behandlungsgruppe mit niedrigem Albumin, die über drei Tage 180 Gramm humanes Albumin bekam. Es wurden Blutproben für Standardlaborwerte, detaillierte Messungen von S1P und Zählungen verschiedener weißer Blutkörperchen entnommen. Die Forscher nutzten außerdem spezialisierte Methoden, um zu bestimmen, ob S1P in jeder Probe hauptsächlich an Albumin oder an HDL gebunden war, und führten Laborassays durch, um zu sehen, wie das Plasma der Patienten die Bewegung von weißen Blutkörperchen und die Dichtheit von Gefäßzellschichten beeinflusste.
Was sich im Blut veränderte — und was nicht
Wie erwartet erhöhten Albumininfusionen die Albuminspiegel im Blut der behandelten Gruppe deutlich, was bestätigt, dass die Behandlung im grundlegenden Sinn wirkte. Überraschenderweise stiegen die Gesamts1P‑Werte im Blut durch die Albumintherapie nicht an und blieben niedriger als bei Intensivpatienten, deren Albumin von Anfang an normal war. Die wichtige Veränderung betraf die Trägerschaft von S1P: Nach der Behandlung war mehr S1P an Albumin gebunden und weniger an HDL, was eine messbare Umverteilung zwischen den Trägern zeigte, ohne die Gesamtmenge zu verändern. Gleichzeitig sanken die Werte von zwei zentralen Typen zirkulierender Immunzellen — CD4‑T‑Zellen und B‑Zellen — über die drei Behandlungstage. Dieses Muster passt zu der Idee, dass Veränderungen im Umgang mit S1P die Rekirkulation von Immunzellen beeinflussen könnten, obwohl das Studiendesign keinen kausalen Nachweis erlaubt.
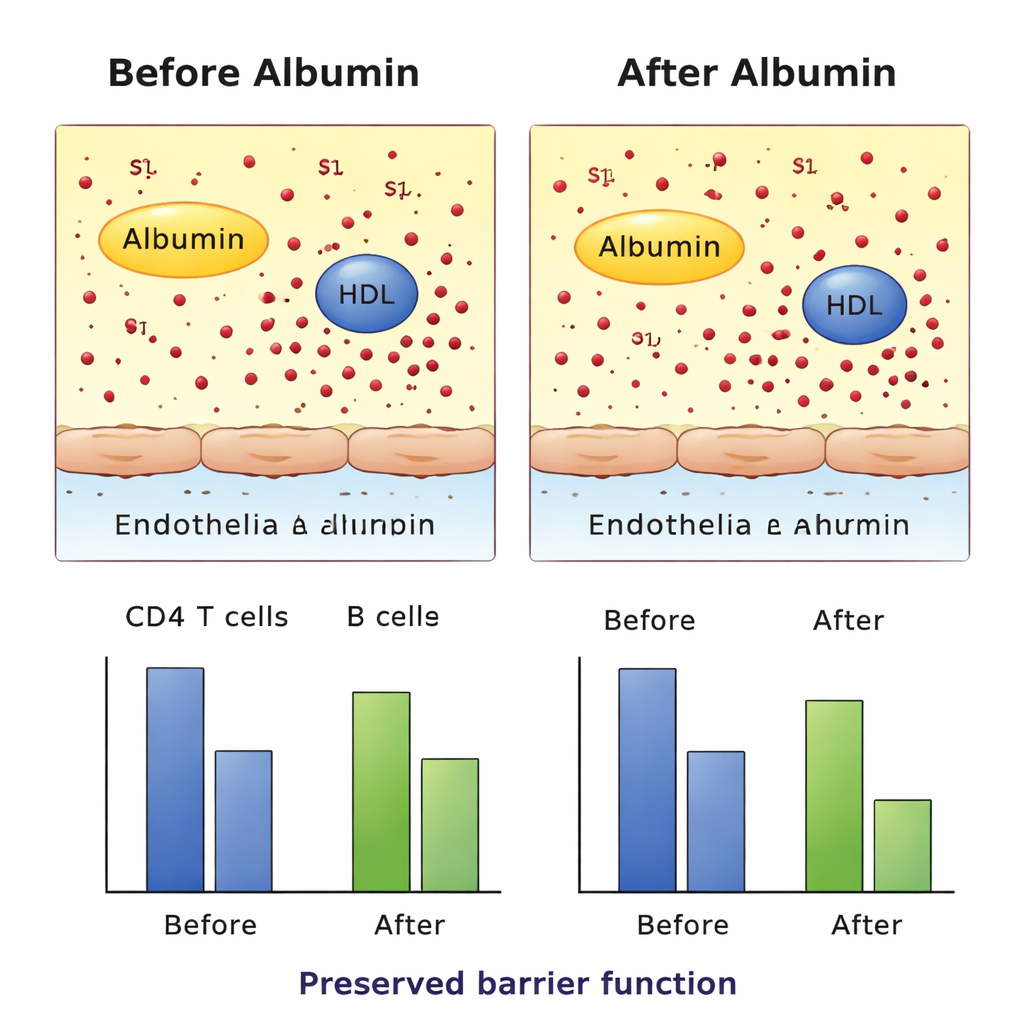
Gefäßschutz und Zellbewegung im Labor getestet
Um herauszufinden, ob dieser Trägerwechsel schädliche Nebenwirkungen hat, prüften die Forschenden Patientenproben in mehreren kontrollierten Laborsystemen. Sie setzten kultivierte Gefäßzellen dem Plasma der verschiedenen Patientengruppen aus und überwachten, wie gut die Zellschicht elektrischen Strom widerstand — ein Maß dafür, wie dicht die Barriere blieb. Außerdem verwendeten sie ein Migrationsassay, bei dem fluoreszierende Immunzellen durch eine Membran in Richtung Patientenplasma wanderten, um das S1P‑gesteuerte „Homing“ zu simulieren. In diesen ex vivo‑Experimenten schwächte das Plasma der albuminbehandelten Patienten die Gefäßbarriere nicht und verringerte die S1P‑getriebene Bewegung von Immunzellen nicht signifikant im Vergleich zu Kontrollen. Zusätzliche Tests auf Rezeptorebene zeigten, dass S1P, das entweder auf HDL oder auf Albumin getragen wird, seine Zielrezeptoren zumindest unter den untersuchten Bedingungen weiterhin aktivieren kann.
Was das für künftige Therapieentscheidungen bedeutet
Für Nicht‑Fachleute lautet die Kernbotschaft: Albumininfusionen bei sehr kranken Patienten scheinen die Gesamtmenge dieses wichtigen Botenmoleküls S1P nicht wiederherzustellen, verschieben es aber im Blut vom HDL hin zum Albumin. Diese Verschiebung geht mit subtilen Veränderungen zirkulierender Immunzellen einher, ohne in Labortests offensichtliche Schädigung der Gefäßstabilität zu zeigen. Die Ergebnisse stützen die Vorstellung, dass Albumin immunmodulierende Rollen hat, die über das bloße Zurückhalten von Flüssigkeit hinausgehen, und dass sein Nutzen — falls vorhanden — auf bestimmte Patientengruppen beschränkt sein könnte, etwa solche mit sehr niedrigem HDL oder ausgeprägter Entzündung. Größere, zielgerichtete Studien sind erforderlich, um zu klären, ob sorgfältig ausgewählte Patienten von dieser nuancierteren Rolle der Albumintherapie klinisch profitieren können.
Zitation: Winkler, M.S., Enzmann, F., Schilder, M. et al. The potential effect of albumin replacement on immune modulation and sphingosine 1-phosphate dynamics. Sci Rep 16, 5412 (2026). https://doi.org/10.1038/s41598-026-38157-8
Schlüsselwörter: Albumintherapie, kritisch Kranke, Sphingosin‑1‑phosphat, Sepsisimmunologie, vaskuläre Barriere