Clear Sky Science · de
RNA-Sequenzierung zeigt unterschiedliche Expression von zirkulären RNAs beim kleinzelligen Lungenkrebs
Warum winzige RNA‑Schleifen die Lungenkrebsversorgung verändern könnten
Kleinzelliger Lungenkrebs gehört zu den tödlichsten Krebsarten: Er breitet sich schnell aus und ist oft gegen Chemotherapie resistent. Ärztinnen und Ärzte haben nach wie vor keine guten Tests, um ihn früh zu erkennen oder vorherzusagen, wer auf eine Behandlung anspricht. Diese Studie untersucht eine ungewöhnliche Gruppe genetischer Moleküle, die zirkulären RNAs — winzige RNA‑Schleifen, die in unseren Zellen überraschend stabil sind — um zu prüfen, ob sie das aggressive Tumorwachstum antreiben und ob sie als neue, verlässlichere Biomarker dienen könnten.
Das aggressivste Lungenkrebs verstehen
Kleinzelliger Lungenkrebs (SCLC) macht nur etwa einen von fünf Lungenkrebsfällen aus, verursacht aber einen überproportionalen Anteil der Todesfälle, weil er schnell wächst, früh streut und nach Chemotherapie meist wiederkehrt. Die meisten Patientinnen und Patienten werden in einem fortgeschrittenen Stadium diagnostiziert, wenn eine Operation nicht möglich ist und Gewebeproben knapp sind. Während Forschende viele DNA‑Mutationen im SCLC kartiert haben, ist wenig bekannt darüber, wie nicht‑kodierende RNAs — Moleküle, die keine Proteine herstellen, aber das Zellverhalten stark beeinflussen — die Krankheit formen. Zirkuläre RNAs (circRNAs) sind besonders interessant, weil ihre geschlossene Schleifenstruktur sie widerstandsfähiger gegen Abbau macht als gewöhnliche RNAs, was die Hoffnung weckt, dass man sie zuverlässig im Gewebe oder sogar im Blut messen könnte.
Auf der Suche nach RNA‑Schleifen im Tumorgewebe
Das Forschungsteam in Indien sammelte Tumorbiopsien von Patientinnen und Patienten mit neu diagnostiziertem SCLC und verglich sie mit normalem Lungengewebe von Personen, die sich einer Operation wegen frühzeitigem nicht‑kleinzelligem Lungenkrebs unterzogen. Mithilfe hochdurchsatzfähiger RNA‑Sequenzierung durchsuchten sie mehr als 26.000 Stellen, an denen sich zirkuläre RNAs bilden können, und filterten und analysierten die Daten, um jene circRNAs zu identifizieren, die sich wirklich zwischen krebsartigen und nicht‑krebsartigen Proben unterschieden. Sie fanden 23 zirkuläre RNAs mit signifikant veränderter Aktivität im SCLC: 13 waren in Tumoren erhöht und 10 vermindert im Vergleich zum normalen Lungengewebe. Diese Moleküle stammten aus 21 verschiedenen Genen, was auf eine umfassende Umstellung der RNA‑Regulation im SCLC hindeutet.
Aufbau eines dreischichtigen RNA‑Steuerungsnetzwerks
Zirkuläre RNAs wirken häufig wie molekulare Schwämme, die microRNAs aufnehmen — kurze RNA‑Fragmente, die normalerweise bestimmte Gene dämpfen. Um dieses Steuerungsnetz abzubilden, nutzten die Forschenden öffentliche Datenbanken, um vorherzusagen, welche microRNAs an jede der 23 veränderten circRNAs binden könnten und welche Gene diese microRNAs wahrscheinlich regulieren. Das Ergebnis war ein dichtes dreischichtiges Netz, das 23 zirkuläre RNAs mit 241 microRNAs und etwa 7.800 protein‑kodierenden Genen verknüpft. Bei der Untersuchung der Funktionen dieser Gene gruppierten sich viele in Bereichen wie Zellzykluskontrolle, Proteinabbausysteme, Stressantworten und bekannten Krebswegen wie p53, MAPK, Hippo und zellulärer Alterung. Anders gesagt: Die fehlregulierten RNA‑Schleifen scheinen an Kreuzungspunkten wichtiger Wachstums‑ und Überlebensschaltkreise in SCLC‑Zellen zu sitzen.
Zwei herausragende RNA‑Schleifen mit diagnostischem Potenzial
Unter allen veränderten circRNAs ragten zwei heraus. Die eine, circLIFR genannt, war in SCLC‑Gewebe und in mehreren SCLC‑Zelllinien durchgängig vermindert gegenüber normalen Lungenzellen. Ihre Partner‑microRNAs, darunter miR‑1234‑3p und miR‑375‑3p, waren stark erhöht, was mit der Idee übereinstimmt, dass der Verlust des circRNA‑Schwamms mehr freie microRNAs zurücklässt, die krebsrelevante Gene beeinflussen. Die andere Schleife, circCAMSAP1, zeigte das gegenteilige Muster: Sie war in Tumoren erhöht, während eine ihrer berichteten microRNA‑Partnerinnen, miR‑145‑5p, deutlich verringert war. Patientinnen und Patienten, deren Krebs trotz Erstlinienchemotherapie weiter verschlechterte, hatten tendenziell höhere circCAMSAP1‑Spiegel, was auf einen Zusammenhang mit Therapieresistenz hindeutet. Bei Tests, wie gut diese Moleküle SCLC‑Gewebe von normaler Lunge unterscheiden, erzielte circLIFR besonders gute Werte mit einer Genauigkeitskennzahl (AUC) über 0,9, während circCAMSAP1 und die zugehörigen microRNAs moderate, aber weiterhin nützliche diagnostische Aussagekraft zeigten.
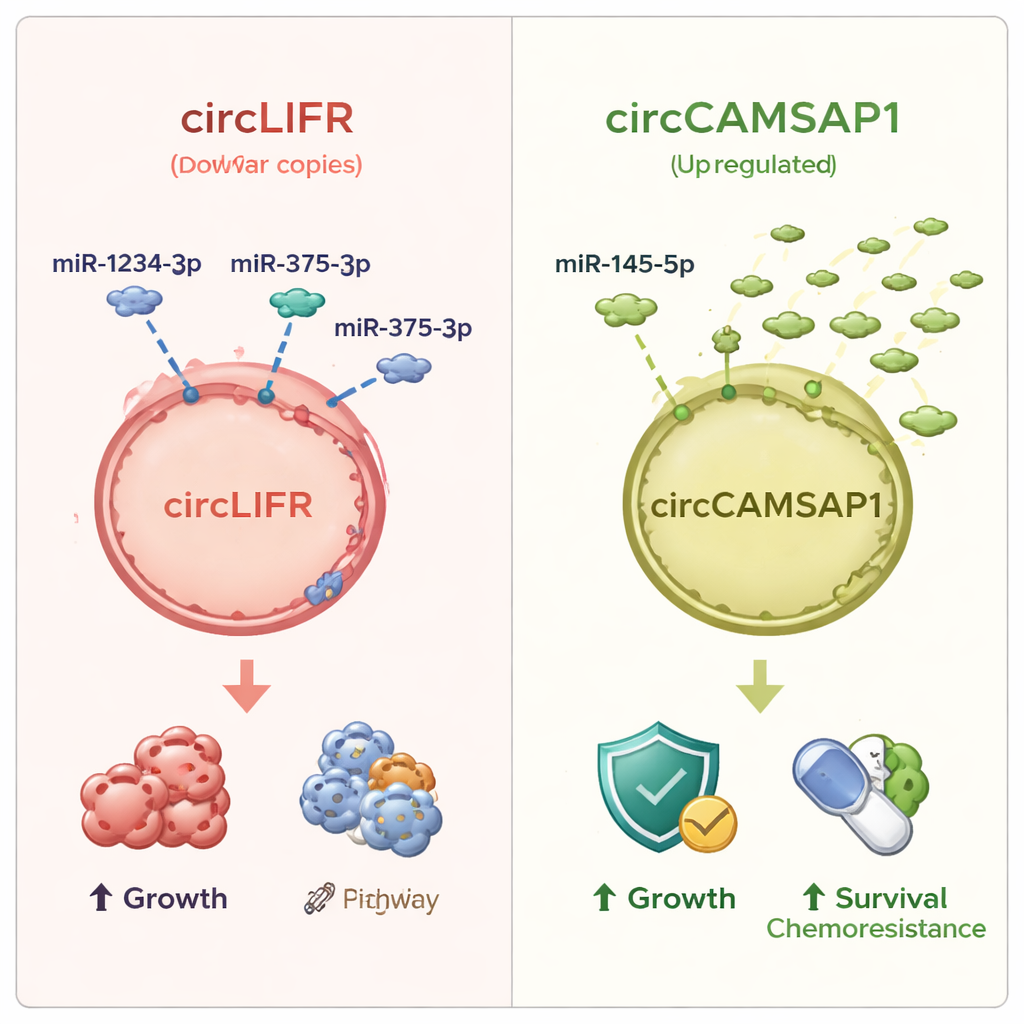
Was das für Patientinnen und Patienten bedeuten könnte
Für Nichtfachleute lässt sich zusammenfassen: Diese Studie deckt eine neue Ebene der Kontrolle beim kleinzelligen Lungenkrebs auf — aufgebaut aus winzigen RNA‑Schleifen und ihren Partnern — die reguliert, wie schnell Tumorzellen wachsen, wie sie auf Stress reagieren und möglicherweise wie sie Chemotherapie widerstehen. Zwei spezifische zirkuläre RNAs, circLIFR und circCAMSAP1, erscheinen besonders vielversprechend: Die eine geht in Tumoren verloren, die andere nimmt zu, und zusammen mit ihren zugehörigen microRNAs können sie dabei helfen, Krebsgewebe von normalem Gewebe zu unterscheiden und Hinweise darauf geben, wie die Krankheit eines Patienten auf eine Behandlung reagieren könnte. Während diese Befunde noch Laborexperimente benötigen, um Ursache und Wirkung zu beweisen, und größere klinische Studien, um den realen Nutzen zu prüfen, deuten sie auf zukünftige Blut‑ oder Gewebetests auf Basis zirkulärer RNAs hin, die Diagnose und Behandlung eines der herausforderndsten Lungenkrebsformen verbessern könnten.
Zitation: Saxena, V., Abhilash, D., Budhraja, A. et al. RNA sequencing reveals differential expression of circular RNAs in human small cell lung cancer. Sci Rep 16, 7134 (2026). https://doi.org/10.1038/s41598-026-38145-y
Schlüsselwörter: kleinzelliger Lungenkrebs, zirkuläre RNA, microRNA, Krebs-Biomarker, RNA-Sequenzierung