Clear Sky Science · de
INHBA: ein mitochondrial-assoziiertes Pan-Zelltod-Gen, das mit der Prognose und der Immunität bei OSCC in Verbindung steht
Warum das für Mundkrebs wichtig ist
Das orale Plattenepithelkarzinom, eine häufige Form von Mundkrebs, kann Menschen grundlegende Fähigkeiten wie Sprechen, Essen und ein entspanntes Lächeln nehmen. Trotz Operation, Bestrahlung und Chemotherapie erleben viele Patienten Rückfälle und eine schlechte langfristige Überlebensrate. Diese Studie betrachtet Mundkrebs aus einer neuen Perspektive, indem sie untersucht, wie ein einzelnes Gen namens INHBA den Zelltod, die Nachbarschaft aus Stütz‑ und Immunzellen des Tumors sowie den Erfolg moderner Therapien wie der Immuntherapie mitprägt.
Ein genauerer Blick auf einen tödlichen Mundkrebs
Die meisten Kopf‑ und Halstumoren entstehen in der Mundschleimhaut, und mehr als 90 % davon sind orale Plattenepithelkarzinome (OSCC). Weltweit nehmen Neuerkrankungen und Todesfälle durch OSCC zu und dürften bis 2040 um etwa 40 % steigen. Die Standardbehandlung beruht auf Operationen kombiniert mit Strahlen‑ und Chemotherapie, doch viele Tumoren sind therapieresistent und rezidivieren. Neuere Immuntherapien, die das körpereigene Abwehrsystem aktivieren sollen, helfen nur einem Teil der Patienten. Um über Versuch‑und‑Irrtum hinauszukommen, müssen Forscher verstehen, welche Gene OSCC antreiben und wie sie mit dem Immunsystem interagieren.
Zelltod, Kraftwerke und eine neue Genkategorie
Unsere Zellen sind darauf programmiert, auf verschiedene kontrollierte Weisen zu sterben, etwa durch Mechanismen wie Apoptose, Autophagie, Ferroptose und andere. Im Krebs sind diese Todesprogramme häufig umgeschaltet, sodass Tumorzellen überleben, obwohl sie es nicht sollten. Das Team dieser Studie konzentrierte sich auf eine breite Gruppe, die sie als „Pan‑Zelltod“-Gene bezeichnen — Gene, die an der Schnittstelle mehrerer Todeswege stehen — und fokussierte weiter auf solche, die mit den Mitochondrien, den kleinen Kraftwerken der Zelle, verbunden sind. Durch die Kombination großer öffentlicher Krebsdatensätze mit einem spezialisierten Mitochondrien‑Genkatalog definierten sie eine Reihe „mitochondrien‑assoziierter Pan‑Zelltod‑Gene“ und suchten jene, die am stärksten mit dem Verhalten von OSCC und dem Patientenoutcome verknüpft sind.
INHBA unter vielen Verdächtigen finden
Mithilfe fortgeschrittener Statistik und neun verschiedener Machine‑Learning‑Algorithmen filterten die Forschenden tausende Gene und identifizierten 19 mitochondriale Pan‑Zelltod‑Gene mit starker Beziehung zur Prognose bei OSCC. Unter diesen stach INHBA hervor. Seine Aktivität war in Tumorproben konsistent höher als im normalen Mundgewebe und mit schlechterem Überleben sowohl bei OSCC als auch in der größeren Gruppe der Kopf‑Hals‑Tumoren verbunden. Bei Aufteilung der Tumoren in INHBA‑hoch und INHBA‑niedrig zeigten die hoch-exprimierenden Proben aggressivere biologische Signale, einschließlich Pfade, die mit Gewebeinvasion, Angiogenese und mitochondrialem Stress zusammenhängen. Laboruntersuchungen an Patientenproben bestätigten, dass die INHBA‑Expressionslevel in realen Tumoren tatsächlich erhöht sind.
Die verborgene Rolle der Stütz‑ und Umgebungszellen
Um herauszufinden, wo INHBA am stärksten aktiv ist, nutzte das Team Einzelzell‑RNA‑Sequenzierung und räumliche Transkriptomik, Technologien, die Genaktivität in einzelnen Zellen und über Gewebeschnitte hinweg abbilden. Sie fanden heraus, dass INHBA nicht primär von den Krebszellen selbst produziert wird, sondern von karzinomassoziierten Fibroblasten — Stütz‑ und Umbaumzellen, die das Gewebe umgestalten und die Immunumgebung prägen. Eine bestimmte Untergruppe, die myofibroblastischen CAFs, wies besonders hohe INHBA‑Spiegel auf. Detaillierte Kommunikationskarten deuteten darauf hin, dass INHBA‑reiche Fibroblasten intensiv mit Immunzellen und Tumorzellen interagieren und so eine immununterdrückende, narbenähnliche Nische um den Tumor schaffen. Diese Mikroumgebung scheint das Tumorwachstum zu fördern und kann bestimmte Formen der Immuntherapie abschwächen.
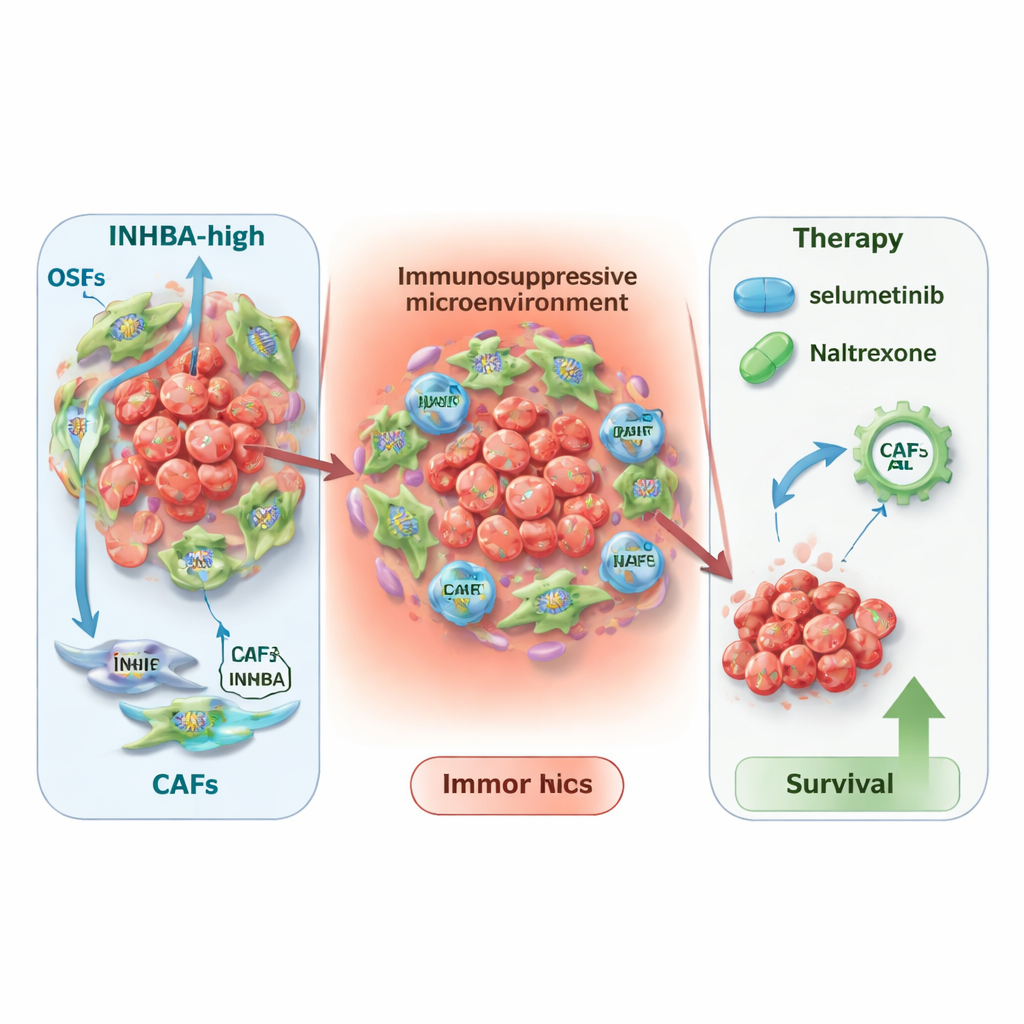
Neue Therapieansätze und breitere Bedeutung
Da INHBA ein gefährlicheres Tumorumfeld markiert, fragten die Forschenden, wie sich das therapeutisch nutzen lässt. Bei Patienten unter Immuntherapie waren niedrige INHBA‑Werte mit besseren Ergebnissen für gängige Medikamente gegen PD‑L1 oder CTLA4 verbunden, während hohe INHBA‑Werte eher auf einen größeren Nutzen von CAR‑T‑Zell‑Ansätzen hinzudeuten schienen. Durch die Auswertung zweier großer Wirkstoff‑Antwort‑Datenbanken identifizierten sie außerdem zwei bereits verfügbare Medikamente — Selumetinib und Naltrexon — als besonders vielversprechend für Tumoren mit hohem INHBA. Computermodelle zeigten, dass beide Wirkstoffe fest an das INHBA‑Protein binden könnten, was auf einen direkten Effekt hindeutet. Abschließend ergab eine Pan‑Cancer‑Analyse, dass INHBA in vielen anderen Tumorarten erhöht ist und mit schlechterem Überleben assoziiert, was darauf hindeutet, dass seine Bedeutung über Mundkrebs hinausgeht.
Was das für Patientinnen und Patienten bedeutet
Einfach ausgedrückt identifiziert diese Studie INHBA als ein „Master‑Switch“-Gen, das tödliche Mundtumoren beim Wachsen, Ausbreiten und Umgehen des Immunsystems unterstützt — vor allem durch Wirkungen in spezialisierten Stütz‑Fibroblasten und nicht allein in den Krebszellen. Die Messung von INHBA in Tumoren könnte Ärzten helfen, Hochrisikopatienten zu erkennen, vorherzusagen, wer von welchen Immuntherapien profitiert, und gezielt Medikamente auszuwählen, die in diesem Kontext besser wirken. Da INHBA in mehreren anderen Krebsarten ähnlich schädlich wirkt, könnten Therapien, die dieses Gen und seine Fibroblasten‑Partner adressieren, vielen Patientengruppen zugutekommen und die Behandlung gezielter und personalisierter machen.
Zitation: Zhang, X., Sun, M., Qiu, T. et al. INHBA: a mitochondrial-related pan-cell death gene associated with the prognosis and immunity of OSCC. Sci Rep 16, 7642 (2026). https://doi.org/10.1038/s41598-026-38131-4
Schlüsselwörter: Plattenepithelkarzinom der Mundhöhle, INHBA, Tumormikroumgebung, karzinomassoziierte Fibroblasten, Immuntherapie