Clear Sky Science · de
CDK2-Hemmung fördert neuronale Differenzierung bei Neuroblastom
Warum diese Studie über Kinderkrebs wichtig ist
Das Neuroblastom gehört zu den häufigsten soliden Tumoren bei Kleinkindern und bleibt trotz intensiver Behandlung für viele Hochrisikopatienten tödlich. Diese Studie untersucht einen neuen Ansatz: Anstatt nur zu versuchen, Krebszellen abzutöten, fragt sie, ob man sie dazu bringen kann, sich in harmlose, nervenähnliche Zellen zu verwandeln. Die Arbeit konzentriert sich auf ein Protein namens CDK2 und zeigt, dass dessen Blockade das Tumorwachstum verlangsamen und gleichzeitig die Reifung der Krebszellen fördern kann — ein möglicher Weg zu schonenderen, gezielteren Therapien.
Ein problematisches Protein in aggressiven Tumoren
Die Forschenden begannen damit, mehrere große Sammlungen von Tumorproben von Kindern mit Neuroblastom auszuwerten. Sie stellten eine einfache Frage: Wann ist das CDK2-Gen am stärksten aktiviert? Die Antwort war deutlich. Tumoren mit den höchsten CDK2-Werten waren meist in einem fortgeschrittenen Stadium, als Hochrisiko klassifiziert und neigten eher zum Rückfall nach der Behandlung. Kinder mit Tumoren, die viel CDK2 aufwiesen, hatten insgesamt eine schlechtere Prognose. Diese Krebsarten trugen häufig zusätzliche Kopien eines anderen starken krebsfördenden Gens, MYCN, und sahen unter dem Mikroskop primitiver und weniger wie normale Nervenzellen aus. Zusammen deuteten diese Muster darauf hin, dass CDK2 eng mit den gefährlichsten Formen der Erkrankung verknüpft ist.
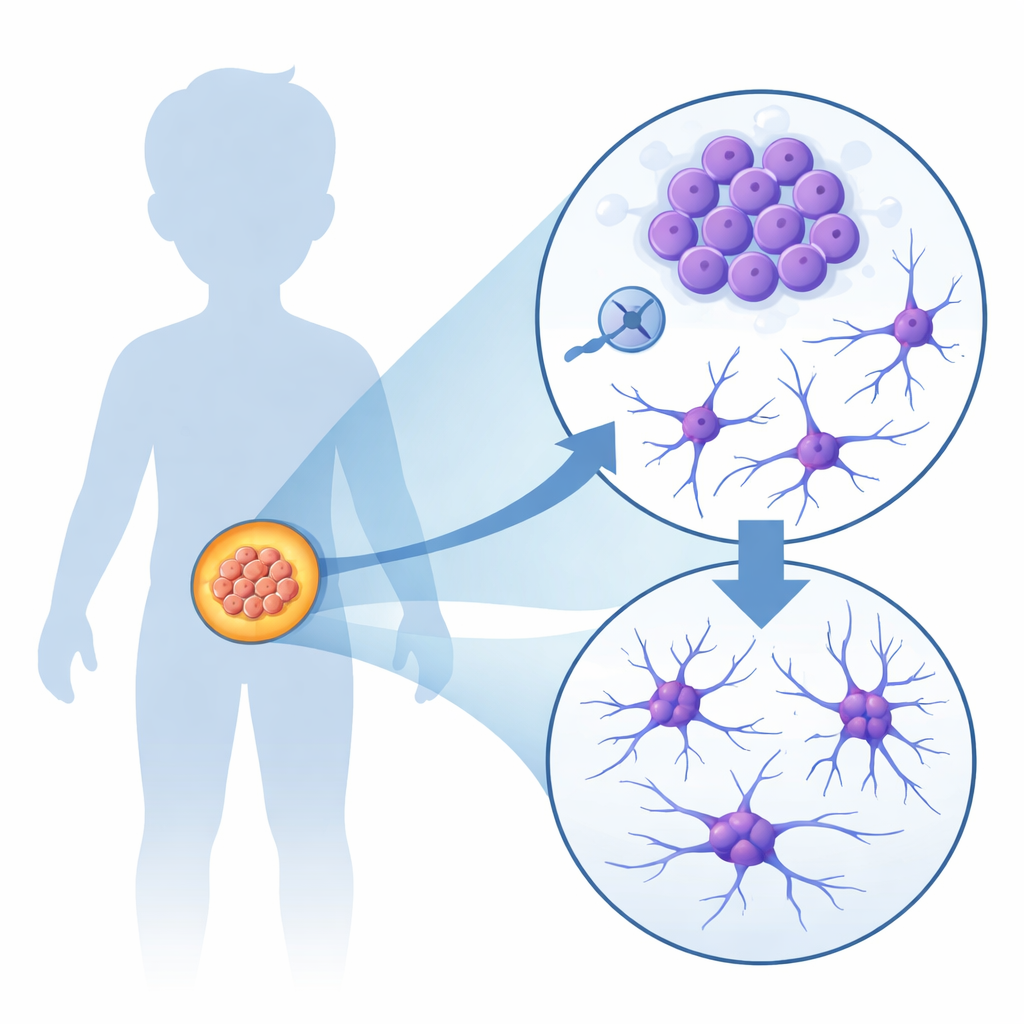
Von schnell teilenden Zellen zu nervenähnlichen Ausläufern
Um herauszufinden, was CDK2 in Tumorzellen tatsächlich bewirkt, verwendete das Team humane Neuroblastom-Zelllinien, die im Labor gezüchtet wurden. Sie schalteten entweder das CDK2-Gen aus oder blockierten das CDK2-Protein mit wirkstoffähnlichen Molekülen. In beiden Fällen geschah etwas Bemerkenswertes: Statt sich endlos zu teilen, wie Krebszellen es normalerweise tun, begannen viele Zellen, lange, dünne Ausläufer zu bilden, die den Verzweigungen sich entwickelnder Nervenzellen ähneln. Gene, die mit Nervenwachstum und Kommunikation assoziiert sind, wurden hochreguliert, während Gene, die mit Zellteilung und DNA-Reparatur verbunden sind, heruntergefahren wurden. Diese Veränderungen waren am stärksten in Zellen mit zusätzlichem MYCN ausgeprägt — genau dem Subtyp, der die aggressivste Form der Erkrankung bei Kindern verursacht.
CDK2 und MYCN: eine sich verstärkende Schleife
Tiefergehende Untersuchungen zeigten, dass CDK2 und MYCN in einer Rückkopplungsschleife miteinander verbunden sind. MYCN bindet direkt an DNA-Stellen in der Nähe des CDK2-Gens und erhöht dessen Aktivität, wodurch CDK2 in Tumorzellen hoch gehalten wird. Wenn MYCN reduziert wurde, sanken die CDK2-Werte. Umgekehrt dämpfte der Verlust von CDK2 das breitere MYC-Signalprogramm, das schnelles Wachstum antreibt. Das bedeutet, dass in vielen Hochrisikotumoren MYCN und CDK2 zusammenwirken, um die Zellen in einem schnell teilenden, unreifen Zustand zu halten und ihre natürliche Neigung zur Reifung in Nervenzellen zu blockieren.
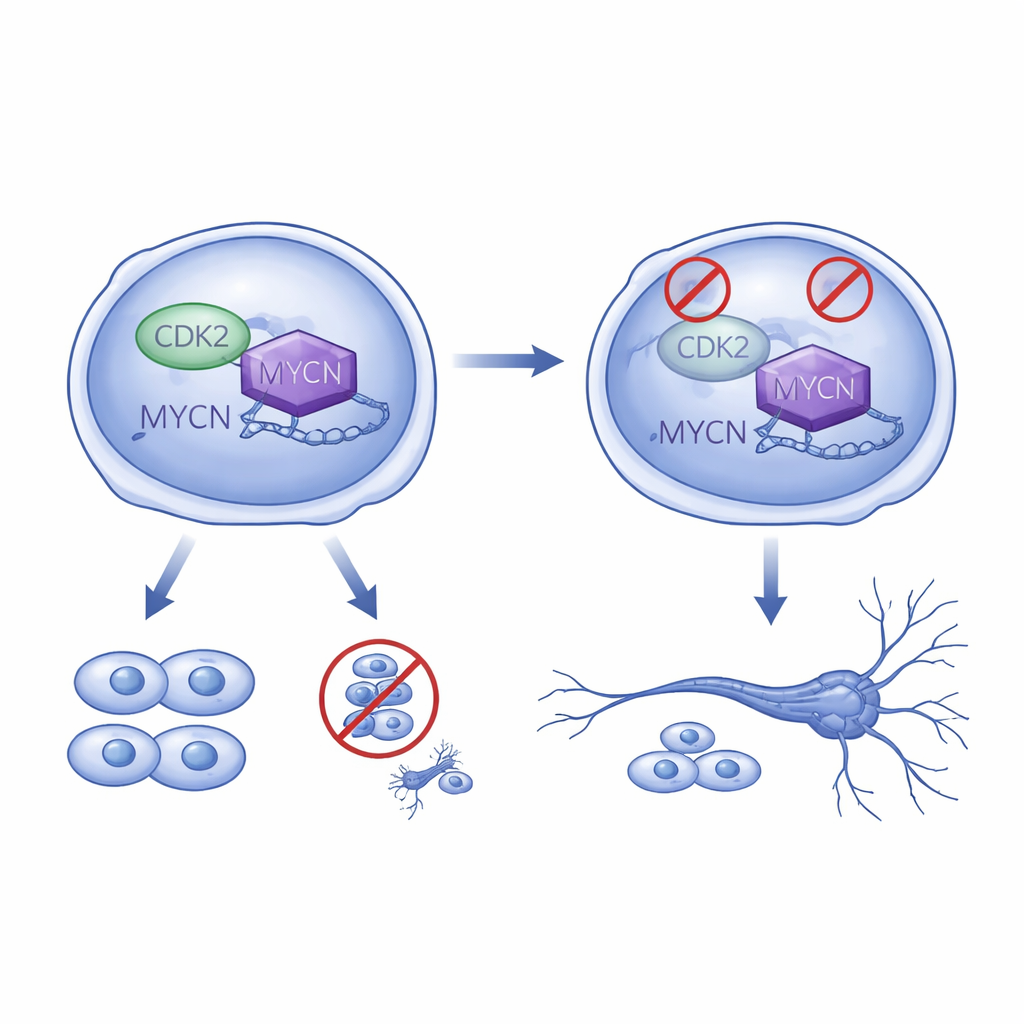
Bestehende Behandlungen stärken, indem man Zellen zur Reifung bringt
Da CDK2 und MYCN kooperieren, testeten die Forschenden Kombinationen von CDK2-blockierenden Wirkstoffen mit experimentellen MYC-gerichteten Verbindungen. In mehreren Neuroblastom-Zellmodellen reduzierten diese Wirkstoffpaare das Überleben der Zellen stärker als die Einzelsubstanzen und führten oft zu ausgeprägteren nervenähnlichen Auswüchsen, was auf eine stärkere Differenzierung hindeutet. Sie kombinierten die CDK2-Hemmung außerdem mit All-trans-Retinsäure (ATRA), einem vitamin-A-ähnlichen Wirkstoff, der bereits eingesetzt wird, um Neuroblastomzellen nach Chemotherapie zur Reifung zu bringen. In Zellkulturen erzeugte die Kombination aus CDK2-Blockern und ATRA höhere „Differenzierungswerte“ — längere Ausläufer und stärkere Nervenmarker — als Einzelbehandlungen, was auf eine mögliche Möglichkeit hinweist, eine bestehende Standardtherapie zu verbessern.
Was das für Kinder mit Neuroblastom bedeuten könnte
Vereinfacht gezeigt beweist diese Studie, dass hohe CDK2-Werte besonders aggressive, unreife Neuroblastomtumoren kennzeichnen und dass das Senken der CDK2-Aktivität Krebszellen dazu bringen kann, sich mehr wie normale Nervenzellen zu verhalten und in einigen Fällen abzusterben. Da CDK2 in dasselbe wachstumsfördernde Netzwerk wie MYCN eingebunden ist, könnte ein gleichzeitiges Angehen beider Komponenten — oder die Kombination von CDK2-Blockern mit Retinoid-Medikamenten wie ATRA — eines Tages eine wirksamere, auf Differenzierung ausgerichtete Behandlungsstrategie bieten. Obwohl diese Ergebnisse noch im Zellkulturstadium sind und sorgfältig in Tiermodellen und klinischen Studien geprüft werden müssen, skizzieren sie einen vielversprechenden Weg zu Therapien, die Tumorzellen nicht nur angreifen, sondern sie dazu bringen, „erwachsen“ zu werden und zur Ruhe zu kommen.
Zitation: Alzrigat, M., Mahmoud, L., Topçu, A.N. et al. CDK2 inhibition promotes neuronal differentiation in neuroblastoma. Sci Rep 16, 5255 (2026). https://doi.org/10.1038/s41598-026-38123-4
Schlüsselwörter: Neuroblastom, CDK2-Hemmung, neuronale Differenzierung, MYCN, Retinoid-Therapie