Clear Sky Science · de
Bovines Serumalbumin-Nanopartikel verbessern die Stabilität von Bakteriophagen und ihre antimikrobielle Wirkung gegen Pseudomonas aeruginosa
Warum es wichtig ist, nützliche Viren zu schützen
Während die Antibiotikaresistenz zunimmt, gehen Ärzten die Behandlungsmöglichkeiten für gefährliche Infektionen aus. Ein hartnäckiger Übeltäter ist Pseudomonas aeruginosa, ein Bakterium, das häufig die Lungen von Menschen mit geschwächtem Abwehrsystem befällt und vielen Wirkstoffen trotzt. Diese Studie untersucht eine kreative Strategie: man nutzt nützliche Viren, die Bakterien angreifen — sogenannte Bakteriophagen — und schützt sie in winzigen Proteinkugeln aus einem verbreiteten Blutprotein, bovinem Serumalbumin (BSA). Ziel ist es, diese Viren lange genug stabil und aktiv zu halten, damit sie hartnäckige Lungeninfektionen besser bekämpfen können.
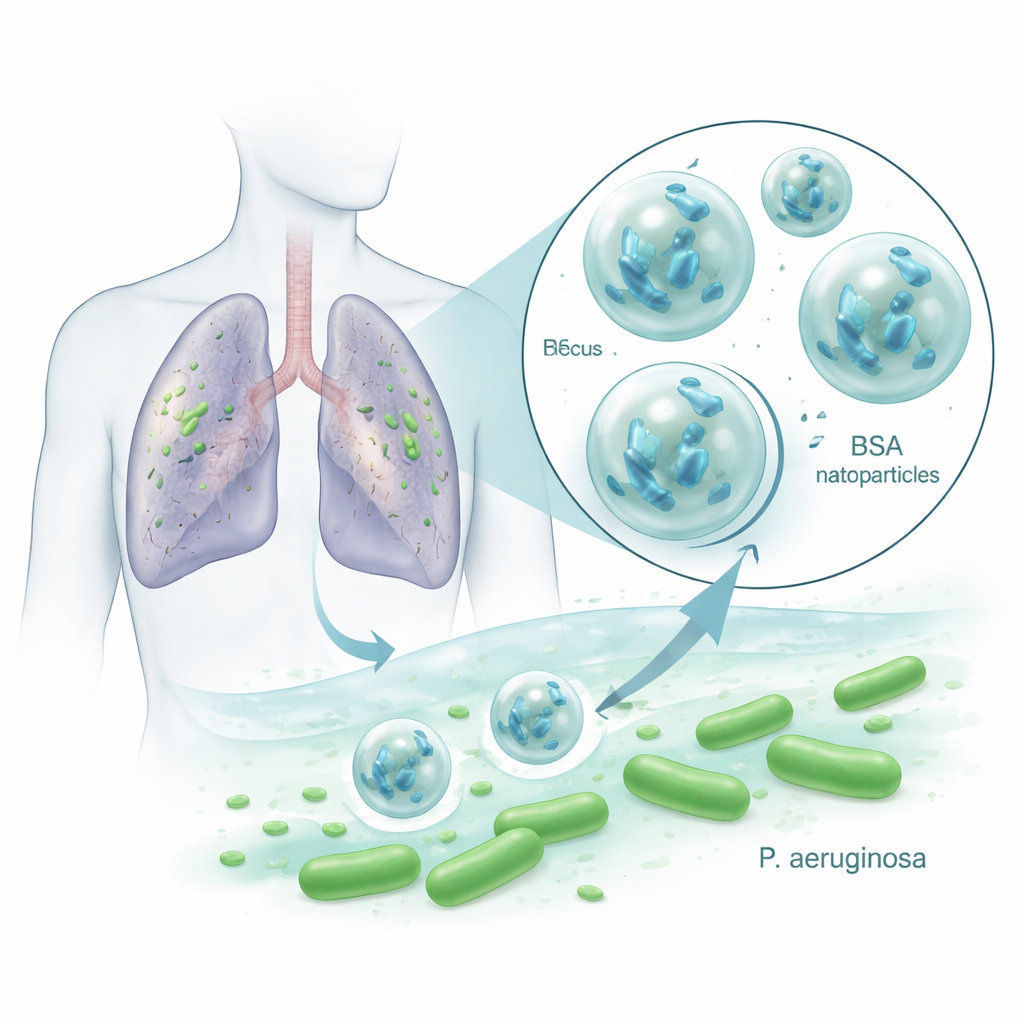
Kleine Verbündete gegen hartnäckige Lungenkeime
Pseudomonas aeruginosa ist in Krankenhäusern berüchtigt, weil es gegen mehrere Antibiotika resistent ist und schleimige Biofilme bildet, die es vor Behandlungen abschirmen. Bakteriophagen, oder Phagen, sind Viren, die spezifische Bakterien infizieren und zum Aufplatzen bringen, während sie menschliche Zellen und nützliche Mikroben weitgehend verschonen. Sie können sich überall dort vermehren, wo ihr bakterieller Wirt vorhanden ist, was sie als Ergänzung oder Alternative zu Antibiotika attraktiv macht. Phagen sind jedoch empfindlich: Hitze, Säure, Enzyme und das Immunsystem können sie schnell inaktivieren, was ihren Erfolg bei realen Patienten eingeschränkt hat. Die Forschenden wollten wissen, ob das Verpacken eines Pseudomonas-tötenden Phagen namens VAC1 in BSA-Nanopartikeln ihn schützen und die Behandlung effektiver machen könnte.
Aufbau einer schützenden Proteinhülle
Das Team musste zunächst ein Partikel entwerfen, das dem Phagen nicht schadet. Sie testeten gängige Lösungsmittel zur Herstellung von BSA-Nanopartikeln und stellten fest, dass Ethanol und Methanol VAC1 zerstörten, während Aceton dies nicht tat; daher verwendeten sie Aceton im Herstellungsprozess. Sie mischten den Phagen mit einer BSA-Lösung und fügten dann vorsichtig Aceton hinzu, sodass das Protein zu nanoskaligen Kugeln verklumpte, die mit einem Vernetzungschemikal stabilisiert wurden. Diese mit Phagen beladenen Partikel, NPPha genannt, hatten im Durchschnitt etwa 220 Nanometer Durchmesser — deutlich kleiner als eine menschliche Zelle — und schlossen über 95 % des Phagen ein. Elektronenmikroskopische Aufnahmen zeigten unregelmäßig geformte BSA-Partikel mit dichteren Bereichen, die vermutlich den Phagen entsprachen, und Tests bestätigten, dass aktive Viren über mindestens zwei Tage bei Körpertemperatur langsam freigesetzt wurden, ohne ihre Infektiosität zu verlieren.
Stärkere bakterientötende Wirkung im Labor
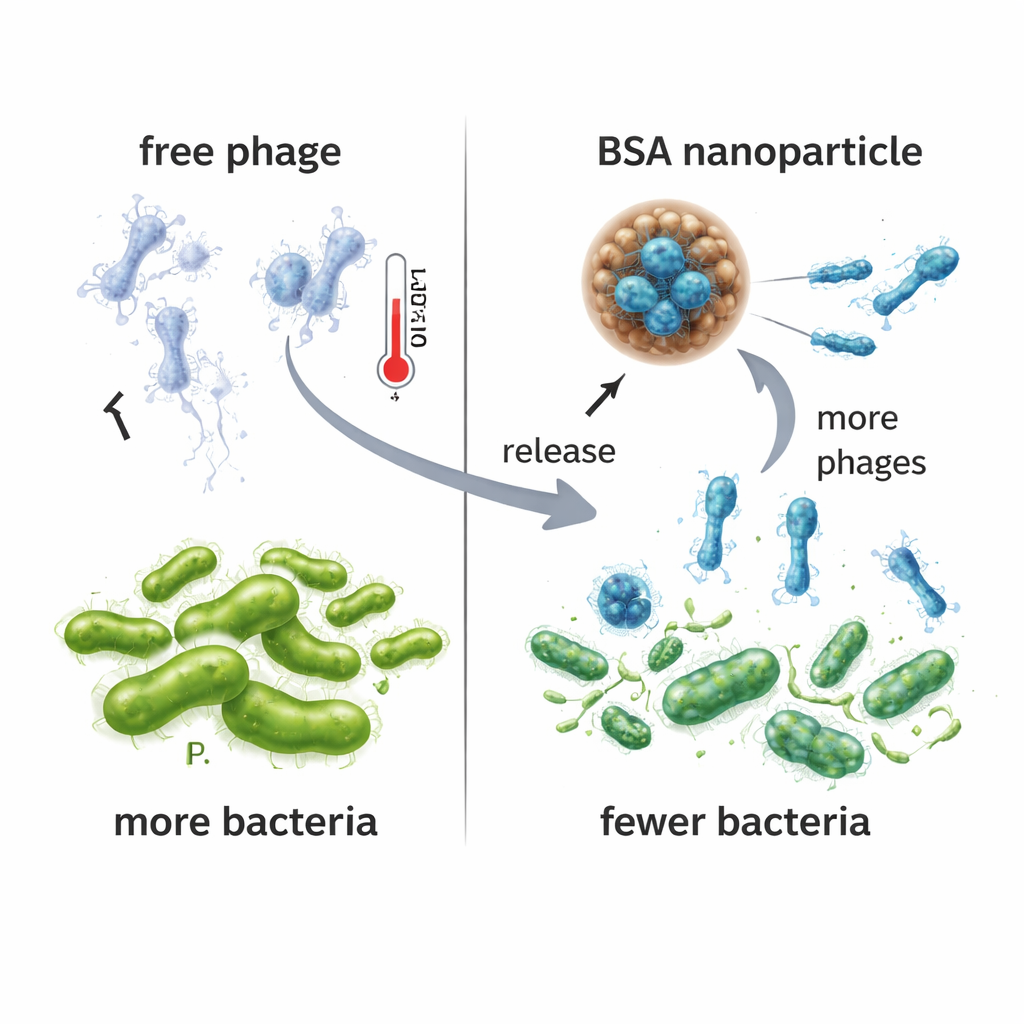
Die Forschenden verglichen dann, wie gut freier VAC1 und NPPha Pseudomonas in flüssiger Kultur kontrollierten. Wurden die Bakterien NPPha ausgesetzt, war ihr Wachstum deutlich stärker unterdrückt als bei derselben Phagenmenge allein oder mit leeren Nanopartikeln. Über 24 Stunden erzeugten Kulturen, die mit NPPha behandelt wurden, etwa hunderttausendmal mehr neue Phagenpartikel als Kulturen mit freiem VAC1, was darauf hindeutet, dass die gleichmäßige Freisetzung aus den Nanopartikeln einen länger andauernden Virus‑Bakterien‑Kampf schuf. Wichtig ist, dass die BSA‑Nanopartikel — gefüllt oder leer — in Toxizitätstests keine Schädigung von menschlichen leberabgeleiteten Zellen zeigten, was ihre potenzielle Sicherheit als Trägersystem unterstützt. Stabilitätsexperimente bei 37 °C zeigten, dass freier Phage innerhalb von zwei Tagen schnell Aktivität verlor, während Phagen in NPPha bis zu fünf Tage lang infektiös blieben.
Erprobung des Ansatzes bei infizierten Mäusen
Um zu prüfen, ob diese Vorteile auch in lebenden Tieren gelten, verwendete das Team ein Mausmodell einer akuten Pseudomonas-Lungeninfektion. Mäuse wurden über die Nase infiziert und eine Stunde später mit NPPha, freiem VAC1, leeren Nanopartikeln oder einer Kochsalzlösung behandelt. In diesem sehr schweren Modell starben alle Tiere, unabhängig von der Behandlung, innerhalb von 12 Stunden, sodass das Überleben nicht verbessert wurde. Bei Untersuchung der Lungen fanden die Forschenden jedoch, dass Mäuse, die NPPha erhalten hatten, weniger Bakterien aufwiesen und eher noch nachweisbare Phagen beherbergten als jene, die mit freiem VAC1 behandelt wurden. Gewebeschnitte aus NPPha-behandelten Lungen zeigten weniger strukturelle Schäden, dünnere Wände zwischen den Luftsäcken und geringere Anhäufung entzündlicher Zellen im Vergleich zu anderen infizierten Gruppen, was darauf hindeutet, dass die Infektion zumindest teilweise abgeschwächt war, auch wenn dies in diesem harten Modell nicht ausreichte, um die Tiere zu retten.
Was das für zukünftige Infektionsbehandlungen bedeutet
Für Nichtfachleute ist die zentrale Botschaft: Das Verpacken von Bakteriophagen in winzige, proteinbasierte Hüllen kann sie länger am Leben und wirksam halten und ihnen helfen, schwer zu behandelnde Bakterien wie Pseudomonas aeruginosa besser anzugreifen. In Reinkulturen und in Mäuselungen steigerten BSA‑Nanopartikel die Phagenzahlen, reduzierten das Bakterienwachstum und verringerten Lungenschäden, obwohl sie in einem sehr aggressiven Infektionsmodell noch nicht den Tod verhinderten. Die Arbeit legt nahe, dass Albumin‑Nanopartikel eine einfache, kostengünstige und relativ sichere Methode bieten, therapeutische Phagen zu stabilisieren. Mit verfeinerter Dosierung, besserem Timing und möglicherweise dem Einsatz in weniger extremen oder chronischen Infektionen könnten solche nano-verpackten Phagen ein wertvolles Werkzeug neben Antibiotika im Kampf gegen multiresistente Bakterien werden.
Zitation: Cunha, G.A.d., Marangoni, G.S., Durante, M.F.R. et al. Bovine serum albumin nanoparticles improve bacteriophage stability and antimicrobial activity against Pseudomonas aeruginosa. Sci Rep 16, 7146 (2026). https://doi.org/10.1038/s41598-026-38106-5
Schlüsselwörter: Phagentherapie, Nanopartikel, Pseudomonas aeruginosa, Antibiotikaresistenz, Lungeninfektion