Clear Sky Science · de
Obinutuzumab induziert lysosomale Destabilisierung durch sphingomyelin‑abhängige Hemmung von TRPML2
Warum diese Antikörper‑Geschichte von Bedeutung ist
Für viele Menschen mit B‑Zell‑Lymphomen haben moderne Antikörpertherapien eine einst durchgängig tödliche Diagnose in eine behandelbare Krankheit verwandelt. Doch nicht alle Antikörper sind gleich: Einige töten Krebszellen stärker und verlässlicher als andere. Diese Arbeit untersucht, warum ein solcher Wirkstoff, Obinutuzumab, Lymphomzellen direkter abtötet als sein Vorgänger Rituximab, indem sie auf einen unerwarteten Übeltäter tief im Zellinneren zoomt — die zelleigenen Recyclingzentren, die Lysosomen, und das feine Gleichgewicht von Lipiden und Ionenkanälen in ihren Membranen.
Vom Oberflächenziel zum inneren Selbstzerstörungssignal
Sowohl Rituximab als auch Obinutuzumab erkennen dasselbe Ziel auf B‑Zellen, ein Protein namens CD20. Die Autoren zeigen jedoch, dass Obinutuzumab viel schneller und effizienter in die Zelle aufgenommen wird. Sobald der Antikörper an CD20 auf der Zelloberfläche gebunden ist, werden die Antikörper‑Rezeptor‑Komplexe durch Endozytose ins Zellinnere gezogen und in saure Kompartimente, darunter Lysosomen, geliefert. Dort löst Obinutuzumab eine Permeabilisierung der lysosomalen Membran aus: Die normalerweise robuste Lysosomenmembran wird undicht, erlaubt Verdauungsenzyme wie Kaspasen (Kathepsine) ins Zellinnere zu entweichen und aktiviert Todeswege. Veränderungen im Salz‑ und Wasserhaushalt dieser Kompartimente, die zu einer Aufquellung der Lysosomen führen, verstärken diesen tödlichen Effekt erheblich.
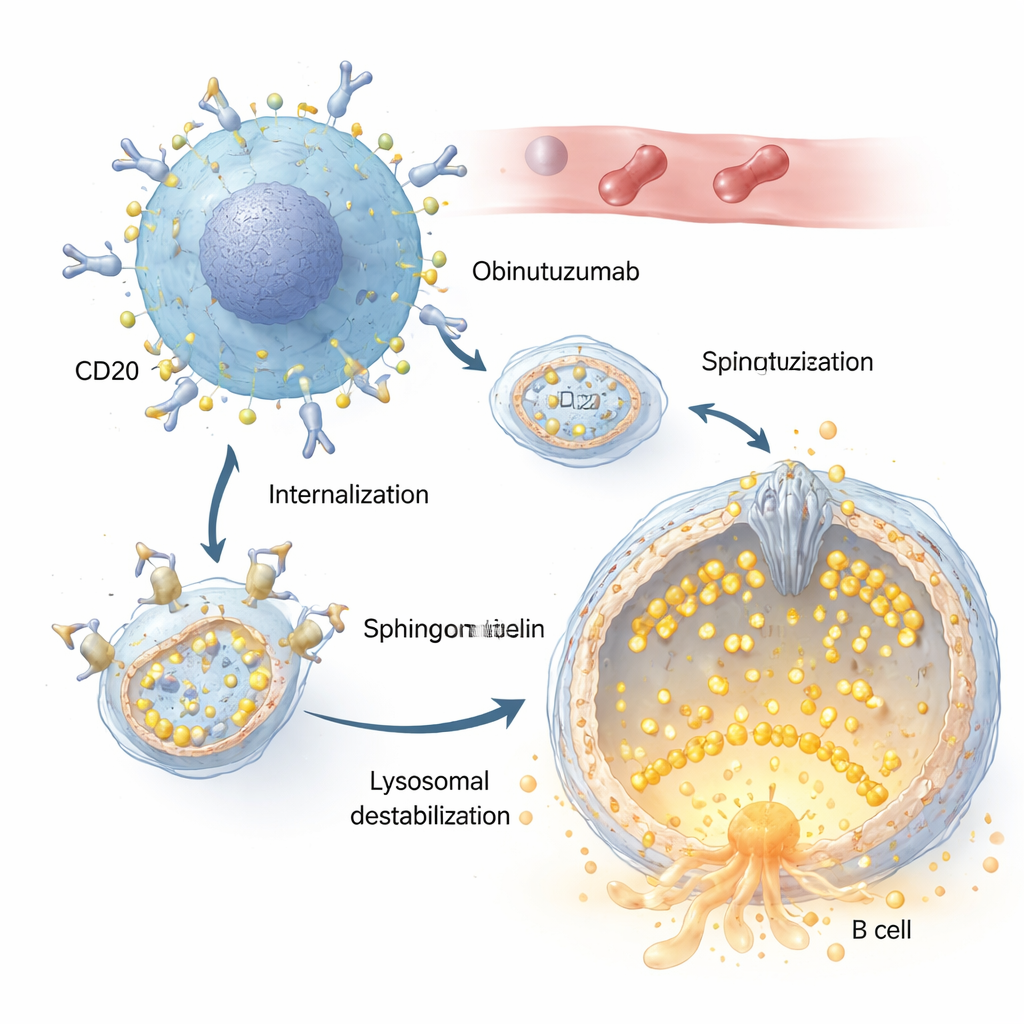
Die Rolle eines winzigen Wächterkanals
Zentral in dieser Geschichte ist TRPML2, ein in der lysosomalen Membran verankerter Calciumkanal. Unter normalen Bedingungen hilft TRPML2 den Lysosomen, mechanischen und osmotischen Stress zu bewältigen, indem es Calcium freisetzt, was Membranreparatur, Transportvorgänge und Volumenkontrolle unterstützt. Mithilfe fluoreszenter Calciumsonden und gentechnisch veränderter, calcium‑sensitive TRPML2‑Varianten zeigen die Forschenden, dass Obinutuzumab diesen Kanal schnell abschaltet: Innerhalb von Minuten nach Behandlung erzeugt ein Wirkstoff, der normalerweise TRPML‑Kanäle öffnet, keinen Calciumschub mehr. Genetische Ansätze, die TRPML2‑Spiegel reduzieren, oder kleinmolekulare Inhibitoren, die TRPML‑Aktivität blockieren, machen Lymphomzellen beide empfindlicher gegenüber Obinutuzumab, führen zu mehr lysosomaler Undichtigkeit und höheren Raten direkten Zelltods.
Wie Membranlipide das Gleichgewicht kippen
Die Studie fragt dann, was die Antikörperaufnahme mit der Kanalabschaltung verbindet. Der Blick richtet sich auf Sphingomyelin, ein in Zellmembranen reichlich vorhandenes Lipid, das bekannt dafür ist, TRPML‑Kanäle zu stören. Mit einer fluoreszenten Sphingomyelin‑bindenden Sonde finden die Autoren heraus, dass Vesikel mit Obinutuzumab, sobald sie saure Kompartimente erreichen, reich an Sphingomyelin sind, deutlich stärker als Vesikel mit Rituximab. Werden Zellen mit Sphingomyelinase behandelt — einem Enzym, das Sphingomyelin abbaut —, stellt sich die Calcium‑freisetzende Aktivität von TRPML2 selbst in Anwesenheit von Obinutuzumab wieder her. Unter diesen Bedingungen neigen Lysosomen weniger zum Austreten, und weniger Zellen sterben, was stark dafür spricht, dass angesammeltes Sphingomyelin TRPML2 deaktiviert und Lysosomen für ein Aufreißen präpariert.
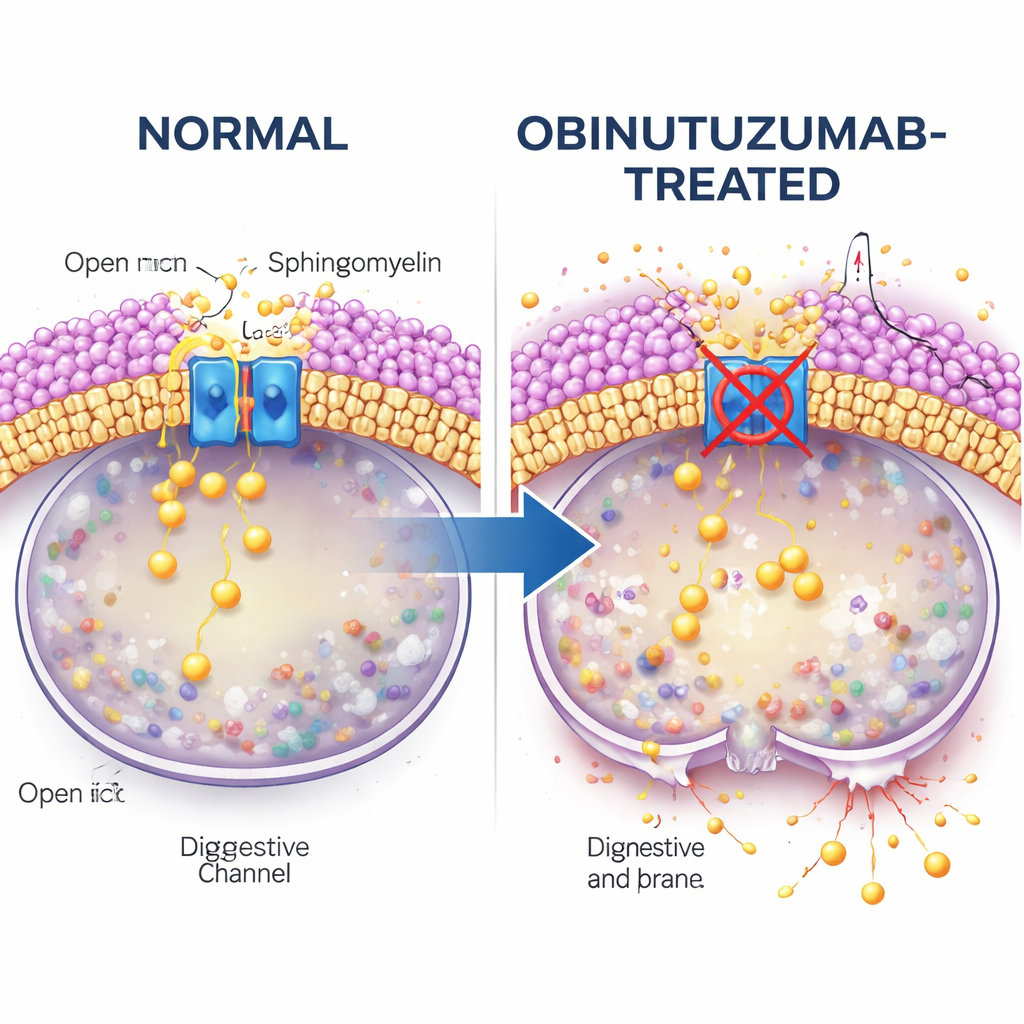
Transportwege und Cholesterinkontrollen
Auch der Weg, den Obinutuzumab in die Zelle nimmt, ist wichtig. Elektronenmikroskopie und pH‑sensitive Antikörpermarkierungen zeigen, dass Obinutuzumab die Zelloberfläche schneller verlässt und schneller in intrazelluläre Vesikel gelangt als Rituximab. Wenn die Forschenden bestimmte Aufnahmewege stören, finden sie, dass die Blockade einer cholesterinabhängigen Form der Endozytose (mit einem Wirkstoff namens Filipin) verhindert, dass Obinutuzumab TRPML2 ausschaltet, und teilweise lysosomale Schäden sowie Zelltod reduziert. Andere Endozytosehemmer zeigen diesen protektiven Effekt nicht. Das deutet auf einen spezialisierten, cholesterin‑ und sphingomyelinreichen Weg hin, der Obinutuzumab in einer Weise zu Lysosomen transportiert, die die Hemmung von TRPML2 und die anschließende Membrandestabilisierung ermöglicht.
Was das für künftige Krebsbehandlungen bedeutet
Einfach ausgedrückt zeigt diese Arbeit, dass Obinutuzumab B‑Zell‑Lymphome so effizient abtötet, weil es deren Lysosomen in einen fragilen Zustand zwingt. Indem Antikörper‑CD20‑Komplexe in sphingomyelinreiche Kompartimente getrieben werden, schaltet das Medikament indirekt einen schützenden Calciumkanal, TRPML2, aus. Fehlt diese Absicherung, platzen Lysosomen bei Stress eher auf und setzen ätzende Enzyme frei, die die Krebszelle von innen heraus zerlegen. Das Verständnis dieser Lipid‑Ionenkanal‑Achse erklärt nicht nur, warum Obinutuzumab besser ist als Rituximab; es legt auch neue Strategien nahe, Antikörpertherapien zu verstärken — etwa durch Kombination mit Wirkstoffen, die Sphingolipide modulieren oder TRPML2‑Aktivität steigern, um zu steuern, wie und wann Tumorlysosomen sich selbst zerstören.
Zitation: Oh, J., Jin, N., Kwon, S. et al. Obinutuzumab induces lysosomal destabilization via sphingomyelin-dependent inhibition of TRPML2. Sci Rep 16, 7079 (2026). https://doi.org/10.1038/s41598-026-38087-5
Schlüsselwörter: obinutuzumab, B‑Zell‑Lymphom, Lysosom, Sphingomyelin, TRPML2