Clear Sky Science · de
Verbesserung der Wundheilung mit synergistischen, zweifach beladenen elektrogesponnenen PLA/PVA-Nanofasern mit Roflumilast und L‑Arginin durch Herstellung, Optimierung und In-vivo-Bewertung
Warum schnellere Heilverbände wichtig sind
Wer schon einmal eine tiefe Schnittwunde, eine Operationsnarbe oder ein chronisches Geschwür hatte, weiß, dass das Warten auf Hautheilung langsam, schmerzhaft und riskant sein kann. Ärzte suchen nach Verbänden, die mehr leisten als bloßes Abdecken – sie wollen Pflaster, die aktiv Entzündungen dämpfen, neues Gewebe unterstützen und die Wunde feucht, aber stabil halten. Diese Studie untersucht einen neuen Typ „smarter“ Verbände aus ultrafeinen Fasern, die gleichzeitig zwei verschiedene Wirkstoffe transportieren und darauf ausgelegt sind, die Haut schneller und mit besserer Reparaturqualität verschließen zu lassen.
Ein winziges Fasergeflecht, das die Hautstütze nachahmt
Die Forschenden bauten ihren Verband aus einer luftigen Matte nanofaseriger Fäden – Stränge, die tausendfach dünner sind als ein menschliches Haar. Diese Fasern bilden ein atmungsaktives Geflecht, das der natürlichen Stützstruktur der Haut ähnelt und den Zellen eine Oberfläche bietet, an der sie sich anheften und wachsen können. Zur Herstellung nutzte das Team ein Verfahren namens Electrospinning: Flüssige Polymerlösungen werden durch ein Hochspannungsfeld zu langen, dünnen Fasern gezogen und als weiches Blatt aufgefangen. Eine Lösung basierte auf PLA, einem stabilen, langsam abbauenden Kunststoff, der bereits in medizinischen Geräten eingesetzt wird. Die andere bestand aus PVA, einem wasserfreundlichen Material, das anschwillt und hilft, Wunden feucht zu halten. 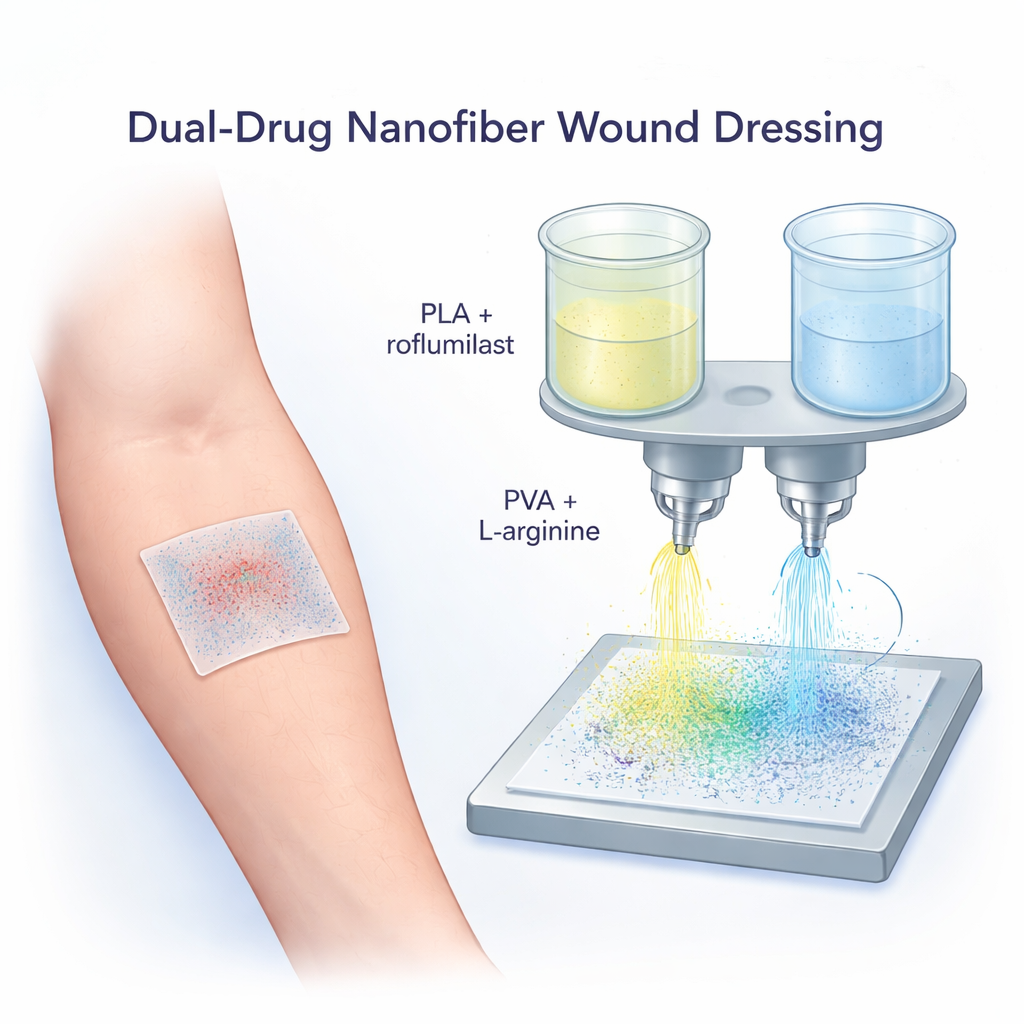
Zwei Wirkstoffe für einen doppelten Heilungseffekt
Zusätzlich zu diesem durchdachten Faserdesign luden die Forschenden jedes Polymer mit einem anderen Wirkstoff. Die PLA‑Fasern enthielten Roflumilast, ein Medikament, das eher aus der Behandlung von Lungenerkrankungen und Psoriasis bekannt ist und Entzündungen im Körper dämpft. Die PVA‑Fasern trugen L‑Arginin, eine natürliche Aminosäure, die der Körper zur Produktion von Stickstoffmonoxid nutzt, welches die Durchblutung fördert, Immunzellen unterstützt und beim Aufbau von Kollagen hilft – alles wichtige Schritte der Hautreparatur. Durch gleichzeitiges Spinnen beider Lösungen durch zwei Düsen entstand eine einheitliche Matte, in der die beiden Wirkstoffe nebeneinander in separaten, aber verflochtenen Fasern sitzen und koordiniert freigesetzt werden können.
Prüfung der Struktur und der Wasseraufnahme des Verbands
Bevor Tierversuche erfolgten, mussten die Autorinnen und Autoren zeigen, dass die Materialien sicher, stabil und gut gemischt sind. Mit Elektronenmikroskopen beobachteten sie glatte, perlenfreie Fasern mit gleichmäßiger Dicke, auch nach dem Einbringen der Wirkstoffe. Chemische Analysen bestätigten, dass beide Wirkstoffe physikalisch in der PLA/PVA‑Matrix eingeschlossen waren, ohne unerwünschte neue Verbindungen zu bilden. Röntgenanalysen zeigten, dass die Wirkstoffe innerhalb der Fasern von ihrer üblichen kristallinen Form in einen ungeordneteren, „amorpheren“ Zustand übergingen, der oft schneller und gleichmäßiger löslich ist. Das Team maß außerdem, wie die Matten Wasser aufnehmen. Die doppelt beladene Version quoll schnell auf – zunächst nahm sie über das Sechsfache ihres Trockengewichts auf – und stabilisierte sich dann auf einem gleichmäßigen Niveau, was bedeutet, dass sie Wundflüssigkeit aufnehmen und feucht halten kann, ohne in ein matschiges, brüchiges Gel überzugehen. 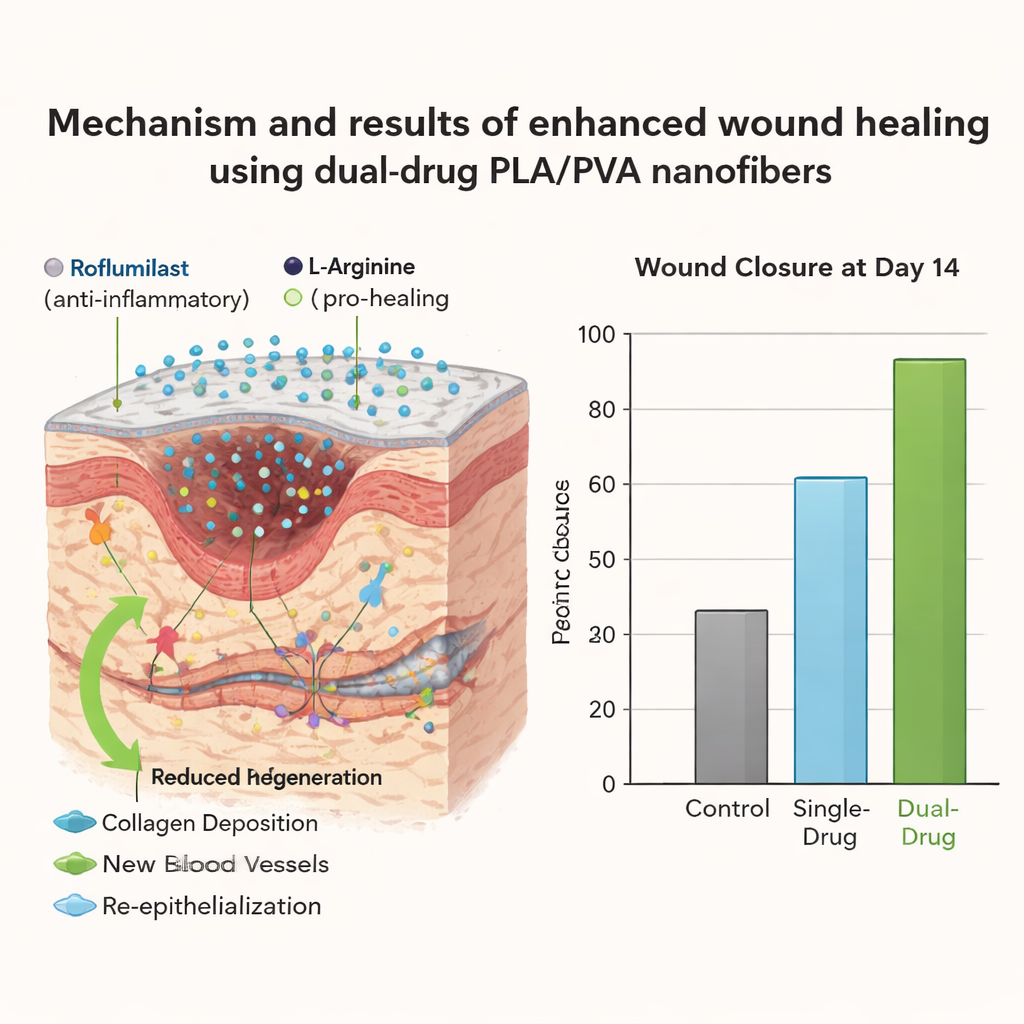
Den smarten Verband an echten Wunden testen
Um zu prüfen, ob dieses Design die Heilung tatsächlich verbessert, behandelten die Forschenden kleine, kreisrunde Hautwunden bei Ratten mit verschiedenen Versionen der Fasermatten: ohne Wirkstoff, nur mit Roflumilast, nur mit L‑Arginin oder mit beiden Wirkstoffen zusammen. Eine Kontrollgruppe erhielt nur gewöhnliche Gaze. Über zwei Wochen fotografierten sie die Wunden und maßen, wie viel der ursprünglichen offenen Fläche geschlossen war. Alle medikamentösen Matten schnitten besser ab als Gaze allein, doch der Doppelwirkstoff‑Verband hob sich deutlich ab. Am Tag 14 waren die mit Roflumilast und L‑Arginin behandelten Wunden nahezu vollständig verschlossen und erreichten etwa 99,8 % Heilung, verglichen mit deutlich langsamerem Verschluss in unbehandelten und einstoffigen Gruppen.
Blick in die Haut zur Beurteilung der Reparaturqualität
Heilen bedeutet nicht nur, eine Lücke zu schließen – die Qualität des neuen Gewebes ist entscheidend. Bei der Untersuchung dünner Hautschnitte unter dem Mikroskop zeigten die unbehandelten und einige einstoffige Gruppen noch „Granulationsgewebe“, ein Zeichen unvollständiger Reparatur, obwohl die Oberfläche geschlossen erschien. Im Gegensatz dazu zeigte die mit Roflumilast behandelte Haut reiferes Narbengewebe, und die Kombinationstherapie war insgesamt am erfolgreichsten. Diese Proben wiesen dichtes, organisiertes fibröses Gewebe, eine vollständige Wiederherstellung der äußeren Hautschicht, kein verbleibendes Granulationsgewebe und nur leichte, verbleibende Entzündungszeichen auf, was auf eine vollständigere und robustere Reparatur hindeutet.
Was das für zukünftige Verbände bedeuten könnte
Für Nicht‑Fachleute ist die Botschaft klar: Durch die Kombination eines entzündungshemmenden Medikaments und eines pro‑heilenden Nährstoffs in einem sorgfältig konstruierten Fasergeflecht hat diese Studie einen Verband entwickelt, der Wunden bei Ratten schneller und vollständiger schließen ließ als Standardverbände oder einstoffige Varianten. Obwohl weitere Studien am Menschen erforderlich sind, zeigt der Ansatz, wie Verbände der nächsten Generation direkt vor Ort die richtige Mischung aus Signalen abgeben könnten und so aus einer einfachen Abdeckung einen aktiven Partner der Wundheilung machen – mit dem Potenzial, die Genesung von Patientinnen und Patienten mit schwer heilenden Hautverletzungen zu verbessern.
Zitation: Salim, S.A., Elbadry, A.M.M., Abdelazim, E.B. et al. Enhancing wound healing with synergistic dual-drug electrospun roflumilast and L-arginine loaded PLA/PVA nanofibers through fabrication, optimization, and in vivo assessment. Sci Rep 16, 7481 (2026). https://doi.org/10.1038/s41598-026-38086-6
Schlüsselwörter: Wundheilung, Nanofaser-Verbandstoffe, Doppelwirkstofffreisetzung, Roflumilast, L‑Arginin