Clear Sky Science · de
Funktionelle Eigenschaften extrazellulärer Vesikel aus Skelettmyotuben basierend auf microRNA-Profilen: eine vergleichende Analyse mit extrazellulären Vesikeln aus mesenchymalen Stammzellen
Muskelbotschaften in winzigen Paketen
Unsere Muskeln tun weit mehr, als uns zu bewegen – sie senden beständig molekulare „Textnachrichten“ durch den Körper. Diese Studie untersucht, wie winzige Partikel, die von Muskelzellen freigesetzt werden, im Vergleich zu ähnlichen Partikeln aus weit verbreiteten Stammzellen für zukünftige Therapien abschneiden. Indem die Autorinnen und Autoren die genetischen Signale entschlüsseln, die diese Partikel tragen, stellen sie eine praktische Frage: Bei welchen Erkrankungen könnten muskelspezifische Partikel besser geeignet sein als solche aus Stammzellen?
Kleine Kurierdienste unterwegs im Körper
Alle Zellen geben mikroskopische Bläschen ab, sogenannte extrazelluläre Vesikel (EVs). Das sind nanoskalige Pakete aus Lipidmembranen, beladen mit molekularem Gepäck. Eine zentrale Fracht sind microRNAs – kurze RNA-Stücke, die Gene hoch- oder runterregeln und damit das Verhalten von Zellen prägen. Die Skelettmuskulatur, das Gewebe, das Bewegung antreibt, erweist sich als das größte sekretorische Organ des Körpers und kann besonders nach nichtinvasiven Stimuli wie Ultraschall große Mengen an EVs freisetzen. Mesenchymale Stammzellen dagegen sind bereits ein Arbeitstier in klinischen Studien; ihre EVs werden auf Gewebereparatur und die Dämpfung von Entzündungen getestet.
Den genetischen Code der Fracht lesen
Anstatt EVs direkt in Tieren oder Menschen zu testen, reanalysierten die Forschenden bestehende Sequenzierungsdatensätze, die katalogisieren, welche microRNAs in EVs aus murinen Skelettmyotuben (im Labor gezüchtete Muskelfasern) und in EVs aus Knochenmark-abgeleiteten mesenchymalen Stammzellen vorhanden sind. Muskel-EVs enthielten einige dominante microRNAs, wie miR-206-3p und miR-378a-3p, die mehr als 60 Prozent ihrer Fracht ausmachten, während Stammzell-EVs eine ausgeglichenere Mischung trugen, darunter die breit wirkende let-7-Familie. Weil jede microRNA viele Zielgene beeinflussen kann und viele microRNAs auf denselben Weg konvergieren können, entwickelten die Autoren rechnerische Methoden, um zu verstehen, wie ganze Profile – nicht nur einzelne Moleküle – zelluläre Programme umformen könnten.
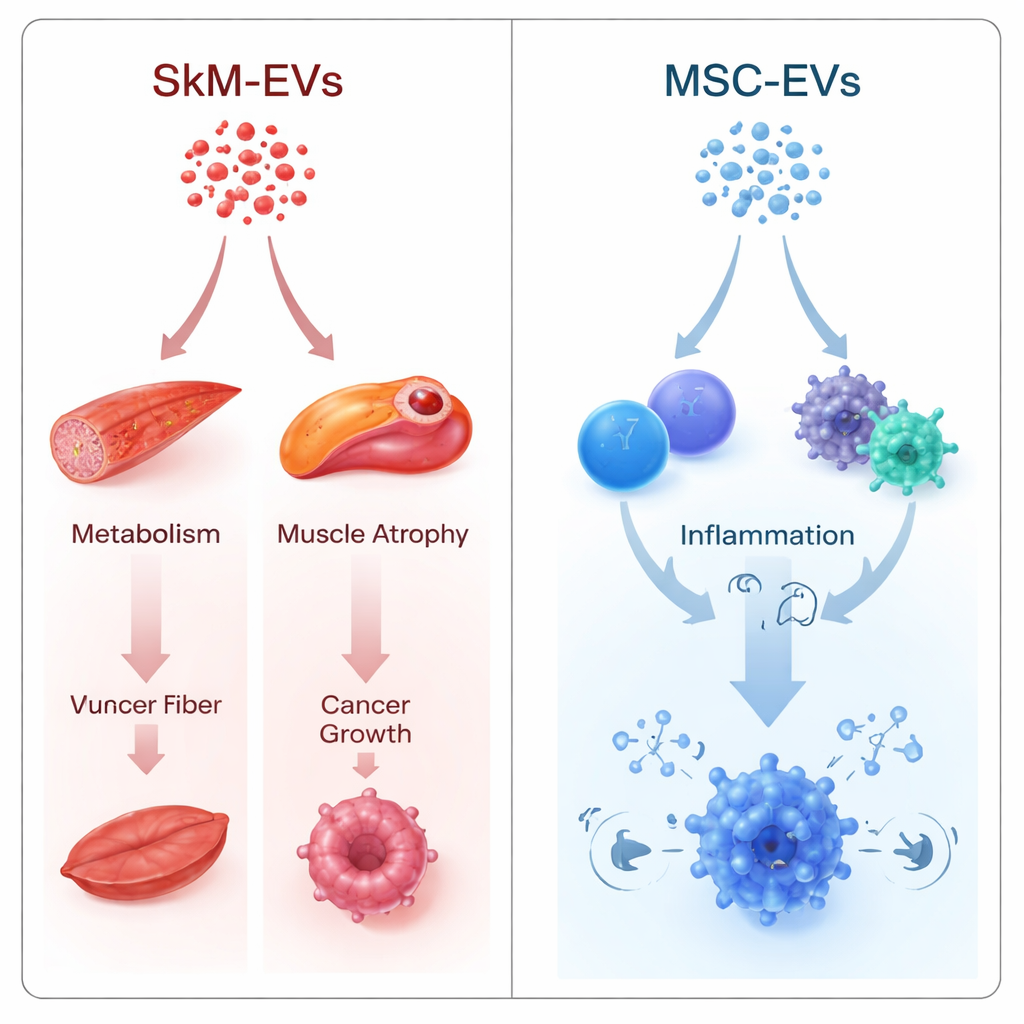
Signalwege verknüpft mit Muskel, Metabolismus und Krebs
Die Autorinnen und Autoren nutzten zwei komplementäre Strategien. Die eine verglich Muskel- und Stammzell-EVs direkt miteinander und fragte, wo sich ihre microRNAs unterschieden. Die andere behandelte jeden EV-Typ separat und wandelte sein microRNA-Profil in einen genbasierten „Impact-Score“ um, der abschätzt, wie stark die Fracht bestimmte Signalwege dämpfen könnte. Trotz unterschiedlicher Mathematik deuteten beide Ansätze in dieselbe Richtung. Muskelabgeleitete EVs zeigten eine vorhergesagte Tendenz, Signalwege zu unterdrücken, die mit Muskelschwund (FoxO- und TGF-β-Signalgebung), Blutzuckerregulation und Energiestoffwechsel (FoxO, mTOR, AMPK) sowie Tumorwachstum (ErbB-Signalweg und eine Gruppe bezeichnet als „microRNAs in cancer“) zusammenhängen. Viele der einflussreichsten Ziele waren zentrale Regulatoren der Glukoneogenese in der Leber, wichtige Treiber der Muskelatrophie und zentrale krebspromovierende Gene.
Vesikel aus Stammzellen und das Immunsystem
Stammzell-EVs erzählten eine andere Geschichte. Ihre microRNA-Fracht wurde vorhergesagt, stärker auf immunbezogene Wege einzuwirken: NF-κB-Signalgebung, Zytokin–Rezeptor-Interaktionen, B- und T-Zell-Rezeptor-Signalwege sowie Th17-Zelldifferenzierung. Diese sind zentral dafür, wie der Körper Infektionen erkennt, Entzündungen an- und abschaltet und die Identität von Immunzellen formt. Diese Neigung passt zu wachsender experimenteller Evidenz, dass Stammzell-EVs Immunantworten breit modulieren können und in Erkrankungen getestet werden, bei denen das Beruhigen von Entzündungen entscheidend ist, etwa Autoimmun- und entzündliche Erkrankungen.
Von Computervorhersagen zu künftigen Therapien
Insgesamt legt die Arbeit nahe, dass muskelspezifische EVs von Natur aus für Zustände mit Muskelschwund, gestörtem Stoffwechsel oder unkontrolliertem Zellwachstum geeignet sein könnten, während Stammzell-EVs besser zu Erkrankungen passen, die von fehlgesteuerter Immunität getrieben werden. Die Ergebnisse beruhen ausschließlich auf rechnerischer Analyse bestehender Daten und beweisen noch keinen Nutzen beim Patienten; sie berücksichtigen zudem nicht andere EV-Frachten wie Proteine oder Lipide. Dennoch bietet die Studie, indem komplexe microRNA-Profile in pathway-basierte „Fingerabdrücke“ übersetzt werden, eine Landkarte zur Zuordnung von EV-Quellen zu Krankheitstypen und hilft bei der Priorisierung jener Kombinationen, die vielversprechend sind, im Labor und schließlich klinisch getestet zu werden.
Zitation: Kawamoto, Y., Yamaguchi, A., Ma, X. et al. Functional properties of skeletal myotube-derived extracellular vesicles based on microRNA profiles: a comparative analysis with mesenchymal stem cell-derived extracellular vesicles. Sci Rep 16, 7436 (2026). https://doi.org/10.1038/s41598-026-38076-8
Schlüsselwörter: extrazelluläre Vesikel, Skelettmuskulatur, microRNA, mesenchymale Stammzellen, Zellsignalwege