Clear Sky Science · de
Entwicklung von polyethylenglykolamin–Metall-funktionalisierten Kryogelen für überlegene Katalasebindung, Aktivität und Langzeitbeständigkeit
Warum das Festhalten von Enzymen wichtig ist
Wasserstoffperoxid ist ein häufiger chemischer Nebenproduktbereich von Prozessen von der Lebensmittelverarbeitung bis zu medizinischen Anwendungen, und lebende Zellen sind auf das Enzym Katalase angewiesen, um es in harmloses Wasser und Sauerstoff zu zerlegen. In der Industrie wird Katalase jedoch meist in gelöster Form verwendet, die schnell an Aktivität verliert, sich nicht leicht zurückgewinnen lässt und häufig ersetzt werden muss. Diese Studie untersucht einen Weg, Katalase in einem schwammartigen Material „abzustellen“, sodass sie länger aktiv bleibt, vielfach wiederverwendet werden kann und effizienter arbeitet – Aspekte, die die Kosten senken und enzymbasierte Prozesse sauberer und nachhaltiger machen könnten.

Aufbau eines intelligenten Schwamms
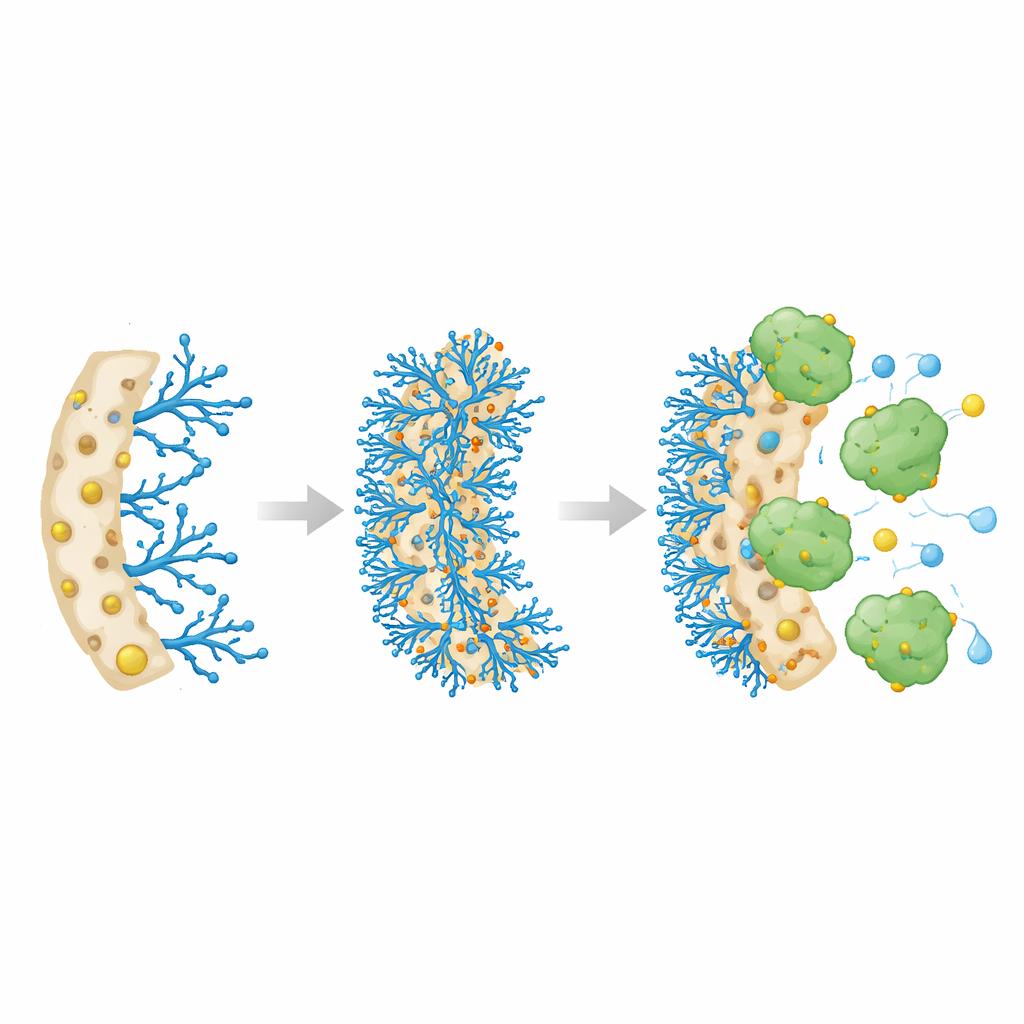
Die Forschenden entwarfen einen speziellen Polymer-Schwamm, ein sogenanntes Kryogel, das durch Einfrieren und Auftauen einer Flüssigkeitsmischung entsteht, wobei Eiskristalle große, miteinander verbundene Poren ausformen. Diese Poren lassen Flüssigkeiten frei durchströmen, ähnlich wie Wasser durch einen Luffa, während das feste Gerüst zäh und elastisch bleibt. Als Basismaterial nutzte das Team Poly(HEMA-co-GMA) und graftete chemisch ein verzweigtes, stickstoffreiches Molekül darauf: Polyethylenimin (PEI). Schließlich befestigten sie Metallionen – Kupfer, Nickel oder Kobalt – an diesen Stickstoffstellen. Die Idee war, dass die Metallionen als Andockpunkte wirken, die Katalasemoleküle stark anziehen und festhalten, ohne den Flüssigkeitsdurchfluss durch den Schwamm zu blockieren.
Materialeinstellung für beste Leistung
Um zu verstehen, wie jeder Schritt des Designs das Material veränderte, verwendete das Team mehrere Labortechniken, um Struktur, Chemie und Stabilität zu untersuchen. Sie zeigten, dass das Hinzufügen von PEI und anschließend von Metallen das poröse Netzwerk nicht zum Kollaps brachte, sondern die Wasserhaltekapazität des Schwamms tatsächlich erhöhte, was günstig ist, um Enzyme in einem komfortablen, aktiven Zustand zu erhalten. Unter den drei Metallen erzeugte Kupfer die am besten hydratisierte und geordnete Umgebung. Mikroskopische Aufnahmen zeigten, dass das Ausgangsmaterial wie gepackte Granulate aussah, während die PEI- und Metall-behandelten Varianten zu einem saubereren, kontinuierlicheren Netzwerk großer Poren aufgingen. Messungen des Metallgehalts bestätigten, dass sich Kupfer stärker und in höheren Mengen anlagerte als Nickel oder Kobalt, was darauf hindeutet, dass es die effektivsten Andockstellen für Katalase bieten würde.
Katalase fest verankern
Als Katalase in die verschiedenen metallbeladenen Schwämme eingebracht wurde, banden alle drei das Enzym schnell, doch die Kupfervariante fiel besonders auf. Sie lud die höchste Menge an Katalase – etwa 392 Milligramm pro Gramm Trockenschwamm – und erreichte innerhalb von etwa acht Stunden ein Gleichgewichtsniveau. Die Forschenden untersuchten dann, wie gut das immobilisierte Enzym im Vergleich zur freien Katalase in Lösung arbeitete. Obwohl die maximale Reaktionsgeschwindigkeit pro Gramm Enzym etwas abnahm, zeigte die immobilisierte Katalase eine deutlich stärkere scheinbare Affinität zu ihrem Substrat, Wasserstoffperoxid. Praktisch bedeutet das, dass das gebundene Enzym seine Aufgabe bei niedrigeren Substratkonzentrationen effizienter erfüllte, vermutlich weil der poröse, wassergefüllte Kupferschwamm das Substrat in der Nähe des Enzyms konzentrierte und dessen aktive Konformation unterstützte.
Ein Enzym, das durchhält
Einer der größten Vorteile der Enzymimmobilisierung ist die Aussicht auf Wiederverwendbarkeit und lange Lagerfähigkeit. Hier erwies sich die an das kupferbasierte Kryogel gebundene Katalase als deutlich langlebiger als ihr freies Pendant. Nach 15 wiederholten Einsatzzyklen behielt das immobilisierte Enzym noch etwa ein Drittel seiner Anfangsaktivität, während freie Katalase typischerweise nach einem einzigen Einsatz verworfen würde. In Lagerungstests bei Kühlschranktemperatur über 70 Tage hielt die immobilisierte Katalase mehr als 60 % ihrer Aktivität – etwa das Doppelte der freien Form. Der Schwamm erlaubte außerdem, das Enzym mit einer einfachen Salzlösung zu lösen und wieder aufzuladen, sodass das Material selbst mehrfach wiederverwendet werden kann, ohne große Kapazitätsverluste.
Was das für die Praxis bedeutet
Für Nicht-Spezialisten lautet die Hauptbotschaft, dass die Forschenden eine Art wiederverwendbaren „Enzymschwamm“ gebaut haben, der Katalase fest, aber schonend hält, wodurch sie bei niedrigeren chemischen Konzentrationen besser arbeitet und in Gebrauch sowie Lagerung deutlich länger hält. Durch die Kombination eines hochporösen Kryogels mit PEI und Kupferionen schufen sie eine Plattform, die hohe Enzymladung, verbesserte Effizienz und starke Langzeitstabilität vereint. Solche Materialien könnten in industrielle oder umwelttechnische Systeme integriert werden, um Wasserstoffperoxid und verwandte Stoffe zuverlässiger und mit weniger Abfall abzubauen – ein praxisnaher Schritt hin zu grüneren, enzymgetriebenen Technologien.
Zitation: Erol, K., Alkan, M.H. & Alacabey, İ. Engineering polyethylenimine–metal functionalized cryogels for superior catalase binding, activity, and long-term durability. Sci Rep 16, 7880 (2026). https://doi.org/10.1038/s41598-026-38040-6
Schlüsselwörter: Enzymimmobilisierung, Katalase, Kryogel, kupferfunktionalisierte Polymere, Biokatalyse