Clear Sky Science · de
Untersuchung der onkogenen Rolle des fehlregulierten EZH2 beim Hepatoblastom
Warum diese Krebsgeschichte für Familien wichtig ist
Hepatoblastom ist ein seltener, aber schwerwiegender Leberkrebs, der vorwiegend sehr kleine Kinder betrifft. Die heutigen Behandlungen beruhen weitgehend auf intensiver Chemotherapie und umfangreichen Operationen, manchmal sogar auf Lebertransplantationen, die bleibende Nebenwirkungen hinterlassen können. Diese Studie stellt eine hoffnungsvolle Frage: Gibt es einen molekularen „Hauptschalter“, der dieses Krebswachstum antreibt und den man abschalten könnte, um die Behandlung präziser und wirksamer zu machen?
Ein verborgener Schalter in Lebertumorzellen
Die Forscher konzentrierten sich auf ein Protein namens EZH2, das Teil der Maschinerie ist, die steuert, welche Gene ein- oder ausgeschaltet werden, ohne die DNA selbst zu verändern. Mithilfe einer leistungsfähigen Methode, die die Aktivität von Tausenden Genen in einzelnen Zellkernen liest, untersuchten sie sowohl Tumorgewebe als auch benachbarte gesunde Leber von Kindern mit Hepatoblastom. Sie entdeckten eine spezielle Gruppe von Tumorzellen, die von Leberzellen abstammen, aktiv teilten und sehr hohe EZH2‑Spiegel aufwiesen. Diese sogenannten „zyklischen“ Tumorzellen kamen in der aggressivsten, embryonalen Form der Erkrankung deutlich häufiger vor als im umgebenden Lebergewebe.
Was diese Tumorzellen so aggressiv macht
Durch den Vergleich von Genaktivitätsmustern fand das Team heraus, dass die EZH2‑reichen Tumorzellen von Signalen durchzogen waren, die schnelle Zellteilung und Veränderungen in der Chromosomenstruktur fördern. Sie sahen außerdem Hinweise darauf, dass normale Wachstums‑Kontrollwege verändert waren, was nahelegt, dass EZH2 nicht nur schützende Gene stilllegt, sondern auch andere krebsrelevante Signalwege auf unerwartete Weise umprogrammiert. Beim Blick auf Patientenproben unter dem Mikroskop bestätigten sie, dass EZH2‑Protein besonders in embryonalen Bereichen der Tumoren reichlich vorhanden war und oft in Zellen zu finden war, die sich gerade teilen. Interessanterweise stiegen andere Komponenten des EZH2‑Proteincomplexes nicht immer im gleichen Maß an, was andeutet, dass EZH2 sowohl über klassische Gen‑Silencing‑Rollen als auch über weniger traditionelle, „außerhalb des Drehbuchs“ liegende Mechanismen wirken könnte.
Genetische Hinweise und verwundbare Schwachstellen
Das Team durchsuchte außerdem die DNA von Tumoren von 11 Kindern nach Veränderungen in Genen, die an dieser Maschinerie beteiligt sind. Jedes Tumorexemplar trug Varianten in EZH2 und einem weiteren Komplexmitglied, SUZ12; die meisten zeigten zudem Mutationen in CTNNB1, einem bekannten Treiber von Lebertumoren. Während diese speziellen EZH2‑ und SUZ12‑Varianten noch nicht als eigenständig schädlich nachgewiesen sind, deutet ihr Vorhandensein neben starker EZH2‑Überaktivität darauf hin, dass sie die Funktion des Komplexes subtil verändern könnten. Gesamtgenexpressionsanalysen über viele Tumoren hinweg zeigten, dass EZH2 und mehrere Gene der Zellteilung konsistent höher im Tumor als in normaler Leber waren, während einige Gene, die normalerweise Wachstum und Gewebsorganisation kontrollieren, reduziert waren.
EZH2 drosseln, um Chemotherapie zu verstärken
Um zu prüfen, ob EZH2 mehr als ein bloßer Zuschauer ist, behandelten die Forscher Leberkrebs‑Zelllinien und patientenabgeleitete Tumorzellen im Labor mit Wirkstoffen, die EZH2 blockieren, und setzten sie anschließend Cisplatin, einem Standardchemotherapeutikum, aus. Allein hatten die EZH2‑Inhibitoren nur moderaten Effekt. In Kombination mit Cisplatin jedoch wurden viele Hepatoblastom‑Zellen deutlich empfindlicher und starben bei niedrigeren Chemotherapie‑Dosen, besonders in Zelllinien, die den aggressiven pädiatrischen Tumoren ähneln. In einem Mausmodell mit menschlichem Hepatoblastomgewebe schrumpften Tumoren unter der Kombination von EZH2‑Blockade und Cisplatin stärker als unter einer der beiden Behandlungen allein; außerdem wurde eine chemische Markierung (H3K27me3), die mit EZH2‑Aktivität verknüpft ist, reduziert — ein Hinweis darauf, dass das Medikament sein beabsichtigtes Ziel im lebenden Gewebe traf.
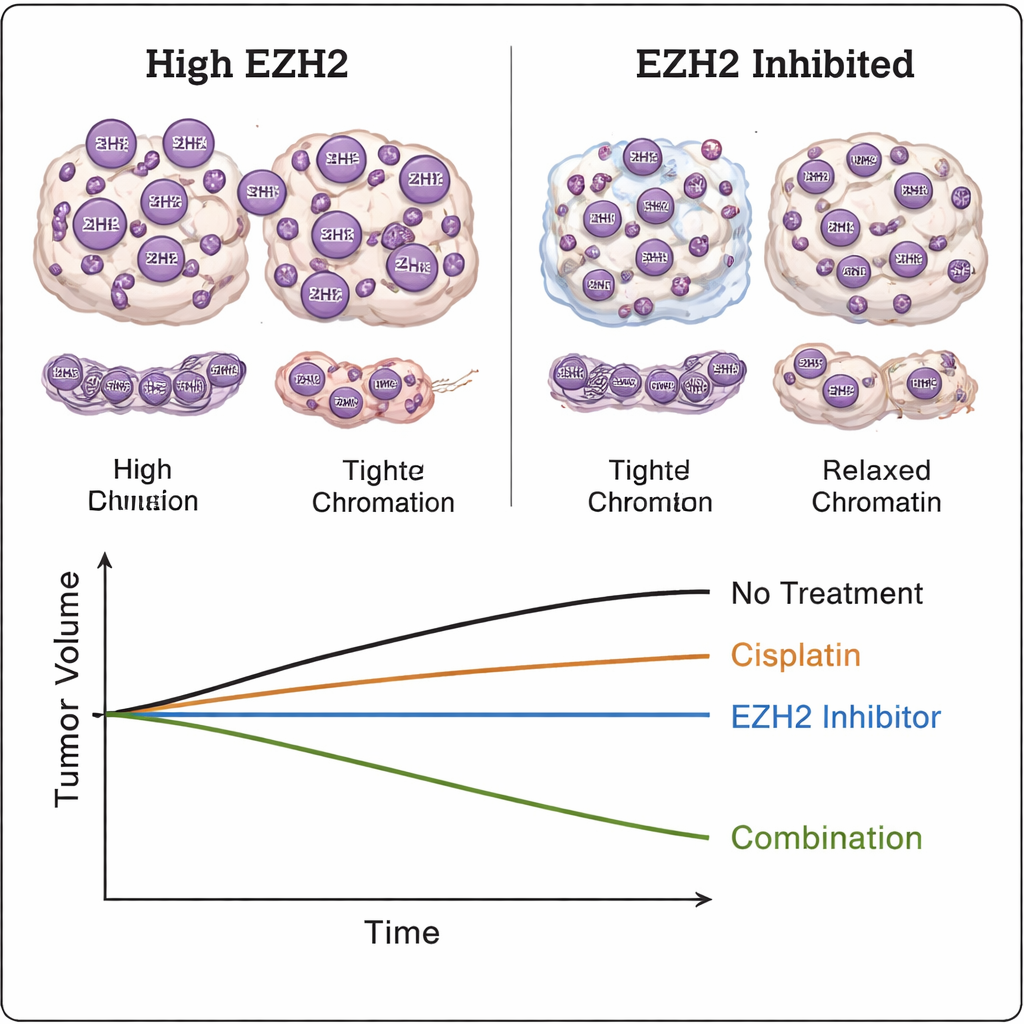
Was das für Kinder mit Leberkrebs bedeuten könnte
Zusammengefasst zeichnen die Ergebnisse EZH2 als zentralen Treiber einer schnell wachsenden, therapieresistenten Zellpopulation im Hepatoblastom, insbesondere im embryonalen Subtyp, der tendenziell aggressiver ist. Durch das Herunterregeln von EZH2 könnten Ärzte eines Tages diese schwer auszurottenden Zellen schwächen und bestehende Chemotherapien wirksamer machen, möglicherweise bei niedrigeren Dosen. Obwohl weitere Forschung und klinische Studien nötig sind, bevor solche Strategien in die Klinik gelangen, liefert diese Arbeit die wissenschaftliche Grundlage dafür, EZH2 als neues, zielgerichteteres Behandlungsziel für Kinder mit diesem seltenen Leberkrebs in Betracht zu ziehen.
Zitation: Glaser, K., DePasquale, E.A.K., Berklite, L. et al. Investigating the oncogenic role of aberrant EZH2 in hepatoblastoma. Sci Rep 16, 7563 (2026). https://doi.org/10.1038/s41598-026-38038-0
Schlüsselwörter: Hepatoblastom, EZH2, pädiatrischer Leberkrebs, epigenetische Therapie, Cisplatin