Clear Sky Science · de
Chronische NH4Cl-Belastung verbessert die Glukosetoleranz, ohne die Insulinsensitivität bei Mäusen zu verändern
Warum das Säure-Basen-Gleichgewicht für den Blutzucker wichtig ist
Menschen mit chronischer Nierenerkrankung entwickeln häufig eine sogenannte metabolische Azidose, bei der das Blut leicht saurer als normal ist. Ärztinnen und Ärzte betrachten das meist als schädlich, unter anderem weil kurzzeitige Azidoseepisoden dafür bekannt sind, die Blutzuckerregulation zu verschlechtern. Diese Studie stellt diese Vorstellung teilweise auf den Kopf: Bei Mäusen verbesserte eine anhaltend milde Azidose tatsächlich den Umgang des Körpers mit Zucker, ohne dass das Hormon Insulin stärker oder schwächer wirkte. Das Verständnis dieser überraschenden Beobachtung könnte langfristig helfen, Therapien für Nierenerkrankungen und Typ‑2‑Diabetes zu verfeinern.
Eine Langzeit‑Säurebelastung bei Mäusen
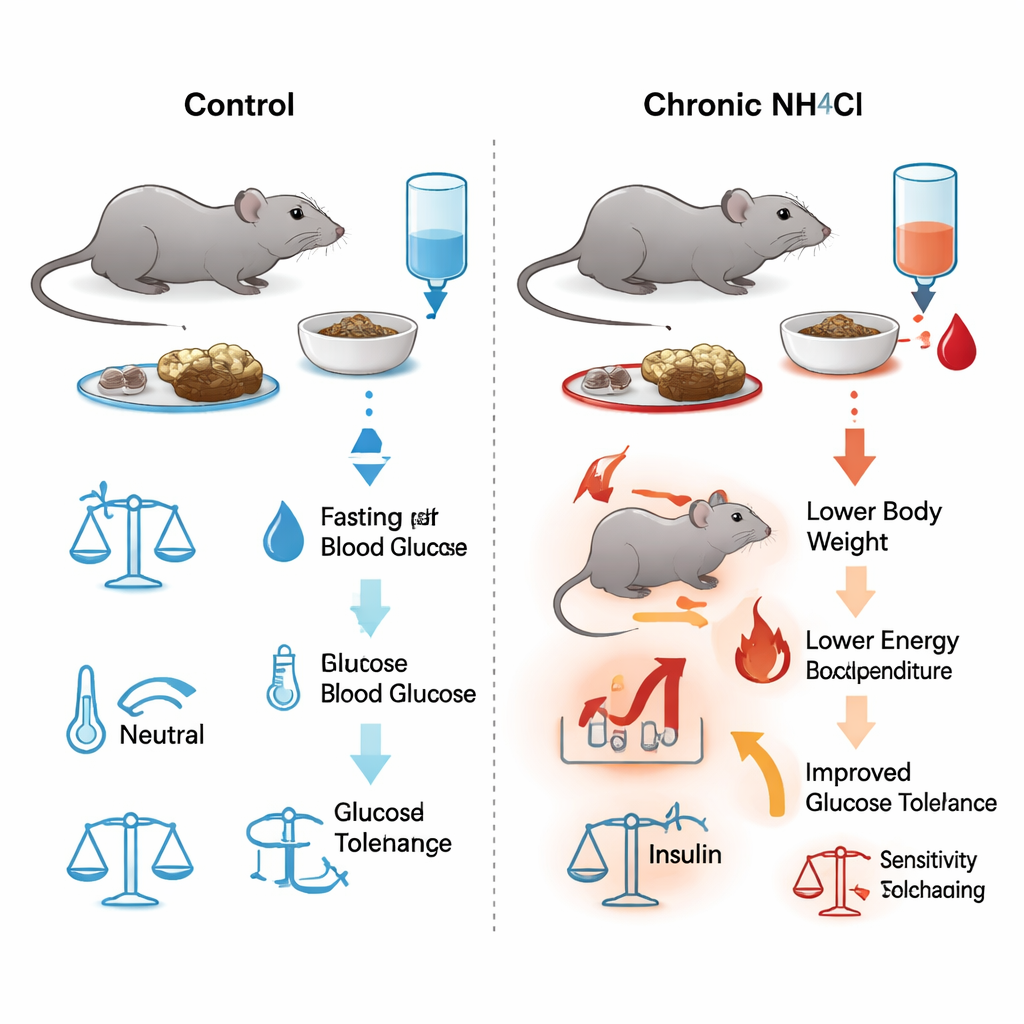
Die Forschenden versorgten männliche Mäuse bis zu sechs Monate lang mit Trinkwasser, das Ammoniumchlorid enthielt — ein Salz, das das Blut sanft ansäuert. Diese Behandlung ahmt die chronische Säurebelastung nach, wie sie bei Nierenerkrankungen vorkommt. Bluttests bestätigten eine anhaltende, milde metabolische Azidose: niedrigerer pH‑Wert und weniger Bikarbonat, erhöhtes Chlorid, bei ansonsten stabilen nierenbezogenen Parametern wie Harnstoff und Hämatokrit. Obwohl die acidotischen Tiere mindestens so viel oder mehr fraßen und tranken wie die Kontrolltiere, hörten sie nach etwa zwei Monaten auf zuzunehmen. Detaillierte Messungen in Stoffwechselkäfigen zeigten, dass diese Mäuse insgesamt mehr Energie verbrannten, weniger Magermasse (muskelreich) hatten und relativ mehr Fett trugen — ein Hinweis auf höhere Stoffwechselkosten unter chronischer Azidose.
Bessere Blutzuckerregulation ohne zusätzliche Insulinwirkung
Das Team testete wiederholt, wie schnell die Mäuse Zucker aus dem Blut entfernten, indem sie Glukose injizierten und die Blutspiegel über die Zeit verfolgten. Bereits eine Woche nach Beginn des säurebildenden Trinkens senkten die behandelten Mäuse ihren Blutzucker schneller als die Kontrollen, und dieser Vorteil blieb an vielen Zeitpunkten bis zu 180 Tagen erhalten. Der nüchterne Blutzucker war in der acidotischen Gruppe durchgehend niedriger. Als die Forschenden jedoch Insulin im Blut während dieser Tests maßen, lagen die Werte in beiden Gruppen gleich. Separate Tests, in denen die Mäuse direkt Insulin erhielten, zeigten außerdem, dass die Gesamtsensitivität gegenüber Insulin unverändert blieb. Mit anderen Worten: Chronische Azidose verbesserte die Glukosetoleranz, ohne dass die Bauchspeicheldrüse mehr Insulin produzierte oder die Gewebe stärker darauf reagierten.
Verlagerung, wo und wie Zucker gebildet und verloren geht
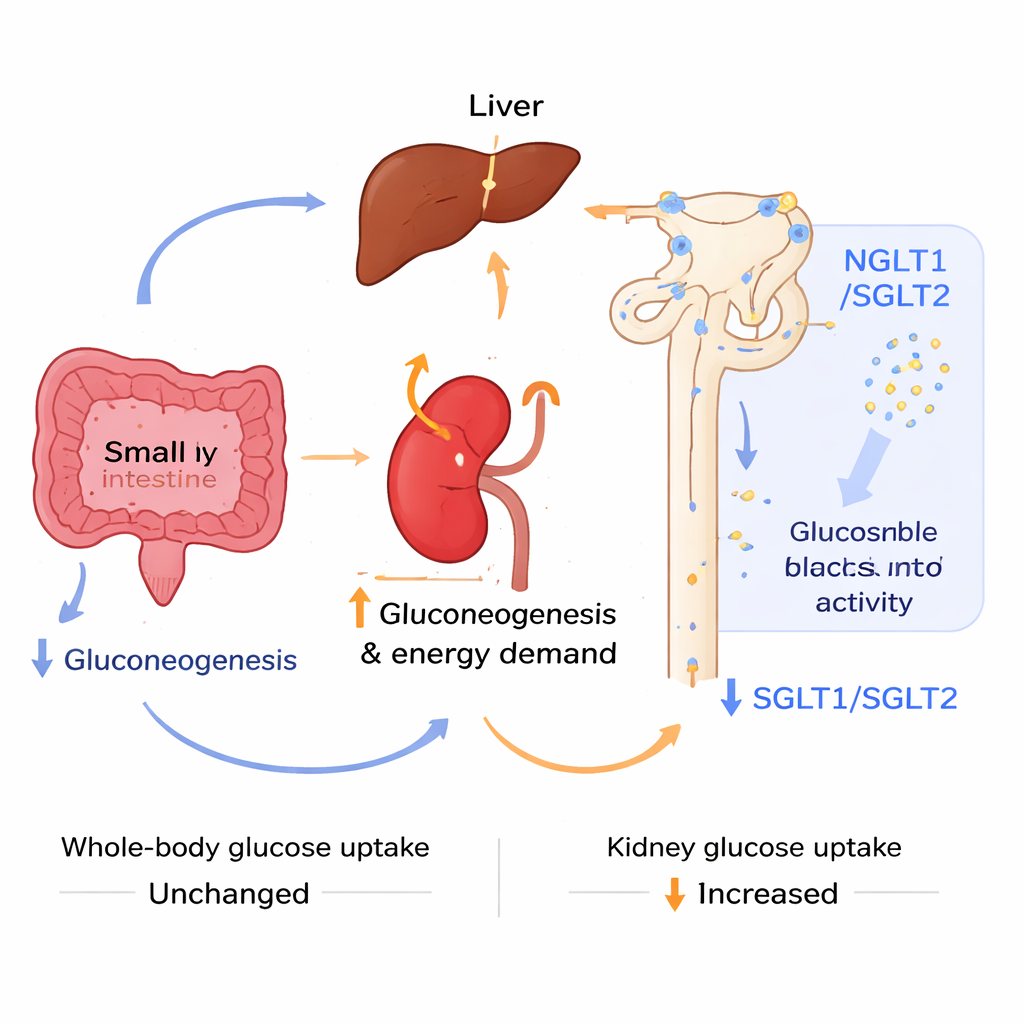
Um herauszufinden, woher die verbesserte Zuckerregulation stammte, untersuchten die Forschenden, wie verschiedene Organe Glukose produzieren. Sie verwendeten spezifische Substrate — Pyruvat, Alanin und Glutamin — die in der Leber, Niere und dem Darm in zuckerbildende Stoffwechselwege eingespeist werden. Im Verlauf der Zeit wurden die Leber und Teile des Darms der acidotischen Mäuse weniger aktiv in der Neuglukoneogenese, besonders aus Alanin und Glutamin. Im Gegensatz dazu zeigte die Niere Anzeichen erhöhter Aktivität: Schlüssengene, die an der Glukoseproduktion und Energieversorgung beteiligt sind, wurden hochreguliert, und Bildgebung mit einem radioaktiven Glukose‑Analogon zeigte eine erhöhte Zuckeraufnahme in Niere und Blase, obwohl die gesamte Körperaufnahme unverändert war. Gleichzeitig ging nach einer Zuckergabe mehr Glukose im Urin verloren, weil die wichtigsten Natrium‑Glukose‑Transporter der Niere, die normalerweise filtrierten Zucker zurückgewinnen, sowohl auf RNA‑ als auch auf Proteinebene herunterreguliert waren. Diese Kombination — weniger Zuckerproduktion in Leber und Darm, mehr Verbrauch und Ausscheidung durch die Niere — trug dazu bei, die Blutzuckerspiegel zu kontrollieren.
Tiefgreifende Veränderungen in Nierenzellen
Genexpressionsaufnahmen der Nieren in den ersten zwei Behandlungsmonaten zeigten eine umfassende Umgestaltung der zellulären Maschinerie. Signalwege, die am Transport geladener Teilchen (Anionen), an der Rückresorption von Bikarbonat sowie an der Mitochondrienfunktion und der oxidativen Phosphorylierung — den wichtigsten Energieerzeugern der Zelle — beteiligt sind, wurden verstärkt. Gene, die mit Zucker‑ und Fettstoffwechsel verbunden sind, wurden ebenfalls nach oben verschoben, während einige Immun‑ und Entgiftungswege, darunter Teile des Komplementsystems und der Cytochrom‑P450‑Familie, gedämpft waren. Diese Muster passen zu einer Niere, die härter arbeitet, um Säure auszuscheiden, mehr Energie verbraucht und gleichzeitig ihren Umgang mit Glukose und Lipiden umprogrammiert, um den erhöhten Energiebedarf zu decken.
Was das für Menschen mit Nieren‑ und Stoffwechselproblemen bedeutet
Zusammengefasst führte eine langfristige, milde metabolische Azidose bei Mäusen nicht zu einer Verschlechterung der Blutzuckerregulation — im Gegenteil, sie verbesserte diese — durch Verringerung der Zuckerproduktion in Leber und Darm, Reduktion der Glukoserückresorption in der Niere und Erhöhung des renal eigenen Energieverbrauchs. Insulin selbst spielte dabei keine größere Rolle als üblich. Das bedeutet nicht, dass Azidose gut ist oder dass Patientinnen und Patienten absichtlich acidotisch bleiben sollten; Azidose hat weiterhin viele schädliche Effekte. Aber die Ergebnisse zeigen, dass der Körper sich unerwartet anpassen kann, und heben die Niere als starken Regulator des Blutzuckers hervor. Künftige Arbeiten könnten versuchen, einige dieser nierenspezifischen Mechanismen — etwa erhöhte renale Glukoseverluste und veränderte Glukoseproduktion — zu nutzen, ohne Patienten den Risiken einer chronischen Azidose auszusetzen.
Zitation: Zaibi, N., Montaigne, J., Baraka-Vidot, J. et al. Chronic NH4Cl loading improves glucose tolerance without modifying insulin sensitivity in mice. Sci Rep 16, 7048 (2026). https://doi.org/10.1038/s41598-026-38007-7
Schlüsselwörter: metabolische Azidose, Glukosetoleranz, Nierenfunktion, Gluconeogenese, Risiko für Typ-2-Diabetes