Clear Sky Science · de
Funktionsverlust-Mutationen im Melanocortin-2-Rezeptor (mc2r) führen bei Knochenfischen zu Hauthyperpigmentierung
Warum Fischfärbung verborgene Biologie offenbaren kann
Von tropischen Riffen bis zum heimischen Aquarium tragen viele Fische kräftige Streifen und Punkte. Diese Farben sind nicht nur Schmuck; sie helfen Tieren, sich vor Fressfeinden zu verbergen, schützen die Haut vor Sonnenlicht und dienen der Kommunikation untereinander. Diese Studie nutzt den winzigen Zebrabärbling – berühmt für seine dunkel-goldenen Streifen – um aufzuklären, wie ein einziger Hormonrezeptor, der sonst vor allem die Stresshormone steuert, auch die Hautfarbe beeinflusst. Die Arbeit zeigt, dass bei Ausfall dieses Rezeptors Fische ungewöhnlich dunkel und gelblich werden, was eine unerwartete Verbindung zwischen dem Stresssystem und der Pigmentierung offenbart.
Ein Stresshormon-Schalter mit Nebenaufgabe
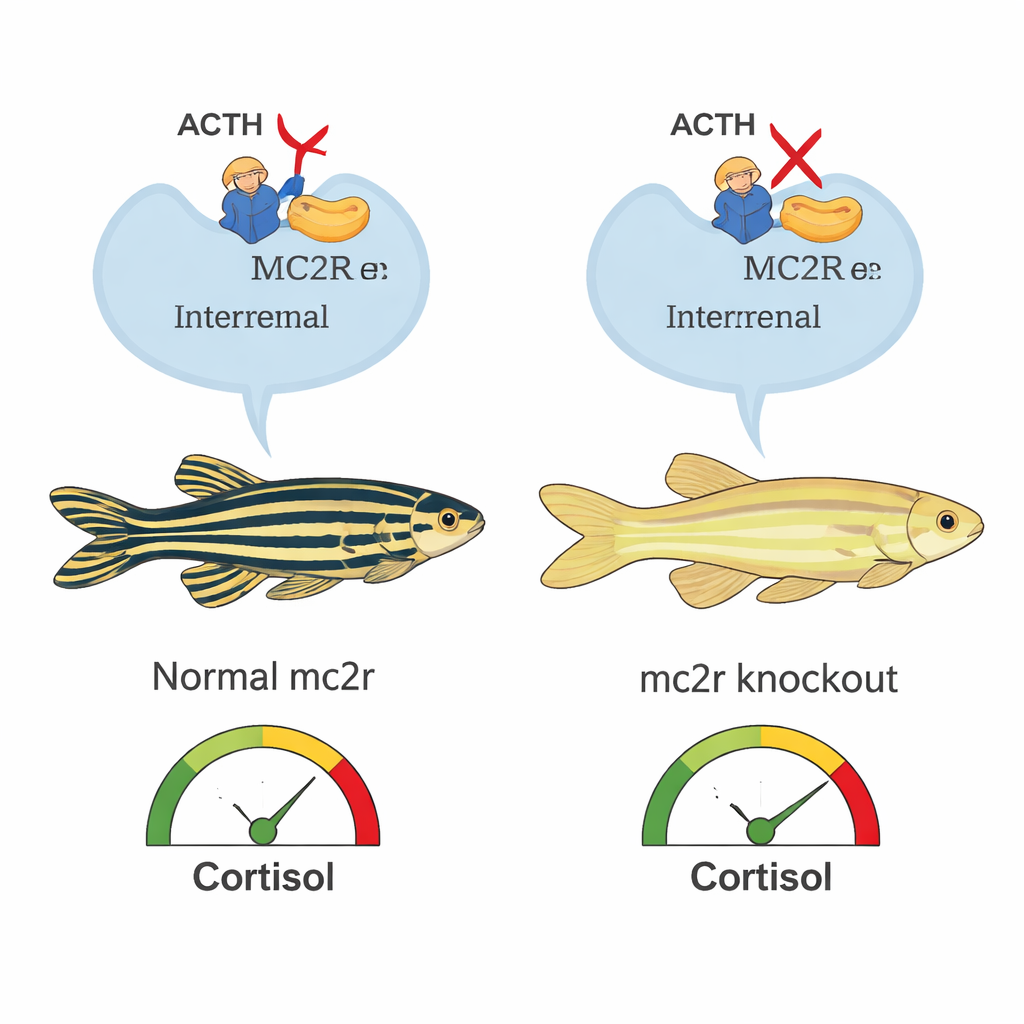
Bei Wirbeltieren hilft eine Hormongruppe, die Melanocortine genannt wird, sowohl die Hautfarbe als auch Stressreaktionen zu steuern. Diese Hormone wirken über mehrere eng verwandte Rezeptoren. Einer davon, MC2R, sitzt in einer neben den Nebennieren stehenden Drüse und wird durch das Hormon ACTH aktiviert, um die Produktion von Cortisol anzustoßen – dem wichtigsten Stresshormon bei Fischen und Menschen. Während andere Melanocortin-Rezeptoren dafür bekannt sind, die Pigmentierung zu beeinflussen, war die Rolle von MC2R für die Hautfarbe, insbesondere bei Fischen, bislang weniger klar. Die Autoren wollten testen, ob MC2R im Zebrabärbling mehr tut als nur die Stressantwort zu steuern.
Ein Gen editieren verändert die Farbintensität, nicht das Muster
Mit CRISPR/Cas9-Geneditierung erzeugte das Team Zebrabärblinge, bei denen das mc2r-Gen ausgeschaltet wurde und verkürzte, nicht funktionale Versionen des Rezeptors entstanden. Diese „Knockout“-Fische überlebten und behielten die vertraute Streifenanordnung aus dunklen und hellen Banden bei, doch ihr Erscheinungsbild veränderte sich deutlich. Im Vergleich zu normalen Geschwistern wirkten die Mutanten insgesamt intensiver gefärbt, mit stärkerem Gelbstich und dunklen Streifen, die in ein bläulich-grünes Farbspektrum verschoben waren. Dunkle Pigmentzellen (Melanophoren) tauchten an ungewöhnlichen Stellen auf, etwa rund um den Kiefer, und gelbe Pigmentzellen (Xanthophoren) wurden entlang der Bauchseite und in den hellen Bändern zwischen den Streifen häufiger. Sorgfältige Zellzählungen bestätigten, dass sowohl Melanophoren als auch Xanthophoren zahlreicher waren, obwohl das gesamte Streifenmuster erhalten blieb.
Eine Stressantwort, die ausfällt
Da MC2R normalerweise die Cortisolproduktion antreibt, prüften die Forschenden, wie die Knockout-Fische mit Stress umgehen. Unter ruhigen Bedingungen waren die Cortisolwerte bei normalen und mutierten Zebrabärblingen ähnlich. Nach einer akuten Stressbelastung jedoch zeigte die normale Fische einen starken Cortisolanstieg, während die Mutanten nur eine schwache Reaktion zeigten. Bei direkter Injektion von ACTH reagierten normale Fische erneut mit einem großen Cortisolanstieg, die Knockouts produzierten jedoch nur einen Bruchteil davon. Diese Experimente bestätigen, dass MC2R für eine volle Stresshormonantwort unerlässlich ist und dass die auffälligen Farbveränderungen neben einer beeinträchtigten Fähigkeit auftreten, unter Druck Cortisol zu bilden.
Farbveränderungen, die im Erbgut niedergelegt sind
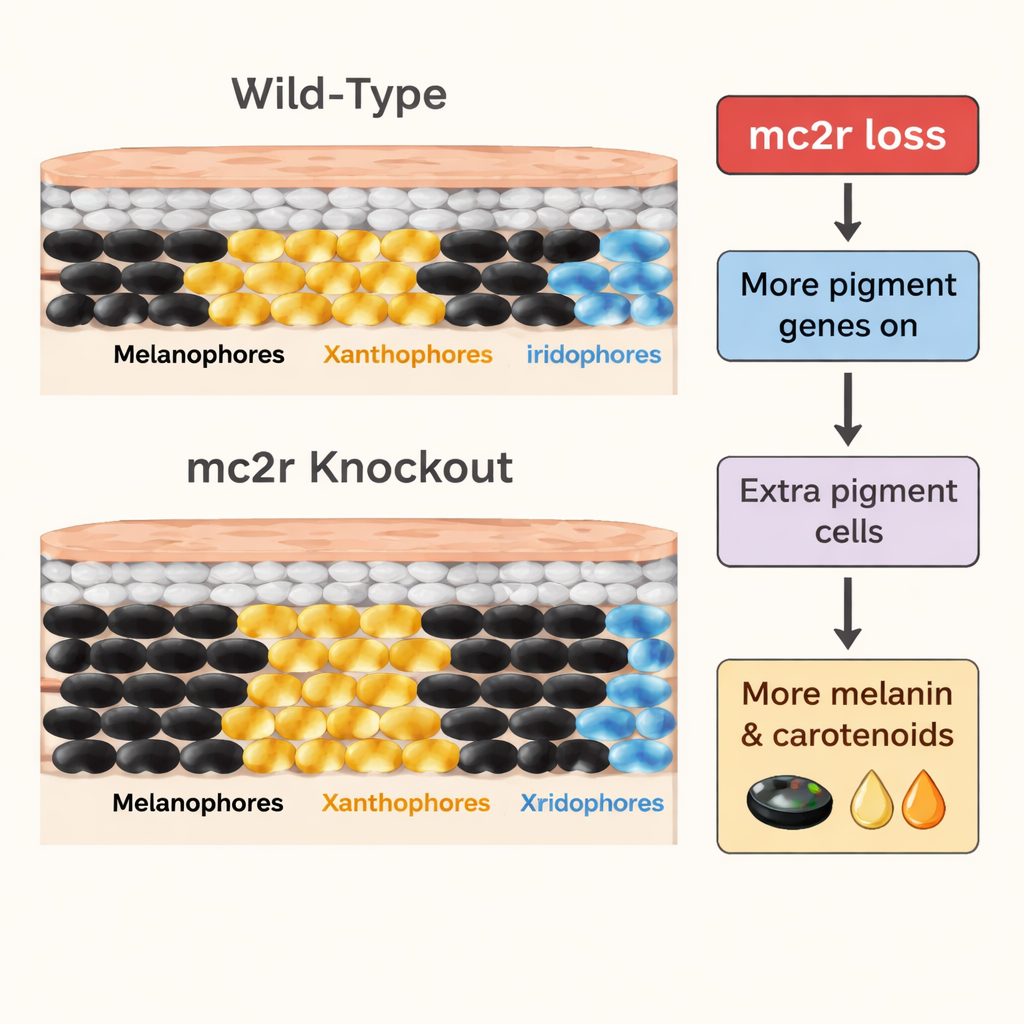
Um zu verstehen, wie ein defekter Stressrezeptor die Färbung umformen kann, untersuchte das Team, welche Gene in der Haut ein- oder ausgeschaltet sind. Sie sequenzierten RNA aus der Haut normaler und mutierter Fische und verglichen die Aktivität Tausender Gene. Bei den Mutanten fanden sie eine erhöhte Aktivität von Genen, die am Aufbau von Pigmentgranula und an der Bildung des dunklen Pigments Melanin beteiligt sind, sowie von Genen, die mit gelber Carotinoidspeicherung und Lipid(fett)-Stoffwechsel verknüpft sind. Durch die Kombination dieser Bulk-Messungen mit Einzelzell-Daten aus spezifischen Pigmentzellen zeigten sie, dass Schlüsselgene der Melanophoren und Xanthophoren in den Knockouts aktiver waren. Interessanterweise waren Gene, die die Organisation des Streifenmusters unterstützen, insbesondere solche, die mit reflektierenden Iridophoren verknüpft sind, nicht maßgeblich verändert. Das deutet darauf hin, dass MC2R vor allem beeinflusst, wie viele Pigmentzellen sich entwickeln und wie viel Pigment sie speichern, statt die Blaupause, die die Platzierung der Streifen auf dem Körper bestimmt.
Was das für Farbe, Stress und darüber hinaus bedeutet
Die Studie zeigt, dass MC2R beim Zebrabärbling eine doppelte Rolle spielt: Er ist entscheidend für die Produktion von Stresshormonen bei plötzlichen Herausforderungen und hilft zugleich, das Gleichgewicht von Pigmentzellzahlen und Pigmentproduktion zu wahren. Wenn mc2r verloren geht, bilden Fische weiterhin normale Streifen, sammeln aber mehr dunkle und gelbe Zellen an und speichern mehr Pigmente, was zu einem deutlich hyperpigmentierten, gelblichen Aussehen führt. Für den Laien ist die Botschaft klar: Ein Gen, das lange als Stressschalter galt, wirkt auch als Farbregler. Diese Erkenntnis könnte helfen, bestimmte menschliche Pigmentstörungen mit Nebennierenproblemen zu erklären, und illustriert, wie eng unsere Hormonsysteme und sichtbare Merkmale miteinander verwoben sind.
Zitation: Barreiro-Docío, E., Guerrero-Peña, L., Soni, P. et al. Loss-of-function mutations in the melanocortin-2-receptor (mc2r) lead to skin hyperpigmentation in teleost fish. Sci Rep 16, 7261 (2026). https://doi.org/10.1038/s41598-026-37998-7
Schlüsselwörter: Zebrabärbling Pigmentierung, Stresshormone, Melanocortin-Rezeptor, Cortisol, Fischfärbung