Clear Sky Science · de
Synergistisches kombinatorisches Antikrebs-Potenzial von Tamoxifen mit Naringin und Diosmetin in MCF-7-Brustkrebszellen und deren liposomale Verabreichung
Warum die Kombination eines gängigen Medikaments mit Zitrus-Verbindungen wichtig ist
Brustkrebs wird häufig mit Tamoxifen behandelt, einer hormonblockierenden Tablette, die viele Leben gerettet hat. Mit der Zeit entwickeln manche Tumoren jedoch Resistenzen gegen das Medikament, und die Nebenwirkungen der Behandlung können belastend sein. Diese Studie untersucht eine reizvolle Idee: Kann man Tamoxifen wirksamer machen und möglicherweise in geringeren Dosen einsetzen, indem man es mit natürlichen Substanzen aus Zitrusfrüchten kombiniert und sie zusammen in winzige fettbasierte Bläschen, sogenannte Liposomen, verpackt, damit sie Krebszellen gezielter erreichen?
Zitrus-Helfer für ein etabliertes Krebsmedikament
Die Forschenden konzentrierten sich auf zwei Pflanzenstoffe, Naringin und Diosmetin, Flavonoide, die häufig in Grapefruits, Orangen und anderen Zitrusfrüchten vorkommen. In Laboruntersuchungen an östrogenempfindlichen Brustkrebszellen (MCF-7) und einer weiteren Brustkrebszelllinie (T47D) bestimmten sie zunächst, wie stark jede Verbindung allein das Zellwachstum hemmen oder Zellen abtöten kann. Tamoxifen war am potentesten, aber auch Naringin und Diosmetin verringerten die Überlebensrate der Krebszellen, insbesondere in MCF-7-Zellen, was darauf hindeutet, dass diese natürlichen Moleküle selbst ein antitumorales Potenzial besitzen. Das bildete die Grundlage, um zu prüfen, ob die Kombination mit Tamoxifen mehr ergibt als die Summe der Einzelwirkungen.
Stärker zusammen: Tests von Wirkstoffkombinationen
Um zu verstehen, wie die Wirkstoffe zusammenwirken, behandelte das Team Brustkrebszellen mit Tamoxifen plus Naringin, Tamoxifen plus Diosmetin oder allen drei zusammen in verschiedenen festen Verhältniskombinationen. Mit einem standardisierten mathematischen Ansatz für Wirkstoffpaare zeigten sie, dass mehrere Kombinationen synergistisch waren – das heißt, das Gemisch tötete mehr Krebszellen als aufgrund der Einzelwirkungen zu erwarten wäre. Ein Verhältnis mit etwa doppelt so viel Flavonoid wie Tamoxifen (1:2) war besonders wirksam, vor allem für Tamoxifen plus Naringin. Unter diesen Bedingungen konnte derselbe krebshemmende Effekt mit geringeren Tamoxifenmengen erreicht werden, ein wichtiger Vorteil, falls sich dies in weniger Nebenwirkungen für Patientinnen und Patienten übersetzt.
Auslösen der Selbstzerstörung der Krebszellen
Als Nächstes untersuchten die Forschenden, was sich innerhalb der Krebszellen abspielt. Sie betrachteten oxidativen Stress – eine Anhäufung reaktiver Sauerstoffspezies – und Anzeichen für programmierter Zelltod, die Apoptose. Die Kombinationen, insbesondere die Dreiermischung aus Tamoxifen, Naringin und Diosmetin, führten zu erhöhtem oxidativem Stress und stärker ausgeprägten Apoptose-Merkmalen als Tamoxifen allein. Unter dem Mikroskop zeigten mehr Zellen das geschrumpfte, intensiv gefärbte Erscheinungsbild, das für spätstadialen Zelltod typisch ist. Proteinanalysen bestätigten dies: Die Kombinationen senkten die Spiegel von Bcl-2 und Bcl-xL, Proteinen, die Krebszellen normalerweise gegen den Tod schützen, und erhöhten aktiviertes Caspase-3, einen zentralen Ausführer der Apoptose. Einfach gesagt halfen die Zitrusverbindungen offenbar, Tamoxifen-behandelte Zellen über die Schwelle zur Selbstzerstörung zu treiben.
Verpackung der Wirkstoffe in winzige Träger
Obwohl die Kombinationen vielversprechend wirkten, sind Naringin und Diosmetin schlecht wasserlöslich und können nur schlecht resorbiert werden. Um dem zu begegnen, entwickelten die Forschenden Liposomen – Nanometer-große Kugeln aus natürlichen Fetten –, die Tamoxifen und die Flavonoide gemeinsam transportieren konnten. Sie optimierten die Lipidzusammensetzung und den Herstellungsprozess so, dass die resultierenden Partikel etwa 150–210 Nanometer groß, relativ gleichförmig und mit einer Oberflächenladung versehen waren, die zur Stabilität in Suspension beiträgt. Die Bildgebung bestätigte, dass die Liposomen glatt und annähernd kugelförmig waren. Tests zeigten, dass ein hoher Anteil jedes Wirkstoffs eingekapselt werden konnte und dass die Freisetzung in eine umgebende Flüssigkeit über 24 Stunden langsam erfolgte, entsprechend diffusionsgetriebenen Kinetiken. Diese Art kontrollierter Freisetzung ist wünschenswert, weil sie länger anhaltende, gleichmäßigere Wirkstoffspiegel ermöglichen kann.
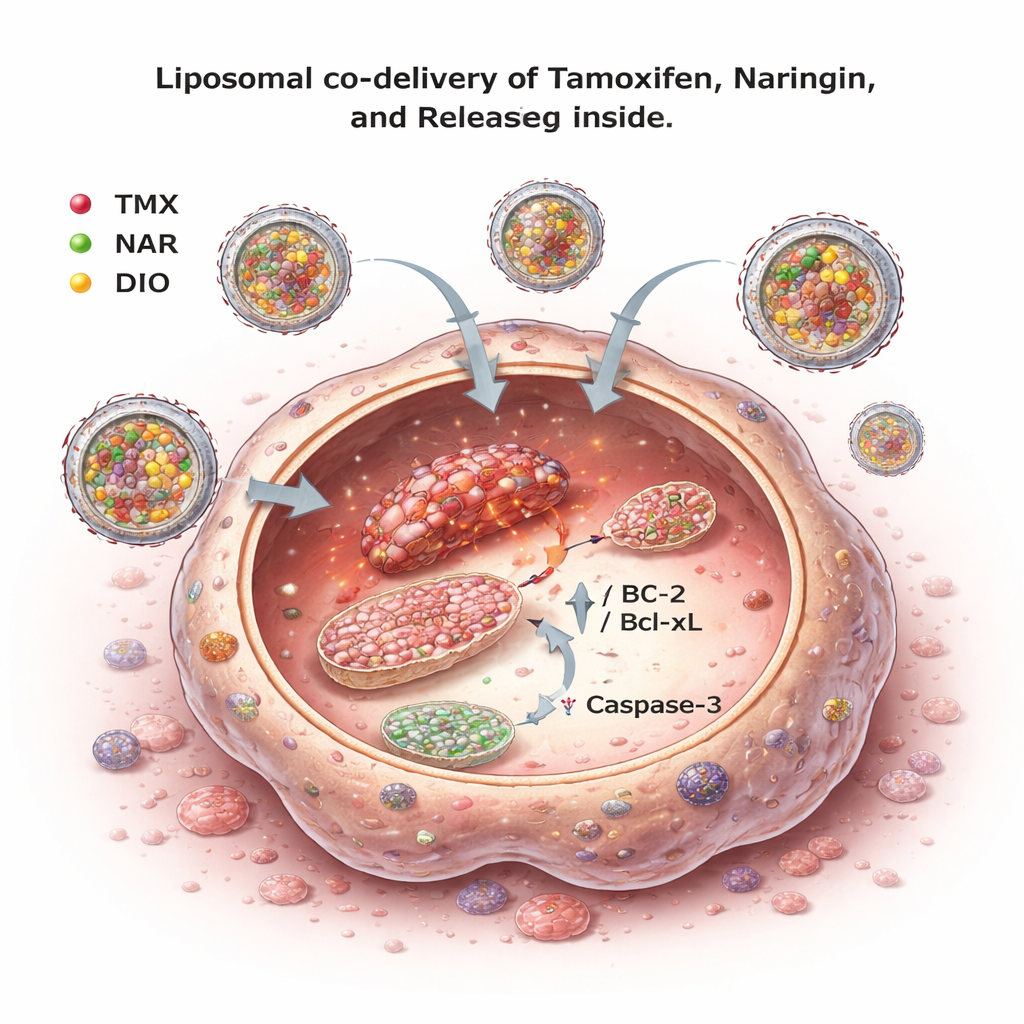
Tumoren stärker treffen und gesunde Zellen schonen
Wurden diese liposomalen Formulierungen erneut an Brustkrebszellen getestet, waren die Liposomen mit allen drei Wirkstoffen (Tamoxifen, Naringin und Diosmetin) effektiver darin, die Überlebensfähigkeit der Krebszellen zu reduzieren, als Liposomen, die nur Tamoxifen oder nur zwei der Wirkstoffe enthielten. Wichtig ist, dass bei Anwendung derselben Formulierungen auf eine nicht-krebsartige menschliche Zelllinie innerhalb des getesteten Dosisbereichs kaum Toxizität auftrat, was auf eine gewisse Selektivität gegenüber Krebszellen hindeutet. Insgesamt deuten die Ergebnisse darauf hin, dass die Kombination von Tamoxifen mit zitrus-abgeleiteten Flavonoiden und deren liposomale Verabreichung das Abtöten von Krebszellen verstärken kann, während gleichzeitig niedrigere und potenziell sicherere Tamoxifendosen möglich werden.
Was das für die zukünftige Brustkrebsbehandlung bedeuten könnte
Für Laien lautet die Kernaussage: Die Kombination eines etablierten Brustkrebsmedikaments mit gut ausgewählten natürlichen Verbindungen und deren Bündelung in intelligente Nano-Träger könnte die Behandlung wirkungsvoller und möglicherweise verträglicher machen. Die Studie zeigt in Zellkulturen, dass Tamoxifen in Kombination mit Naringin und Diosmetin besser wirkt: Sie helfen, Krebszellen vom Überlebensmodus in den Selbstzerstörungsmodus zu schalten, und tun dies besonders effizient bei gemeinsamer Verabreichung in Liposomen. Da diese Arbeit sich jedoch noch im Laborstadium befindet, sind Tierversuche und schließlich klinische Studien nötig, um die Befunde zu bestätigen. Dennoch skizziert sie eine vielversprechende Strategie: Kombinationstherapie plus Nanotechnologie, um resistente Brusttumoren auszumanövrieren und langfristig bessere Ergebnisse zu erzielen.
Zitation: Uniyal, P., Das Pramanik, S., Pandey, S. et al. Synergistic combinatorial anticancer potential of Tamoxifen with Naringin and Diosmetin in MCF-7 breast cancer cells and their liposomal delivery. Sci Rep 16, 7646 (2026). https://doi.org/10.1038/s41598-026-37954-5
Schlüsselwörter: Brustkrebs, Tamoxifen, Flavonoide, liposomale Verabreichung, Kombinationstherapie