Clear Sky Science · de
Erzeugung von TCRγδ + T-Zellen aus humanen embryonalen Stammzellen
Neue Wege, das Immunsystem zu bewaffnen
Krebsbehandlungen nutzen zunehmend das körpereigene Immunsystem, um Tumoren aufzuspüren. Eine besonders vielversprechende Zellart, sogenannte Gamma-Delta-T-Zellen, kann Krebszellen töten, ohne den genauen Gewebetyp des Patienten erkennen zu müssen — was sie zu einem starken Kandidaten für „von der Stange“-Therapien macht. Diese Zellen sind jedoch im erwachsenen Blut selten, und sie in großer Zahl zu vermehren ist schwierig. Diese Studie beschreibt eine Methode, Gamma-Delta-T-Zellen im Labor aus humanen embryonalen Stammzellen zu züchten, was möglicherweise den Weg zu zugänglicheren Krebsimmuntherapien öffnet.
Blanko‑Zellen in Krebsbekämpfer verwandeln
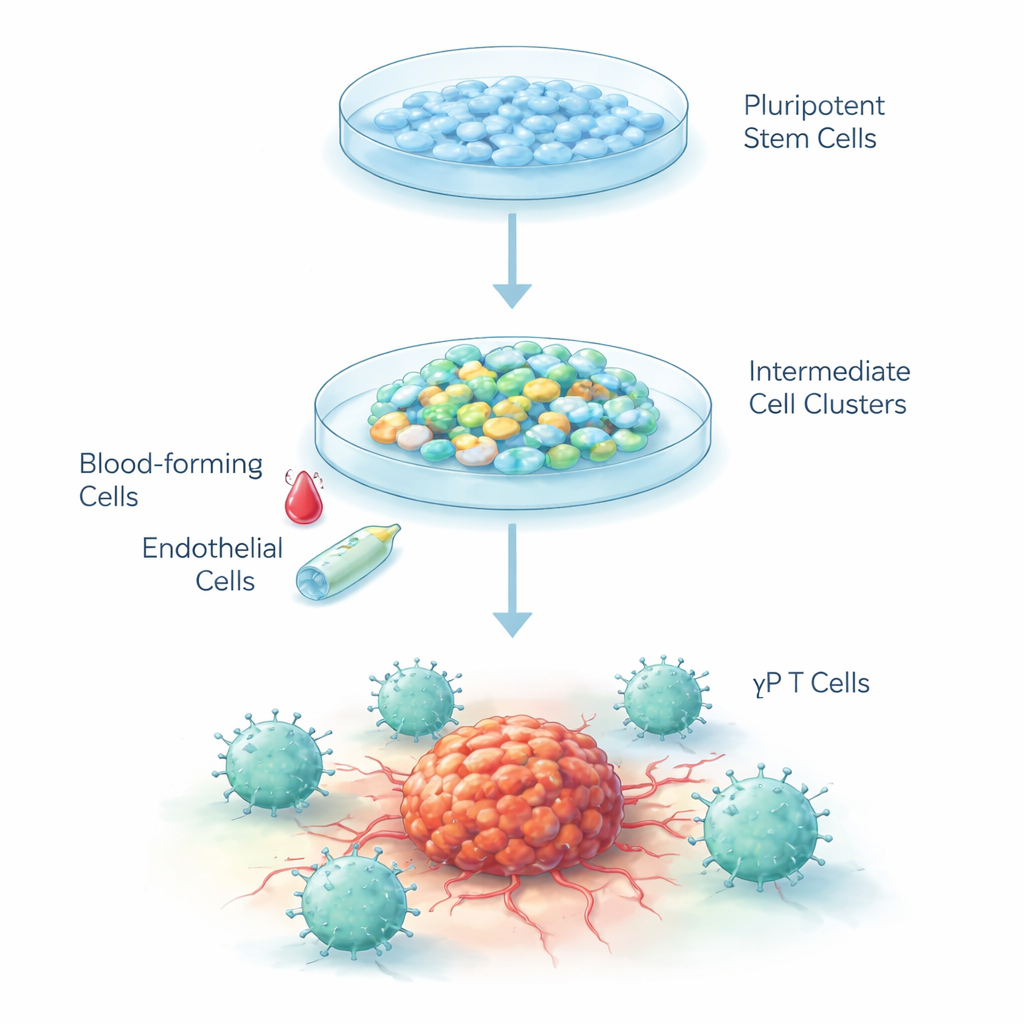
Humane embryonale Stammzellen sind „Blanko“-Zellen, die prinzipiell fast jedes Gewebe des Körpers werden können. Die Forschenden entwickelten ein schrittweises Rezept, um diese Zellen entlang des gleichen Entwicklungspfads zu lenken, den sie im Embryo durchlaufen, wenn Blut- und Immunsystem sich bilden. Sie verwendeten einen dreistufigen Prozess: zunächst die Stammzellen zu frühen gefäßähnlichen Zellen leiten, dann in unreife blutbildende Zellen und schließlich in T‑Zellen des Gamma-Delta-Typs. Die Zellen wurden als dreidimensionale Cluster in speziellen Flüssigkulturen unter niederen Sauerstoffbedingungen gezüchtet, die das sich entwickelnde Embryo nachahmen, und während der Reifung wieder auf normale Sauerstoffwerte zurückgeführt.
Die Immunzell-Fertigungslinie aufbauen
In der ersten Phase lenkten chemische Signale die Stammzellen in Richtung Mesoderm, der frühen Schicht, aus der Blut und Gefäße entstehen. Innerhalb von sechs Tagen zeigten fast 40 % der Zellen in jedem Cluster Marker von „hämatopoetischen Endothelzellen“, einer Übergangszellart, die Blut hervorbringen kann. In der zweiten Phase lösten veränderte Wachstumsfaktoren bei diesen endothelähnlichen Zellen einen Umschaltvorgang hin zu freischwimmenden Blutvorläuferzellen aus. Über 99 % dieser schwimmenden Zellen trugen einen wichtigen frühen Blutmarker, und etwa 90 % exprimierten einen weiteren Blutzellmarker, was auf eine bemerkenswert reine Population mit starkem Potenzial für den weiteren Weg in Richtung Immunzellen hinweist.
Ankunft bei Gamma-Delta-T-Zellen
Für die Abschlussphase versorgte das Team die Zellen mit Signalen, die die T‑Zell-Entwicklung fördern, darunter ein Notch-aktivierendes Protein, das Hinweise im Thymus imitiert. Nach 25 Tagen waren mehr als 40 % der Zellen zu Gamma-Delta-T-Zellen gereift, erkennbar an ihren charakteristischen Oberflächenrezeptoren und einem „Double‑Negative“-Profil (fehlende CD4‑ und CD8‑Marker, die bei den meisten anderen T‑Zellen üblich sind). Wichtig ist, dass nur sehr wenige konventionelle Alpha‑Beta-T-Zellen produziert wurden, was zeigt, dass das Protokoll die Gamma-Delta‑Linie deutlich bevorzugt. Genetische Analysen im Zeitverlauf zeigten, dass die Zellen Gruppen von Genen in einer geordneten Abfolge ein- und ausschalteten, die der Bildung von Blut und T‑Zellen im Körper eng entspricht.
Laborgezüchtete Zellen auf die Probe gestellt
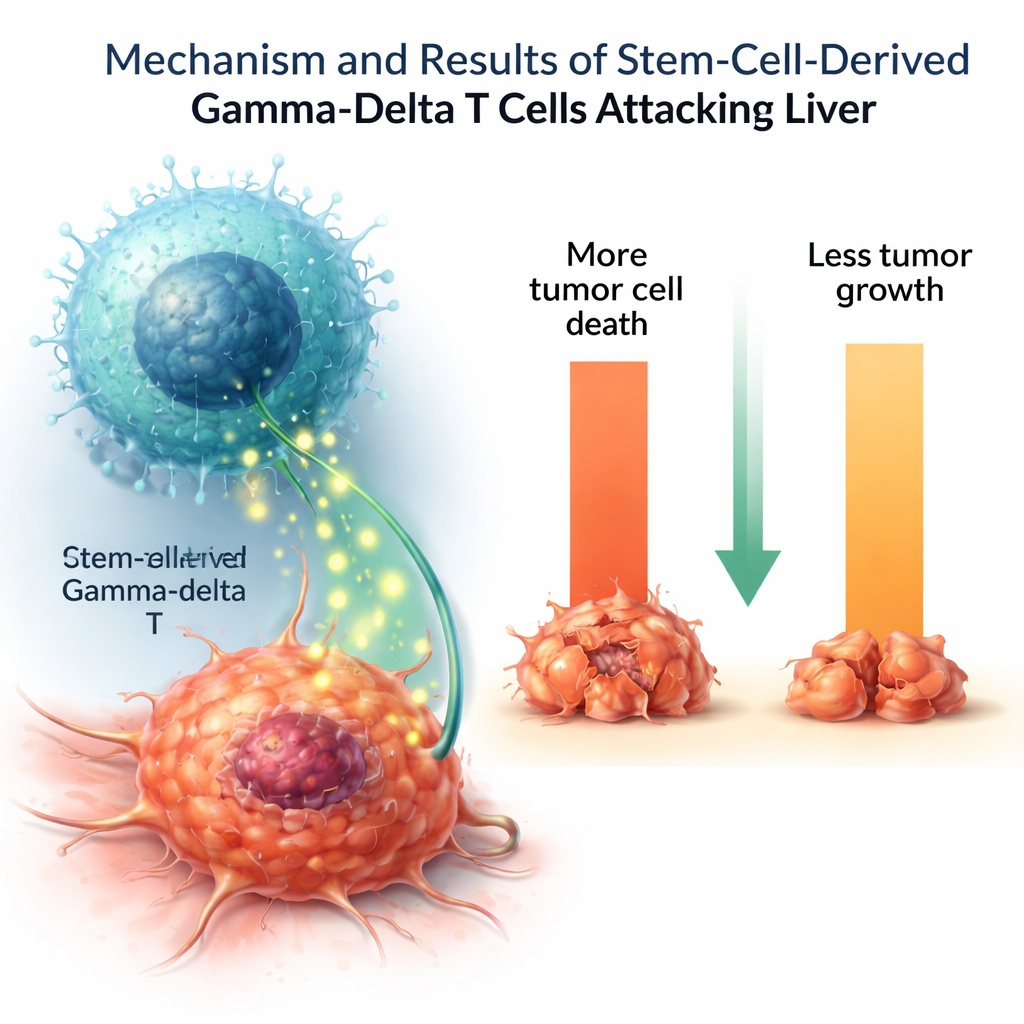
Um zu prüfen, ob diese im Labor gefertigten Zellen als echte Krebsbekämpfer funktionieren, setzten die Forschenden sie mehreren humanen Tumorzelllinien aus. Die Gamma-Delta-T-Zellen töteten einen beträchtlichen Anteil von Leberkrebszellen und verlangsamten ihr Wachstum, während sie gesunde Kontrollzellen kaum beeinflussten. Bei Stimulation schütteten sie wichtige Immunbotenmoleküle wie Tumornekrosefaktor und Interleukin‑2 aus, die helfen, Immunantworten zu koordinieren und zu verstärken. Einige weitere zytotoxische Moleküle lagen jedoch in niedrigeren Konzentrationen als bei natürlichen Gamma-Delta-T-Zellen, was darauf hindeutet, dass die laborgezüchteten Zellen möglicherweise nicht vollständig ausgereift sind oder eine bestimmte funktionelle Untergruppe darstellen.
Was das für die künftige Krebsbehandlung bedeuten könnte
Indem sie eine vereinfachte Version der frühen Blutentwicklung in einer Schale nachstellten — ohne tierische Fütterzellen zu verwenden — erzeugten die Wissenschaftler binnen weniger als eines Monats große Mengen an Gamma-Delta-T-Zellen, schneller und einfacher als frühere Methoden. Zwar sind noch weitere Arbeiten nötig, um die endgültige Zellmischung zu reinigen, die Produktion zu skalieren und das Protokoll an klinisch zugelassene, serumfreie Bedingungen anzupassen, doch dieser Ansatz weist auf eine nachhaltige Quelle standardisierter Gamma-Delta-T-Zellen hin. Wenn sich diese Zellen in weiteren Tests als sicher und wirksam erweisen, könnten sie ein weithin verfügbares Bauelement für die nächste Generation von „von der Stange“-Immuntherapien gegen Krebsarten wie Lebertumoren werden.
Zitation: Zhang, X., Chen, C., Fu, Y. et al. Generation of TCRγδ + T cells from human embryonic stem cells. Sci Rep 16, 6762 (2026). https://doi.org/10.1038/s41598-026-37941-w
Schlüsselwörter: Gamma-Delta-T-Zellen, Krebsimmuntherapie, humane embryonale Stammzellen, Zelldifferenzierung, Leberkrebs