Clear Sky Science · de
Computergestützte Identifizierung und mechanistische Charakterisierung von Naturstoff-Bindern, die die prenylbindende Tunnelstruktur von PDE6D anvisieren
Den bevorzugten Schalter des Krebses gegen sich selbst wenden
Viele der tödlichsten Krebserkrankungen – von Bauchspeicheldrüse über Dickdarm bis zu Lungenkrebs – hängen von einem einzigen molekularen „An“-Schalter namens RAS ab. Wenn dieser Schalter dauerhaft auf EIN gestellt ist, wachsen Zellen unkontrolliert. Medikamentenentwickler kämpfen seit Jahrzehnten damit, RAS direkt abzuschalten. Diese Studie verfolgt einen anderen Ansatz: Sie sucht nach natürlichen Verbindungen, die still und leise das Helferprotein blockieren können, das RAS benötigt, um an seinen Wirkort zu gelangen, und so sein Signal abschwächen könnten, ohne RAS direkt anzugreifen. 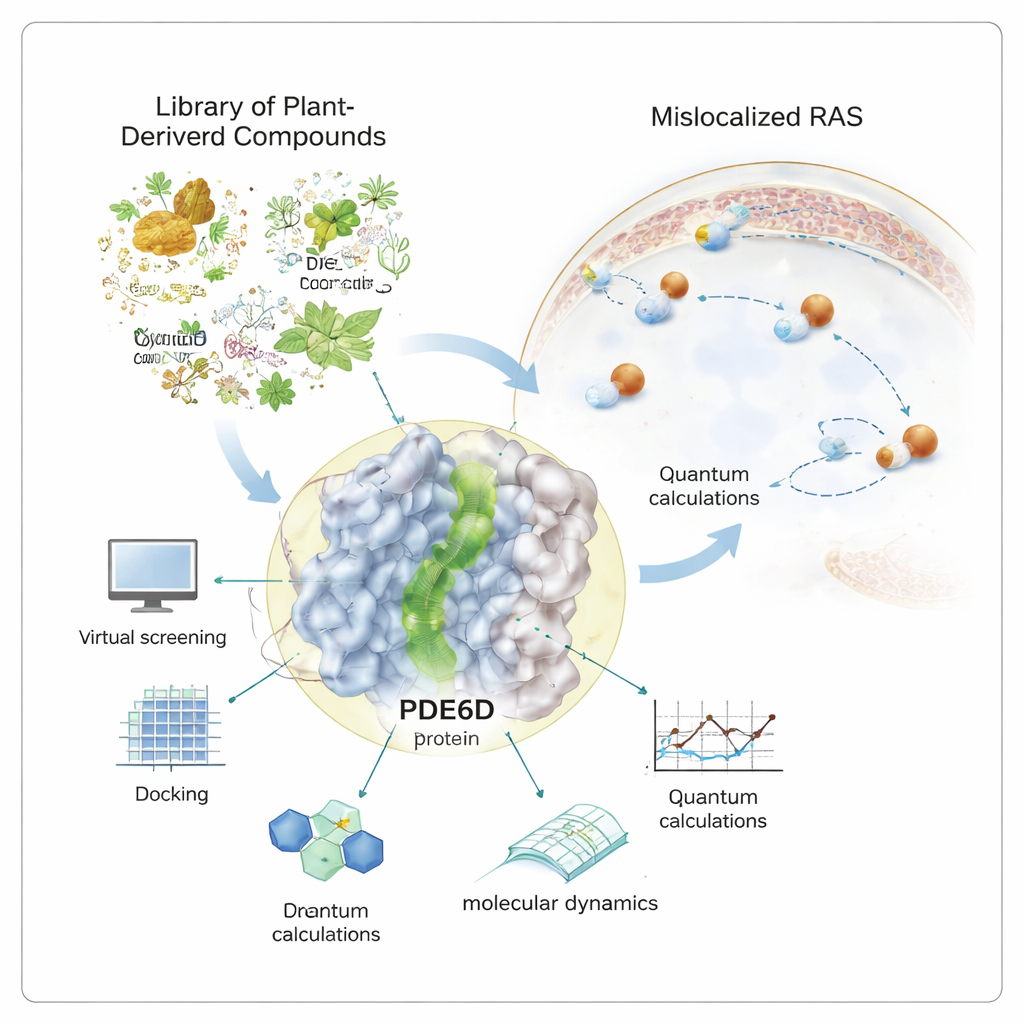
Ein verborgenes Helferprotein in Krebszellen
RAS-Proteine müssen an der inneren Zellmembran sitzen, um Wachstumssignale zu senden. Dafür besitzen sie einen fettigen Schwanz, der ihnen ermöglicht, in der Membran zu verankern. Ein Chaperon-Protein namens PDE6D fungiert wie ein Taxi und schützt diesen Schwanz, während RAS durch das wässrige Zellinnere transportiert wird. PDE6D verfügt über einen schmalen, ölausgekleideten Tunnel, der den RAS-Schwanz umschließt. Wird dieser Tunnel verstopft, landet RAS häufiger am falschen Ort und verliert dadurch an Wirksamkeit bei der Tumorförderung. Da viele vorhandene RAS-Medikamente nur für eine kleine Untergruppe von Mutationen wirksam sind, ist die Erforschung von PDE6D als indirektem, aber breiter anwendbarem Ziel von großem Interesse.
Computerbasiertes Durchsuchen von Natures chemischer Bibliothek
Anstatt sich ausschließlich auf synthetische Chemikalien zu stützen, griff die Autorin auf eine kuratierte Bibliothek von über tausend käuflichen Naturstoffen zurück – Moleküle, die ursprünglich aus Pflanzen, Mikroben und anderen lebenden Quellen stammen. Leistungsfähige Computerwerkzeuge wurden eingesetzt, um diese Bibliothek gegen die 3D-Struktur von PDE6D zu screenen. In diesem virtuellen Test wurde jedes Molekül in den Tunnel „gedockt“, um zu prüfen, wie eng und vorteilhaft es binden könnte. Die bestbewerteten Kandidaten wurden anschließend mit quantenmechanischen Berechnungen genauer untersucht, die die Elektronenverteilung in jedem Molekül und deren Fähigkeit beleuchten, stabilisierende Wechselwirkungen in der Protein-Tasche einzugehen.
Belastungstest vielversprechender Kandidaten in Bewegung
Proteine und kleine Moleküle ruhen nicht still in Zellen, daher ging die Studie über statische Schnappschüsse hinaus. Mithilfe langer Molekulardynamik-Simulationen, die atomare Bewegungen über eine halbe Mikrosekunde verfolgen, beobachtete die Forscherin, wie sich jedes vielversprechende Naturstoffmolekül im Laufe der Zeit im PDE6D-Tunnel verhielt. Zwei Kandidaten, bezeichnet als MolPort-039-052-621 und MolPort-002-507-186, blieben mit stabilen Kontaktnetzwerken im Tunnel verankert, während ein drittes Molekül in Richtung Tunneleingang driftete und weniger fest gebunden war. Weitere Analysen zeigten, welche Teile der PDE6D-Struktur sich beim Binden stärker bewegten oder beruhigten und wie der Komplex seine „Energielandschaft“ erkundete – im Grunde, welche Konformationen am günstigsten und langlebigsten waren. 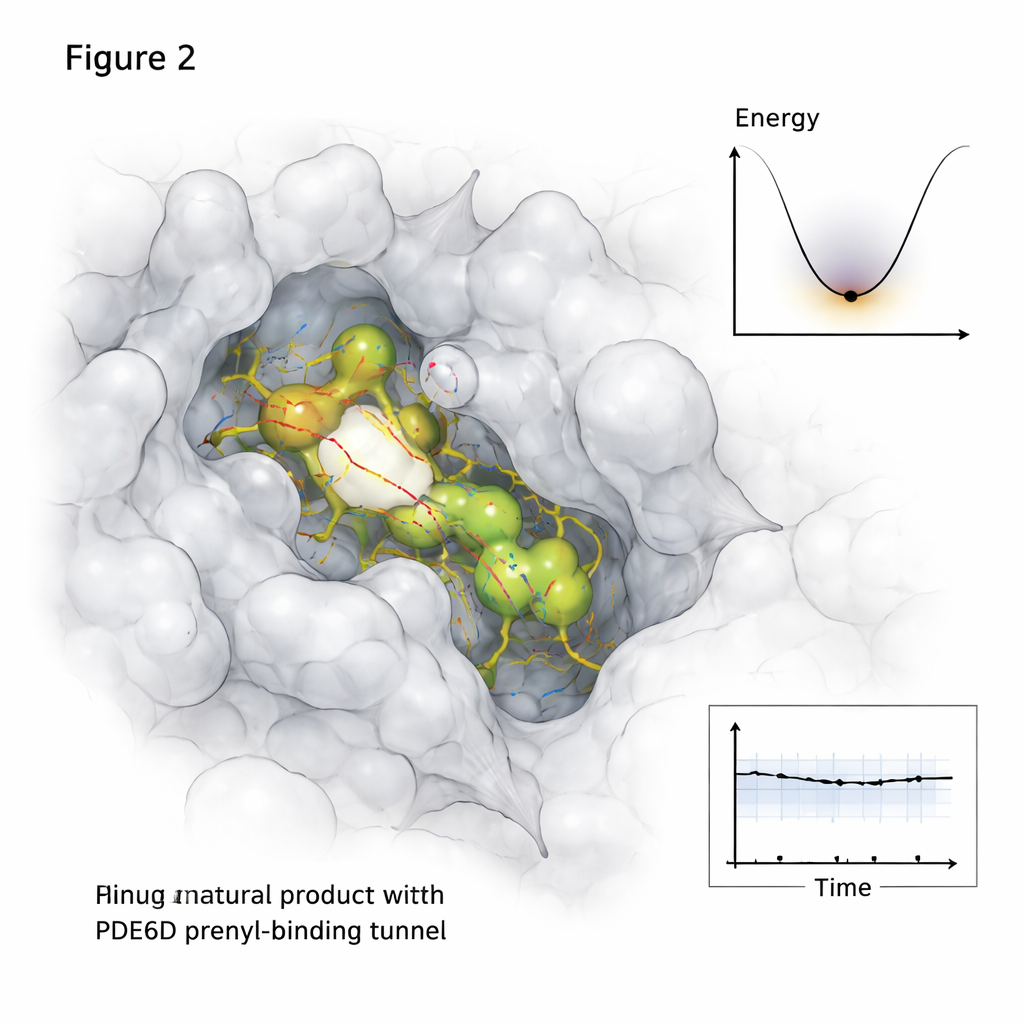
Das Gleichgewicht zwischen Bindungsstärke und arzneimittelähnlichem Verhalten
Die Studie nutzte zudem Online-Vorhersagewerkzeuge, um zu prüfen, ob diese Naturstoffe realistische Ausgangspunkte für Medikamente darstellen. Alle drei Spitzenkandidaten zeigten chemische Merkmale, die mit grundlegender „Drug-Likeness“ vereinbar sind, wiesen jedoch jeweils Warnhinweise auf. Einige wurden hinsichtlich Aufnahme oder Löslichkeit als eher schlecht vorhergesagt; andere zeigten Anzeichen möglicher Toxizität, etwa Effekte auf den Herzrhythmus oder die DNA. Diese Probleme bedeuten, dass die Moleküle in ihrer aktuellen Form kaum fertige Medikamente sind. Vielmehr sollten sie als strukturelle Vorlagen betrachtet werden, die Chemiker modifizieren könnten, indem sie die tunnelfüllenden Eigenschaften erhalten und problematische Bereiche abschneiden.
Was das für zukünftige Krebstherapien bedeutet
Vereinfacht gesagt liefert diese Arbeit kein neues Krebsmedikament, aber sie weist einen vielversprechenden Weg. Durch die Kombination mehrerer Rechenschichten – von schnellem Docking über detaillierte Simulationen bis hin zu Quantenberechnungen – schränkt die Studie eine riesige Menge natürlicher Moleküle auf eine kleine Gruppe ein, die offenbar gut dazu geeignet ist, den PDE6D-Tunnel zu verstopfen. Bestätigen zukünftige Laborexperimente, dass diese Verbindungen RAS tatsächlich in Zellen fehlleiten und das Wachstum RAS-getriebener Tumoren verlangsamen, könnten sie eine neue Klasse von Therapien inspirieren, die die „Logistik“ des Krebses angreifen, statt seinen Haupttreiber direkt zu bekämpfen.
Zitation: Alshahrani, M.M. Computational identification and mechanistic characterization of natural product binders targeting the PDE6D prenyl binding tunnel. Sci Rep 16, 6571 (2026). https://doi.org/10.1038/s41598-026-37939-4
Schlüsselwörter: RAS-Signalübertragung, PDE6D-Inhibitoren, Naturstoffe, computergestützte Wirkstoffforschung, Krebstherapie