Clear Sky Science · de
Ganzzellmodellierung sagt alternative Proteom-Allokationsstrategien im Archaeon Methanococcus maripaludis voraus
Warum winzige Methanproduzenten wichtig sind
Methanococcus maripaludis ist ein mikroskopisches Archaeon, das einfache Verbindungen wie Kohlendioxid und Format in Methan umwandelt — einen Hauptbestandteil von Erdgas. Zu verstehen, wie dieses Mikroorganismus seine internen Ressourcen, insbesondere seine Proteine, einteilt, kann allgemeine Regeln des Lebens unter Energieknappheit offenlegen und dabei helfen, es entweder als biologische Methanfabrik oder als Plattform für grüne Chemie nutzbar zu machen.
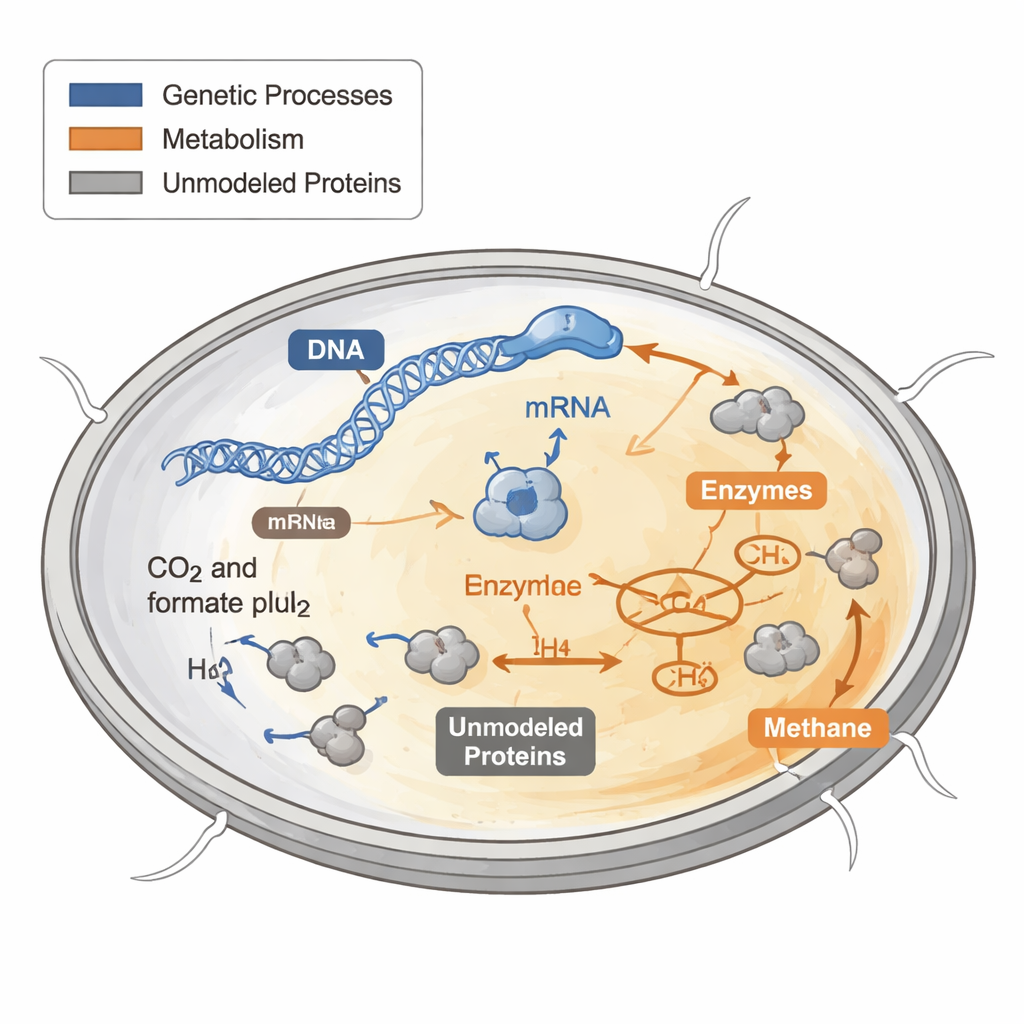
Wie Zellen ihr Proteinbudget ausgeben
Jede Zelle muss entscheiden, wie sie ihr begrenztes Protein-„Budget“ verwendet. Manche Proteine bauen neue Zellbestandteile, andere gewinnen Energie, und wieder andere erfüllen Hausaufgaben-Funktionen. Frühere Computermodelle des Stoffwechsels behandelten diese Proteine, als wären sie frei und unbegrenzt verfügbar, was bei Vorhersagen des Wachstums unter harten oder nährstoffarmen Bedingungen schlecht funktioniert. Bei Bakterien und Hefen haben Experimente gezeigt, dass schnell wachsende Zellen einen größeren Anteil ihres Proteinbudgets den Ribosomen zuweisen — den molekularen Maschinen, die neue Proteine herstellen — während langsam wachsende Zellen Ressourcen anderswohin verlagern.
Ein Archaeon, das die Regeln bricht
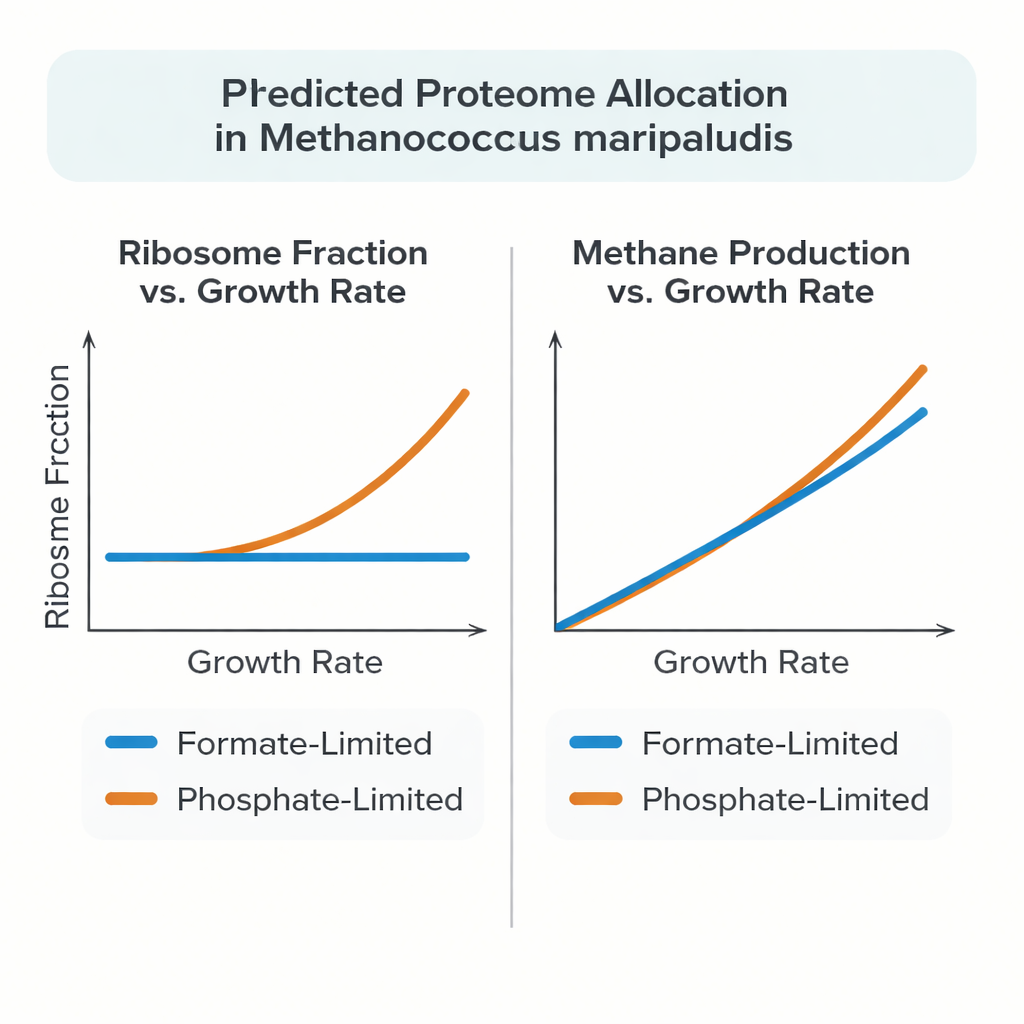
Neuere Experimente zeigten, dass M. maripaludis diesem Muster nicht immer folgt. Wenn es mit Format als sowohl Nährstoff als auch Energiequelle wächst, bleibt der Anteil seines Proteinbudgets, der in Ribosomen investiert ist, beim Abbremsen des Wachstums nahezu konstant. Unter Phosphatbegrenzung hingegen verhält sich das Archaeon konventioneller: Der Ribosomenanteil steigt mit der Wachstumsrate, ähnlich wie bei Escherichia coli und Hefe. Um dieses ungewöhnliche Verhalten zu erklären, entwickelten die Autoren ein detailliertes Ganzzell-ähnliches Modell, das den Stoffwechsel mit dem kostenintensiven Prozess der Herstellung und Assemblierung von Proteinen und RNA verknüpft, statt Proteine als abstrakte Reaktionsraten zu behandeln.
Aufbau eines Ganzzell-ähnlichen Modells
Die Forscher begannen mit einer bestehenden Stoffwechselkarte von M. maripaludis und ergänzten tausende zusätzlicher Reaktionen, die die Genexpression beschreiben: das Kopieren von DNA in RNA, das Beladen von Transfer-RNAs, den Aufbau von Ribosomen und Enzymkomplexen sowie die Verdünnung dieser Komponenten während der Zellteilung. Sie sammelten Geschwindigkeitsgrenzen von Enzymen aus biochemischen Datenbanken und der Literatur und schätzten, welcher Anteil der Proteinmasse aus „unmodellierten“ Proteinen besteht, die nicht direkt mit den Reaktionen in der Karte verknüpft sind. Anschließend legten sie globale Beschränkungen fest, die die Gesamtmasse von Protein und RNA begrenzen, Reaktionsraten an die verfügbare Enzymmenge binden und die Proteinproduktion an die Kapazität der Ribosomen koppeln. Mit diesen Beschränkungen muss das Modell entscheiden, wie ein fixes Proteinbudget zur Unterstützung des Wachstums verteilt wird.
Was die Simulationen zeigten
Gegenüber hochwertiger Chemostat-Experimentaldaten reproduzierte das Modell genau gemessene Protein- und RNA-Massen, Methanproduktionsraten und Wachstumserträge über einen Bereich niedriger Wachstumsraten. Unter Formatbegrenzung legte die simulierte Zelle von selbst einen nahezu konstanten Ribosomenanteil bei veränderlichem Wachstum fest, was die experimentellen Daten widerspiegelt. Unter Phosphatbegrenzung stimmte das Modell mit dem beobachteten Anstieg des Ribosomenanteils nur überein, wenn die Ribosomen bei niedrigen Wachstumsraten schneller arbeiten durften — konsistent mit Messungen, die zeigen, dass mehr Ribosomen aktiv an der Proteinsynthese beteiligt sind. Das Modell deutete außerdem an, dass ein beträchtlicher Anteil der Proteine in M. maripaludis nicht strikt für minimales Wachstum erforderlich ist und dass überschüssiger Kohlenstoff und Energie je nach begrenzendem Nährstoff in andere große Moleküle wie Glykogen oder freie Aminosäuren gespeichert oder umgeleitet werden können.
Mutanten und Wachstumsgrenzen untersuchen
Weil das Modell explizit die Proteinkosten jedes Weges berücksichtigt, kann es nicht nur vorhersagen, ob genetische Mutanten wachsen können, sondern auch, wie gut sie im Vergleich zum Wildtyp wachsen. Die Autoren simulierten Stämme, denen verschiedene wasserstoffverarbeitende Enzyme fehlen, und verglichen die vorhergesagte Fitness mit Labor-Messungen unter mehreren Wachstumsbedingungen, einschließlich Anwesenheit oder Abwesenheit von Wasserstoff und Kohlenmonoxid. In vielen Fällen sagte das Modell korrekt voraus, ob Mutanten wachsen können, und lieferte vernünftige Schätzungen ihrer relativen Wachstumsraten — eine Verbesserung gegenüber früheren Modellen, die nur Ja-/Nein-Antworten geben konnten. Dasselbe Rahmenwerk wurde verwendet, um maximale mögliche Wachstumsraten unter Batch-Bedingungen für verschiedene Substratkombinationen abzuschätzen.
Was das für Wissenschaft und Technik bedeutet
Einfach gesagt zeigt die Studie, dass M. maripaludis eine alternative Strategie zur Budgetierung seiner Proteinbelegschaft verwendet: Unter manchen Bedingungen hält es seine Proteinfabriken auf einem konstanten Anteil des Budgets, anstatt sie bei verlangsamtem Wachstum zurückzufahren. Indem dieses Verhalten in ein detailliertes, datenbasiertes Modell eingebettet wird, liefert die Arbeit ein Testbett, um zu erforschen, wie energiebegrenzte Mikroben Wachstum, Erhaltung und Speicherung ausbalancieren. Für angewandte Forschung bietet das Modell eine Landkarte, um dieses Archaeon so zu konstruieren, dass es mehr Methan oder andere Produkte erzeugt, indem es identifiziert, welche Enzyme und Wege in Bezug auf Proteininvestitionen am kostenintensivsten sind. Größer gedacht erweitert es leistungsfähige Ganzzell-ähnliche Modellierung jenseits von Bakterien und Hefe in den Bereich der Archaeen und hilft, die Lücke zwischen molekularen Details und dem großskaligen Verhalten mikrobieller Gemeinschaften zu schließen, die für Klima, Energie und industrielle Biotechnologie relevant sind.
Zitation: Kasem, G.S., Soliman, T.H.A., Mousa, M.A.A. et al. Whole-cell modeling predicts alternative proteome allocation strategies in the archaeon Methanococcus maripaludis. Sci Rep 16, 7386 (2026). https://doi.org/10.1038/s41598-026-37887-z
Schlüsselwörter: Methanococcus maripaludis, Proteom-Allokation, Ganzzellmodellierung, Methanogenese, Stoffwechsel von Archaeen