Clear Sky Science · de
Sepsis‑Ereignis erzeugt unterschiedliche vaskuläre Reaktionsphenotypen: eine unüberwachte Zeitreihen‑Clustering‑präklinische Studie
Warum das für Patienten mit schweren Infektionen wichtig ist
Sepsis, eine lebensbedrohliche Reaktion auf eine Infektion, kann innerhalb von Stunden den Blutdruck zum Absturz bringen und mehrere Organe schädigen. Ärztinnen und Ärzte erkennen drohendes Kreislaufversagen jedoch meist erst an späten Symptomen – etwa sehr niedrigem Druck oder erhöhtem Laktat. Diese Studie an Schweinen stellt eine einfache, aber wichtige Frage: Verbergen sich in der Form jeder Blutdruckwelle frühe Hinweise darauf, dass der Kreislauf zu versagen beginnt, und verlaufen verschiedene Tiere auf unterschiedlichen Wegen in den Schock? Wenn solche Muster gefunden werden können, könnten Monitorgeräte am Bett eines Tages Klinikern früher warnen und die Behandlung an die individuelle Reaktion jedes Patienten anpassen.
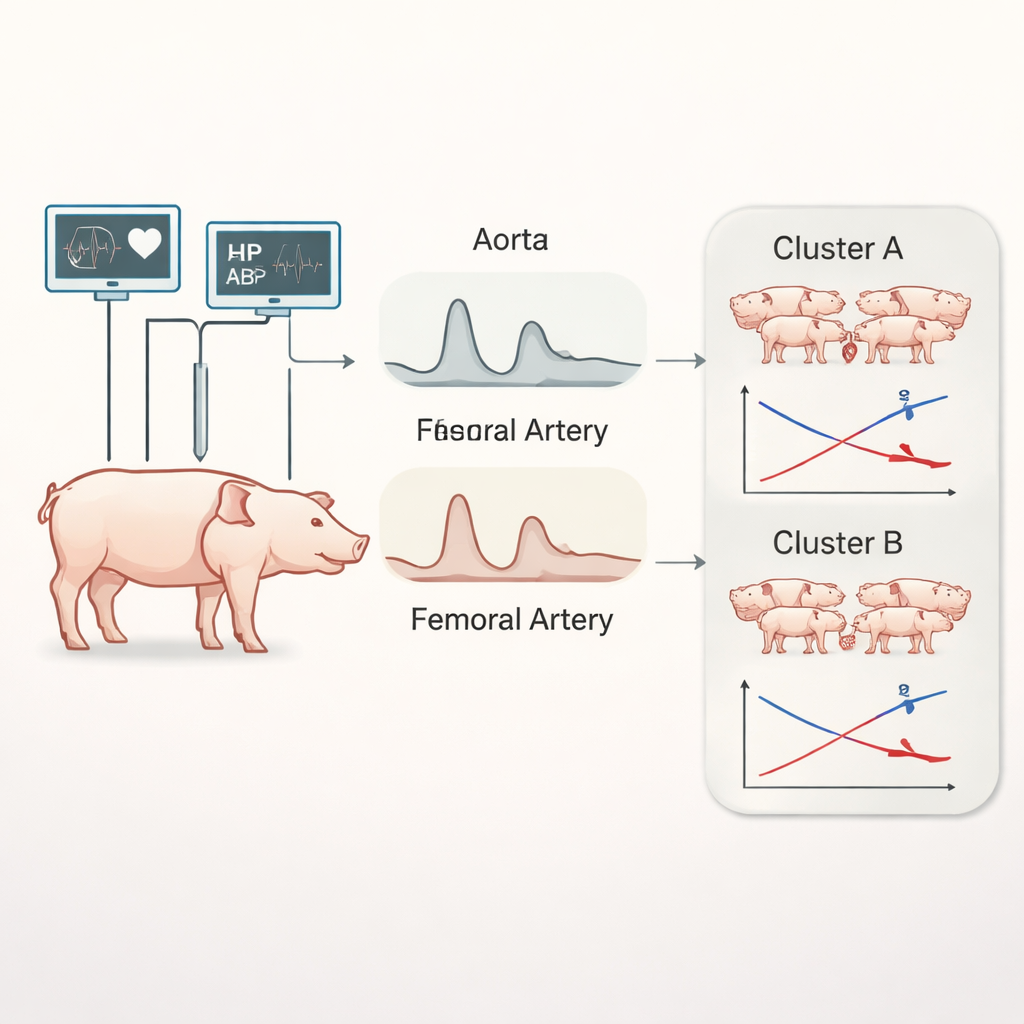
Blick in jeden Herzschlag
Auf Intensivstationen zeigt eine arterielle Leitung den Blutdruck Schlag für Schlag als wellenförmige Kurve auf dem Monitor. Meist konzentrieren sich die Klinikteams auf einfache Zahlen – mittlerer Druck und Pulsdruck – während die detaillierte Form der Welle wenig beachtet wird. In dieser präklinischen Studie zeichneten Forschende kontinuierlich hochwertige Blutdrucksignale aus der Hauptschlagader nahe dem Herzen und aus einer Beinarterie bei 40 Schweinen auf, während diese von gesundem Zustand in einen vollständigen septischen Schock übergingen, der durch eine kontrollierte Bauchinfektion ausgelöst wurde. Neben bekannten Messgrößen wie mittlerem arteriellen Druck, Herzfrequenz, Herzzeitvolumen und Pulsdruck extrahierte das Team neuere Indizes, die beschreiben, wie elastisch oder steif die Gefäße sind, wie stark das Nervensystem den Druck reguliert und wie komplex die Druckwelle wird, während sie durch den Körper wandert.
Zwei verschiedene Wege in den septischen Schock
Indem diese Messungen alle zwei Minuten über viele Stunden verfolgt wurden, nutzten die Untersuchenden unüberwachtes Zeitreihen‑Clustering – eine Form des maschinellen Lernens, die nach natürlichen Gruppierungen in Daten sucht, ohne vorab zu etikettieren –, um zu prüfen, ob die kardiovaskulären Reaktionen der Schweine in unterscheidbare Muster fallen. Obwohl bei Eintritt des vollständigen septischen Schocks alle Tiere dieselben klinischen Kriterien erfüllten – niedriger mittlerer Druck, schnelle Herzfrequenz und reduziertes Herzzeitvolumen – zeigte die Analyse zwei klare Verhaltenscluster. In der einen Gruppe begann der Blutdruck bald nach dem Infekt zu sinken und setzte einen stetigen Abfall fort, begleitet von relativ moderaten Anstiegen der Herzfrequenz und des Herzzeitvolumens. Diese Schweine schienen keine starke kompensatorische Antwort zu mobilisieren und glitten mit allmählich schlechter werdender Zirkulation in den Schock.
Verborgene Signale in der Pulswelle
Die zweite Gruppe erzählte eine andere Geschichte. Über mehrere Stunden blieb ihr Blutdruck trotz Infektion näher an normalen Werten. Diese Stabilität wurde durch einen starken Anstieg der Herzfrequenz und die Aufrechterhaltung des Herzzeitvolumens erreicht. Unter der Oberfläche jedoch schilderten die detaillierten, wellenformbasierten Indizes ein nuancierteres Bild. Ein Maß dafür, wie stark der Pulsdruck zunimmt, wenn er von der zentralen Aorta zur Beinarterie wandert – die Pulsdruckamplifikation – kehrte sich in beiden Gruppen um und signalisierte den Zusammenbruch der üblichen Beziehung zwischen zentralen und peripheren Gefäßen lange bevor ein offensichtlicher Schock auftrat. Eine Zeitkonstante, die mit der Geschwindigkeit zusammenhängt, mit der Blut während jedes Herzschlags aus den Arterien abfließt, verkürzte sich und deutete auf durchlässige, dilatierte Gefäße hin. Und ein Index der Wellenformkomplexität, genannt harmonische Verzerrung, bewegte sich in entgegengesetzte Richtungen: In einer Gruppe wurde die Druckwelle glatter und einfacher, in der anderen komplexer, was auf unterschiedliche Muster von Gefäßversteifung und Wellenreflexion hindeutet.
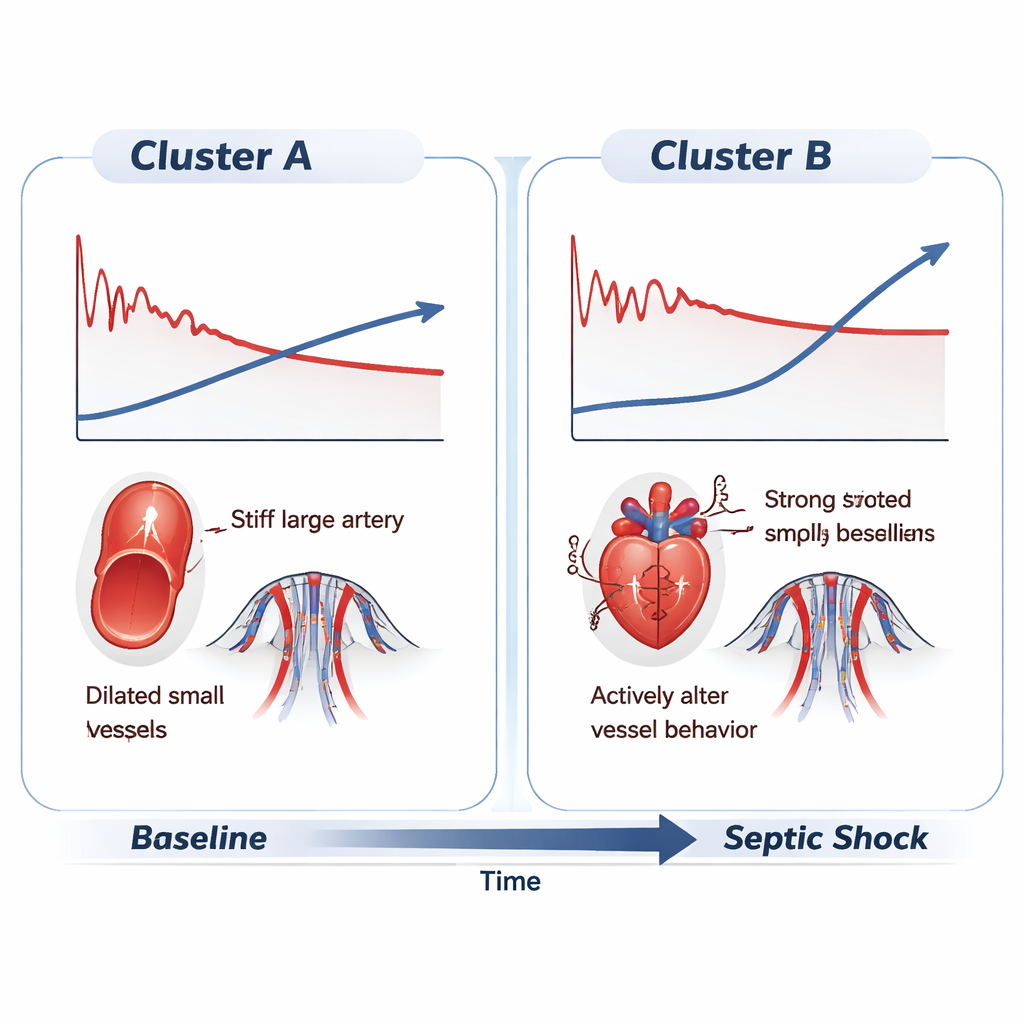
Von komplexen Daten zu einfachen Mustern
Um sicherzustellen, dass diese Muster keine statistischen Zufälle waren, wendeten die Forschenden eine Technik namens Shapelet‑Analyse an, die in langen Zeitreihen nach kurzen Segmenten sucht, die eine Gruppe am besten von einer anderen unterscheiden. Diese Methode hob dieselben Merkmale hervor: ein stetig fallendes Druckmuster versus ein zunächst erhaltenes, dann kollabierendes Muster; auseinanderlaufende Trends in der Wellenformkomplexität; und unterschiedliche Verläufe in der Wechselwirkung zwischen Herzschlägen und dem arteriellen Baum. Bemerkenswert ist, dass schon vor Induktion der Sepsis die Schweine, die später in die jeweiligen Cluster fielen, subtile Unterschiede in Indizes im Zusammenhang mit Gefäßfunktion und nervaler Steuerung zeigten, obwohl sie ähnliche Standardblutdruckwerte hatten. Das legt nahe, dass Tiere – und übertragen auf Menschen – mit unterschiedlichen zugrunde liegenden kardiovaskulären „Einstellungen“ in eine Sepsis eintreten können, die beeinflussen, wie sie auf denselben Reiz reagieren.
Was das für die künftige Versorgung bedeuten könnte
Für Nicht‑Spezialisten ist die wichtigste Erkenntnis, dass in der Blutdruckkurve auf dem Monitor viel mehr Information steckt als nur eine einzige Zahl. Durch die Analyse der feinen Struktur jedes Pulses über die Zeit zeigt diese Arbeit, dass frühe Veränderungen im Verhalten der Arterien während einer Sepsis erkannt und unterschiedliche „Phänotypen“ der vaskulären Antwort aufgedeckt werden können, die an Routinediagnostik am Bett identisch aussehen. Wenn ähnliche Befunde bei Menschen bestätigt werden, könnten Krankenhäuser bestehende Monitore mit Software erweitern, die diese wellenformbasierten Marker automatisch verfolgt. Solche Werkzeuge könnten Patienten melden, die Stunden bevor traditionelle Zeichen erscheinen, ein hohes Risiko für rasche Verschlechterung haben, und Klinikern helfen, Therapien zu wählen, die zum spezifischen Muster des Kreislaufversagens jedes Patienten passen.
Zitation: Vida, I., Carrara, M. & Ferrario, M. Sepsis insult generates different vascular response phenotypes: an unsupervised time-series clustering preclinical study. Sci Rep 16, 6960 (2026). https://doi.org/10.1038/s41598-026-37885-1
Schlüsselwörter: Sepsis, Blutdruckkurve, vaskuläre Dysfunktion, Überwach ung auf der Intensivstation, maschinelles Lernen