Clear Sky Science · de
Interleukin-7 induziert EMT und fördert Tumorwachstum sowie Metastasenbildung bei NSCLC über den Notch1/TGF-β-Weg
Warum ein Signalmolekül bei Lungenkrebs wichtig ist
Lungenkrebs gehört weiterhin zu den tödlichsten Krebserkrankungen weltweit, vor allem weil er häufig erst entdeckt wird, nachdem er bereits gestreut hat. Diese Studie konzentriert sich auf einen natürlich vorkommenden Immunboten, Interleukin‑7 (IL‑7), und stellt eine drängende Frage: Hilft IL‑7 beim nicht‑kleinzelligen Lungenkrebs (NSCLC) dem Körper, den Tumor zu bekämpfen, oder unterstützt es stattdessen das Tumorwachstum und die Ausbreitung? Indem die Forschenden nachverfolgen, wie IL‑7 Lungenkrebszellen bei Patienten, in Zellkulturen und in Mäusen beeinflusst, entwirren sie einen Weg, der offenbar Tumoren zu stärkerem Wachstum, größerer Streuung und Behandlungsminderung treibt.
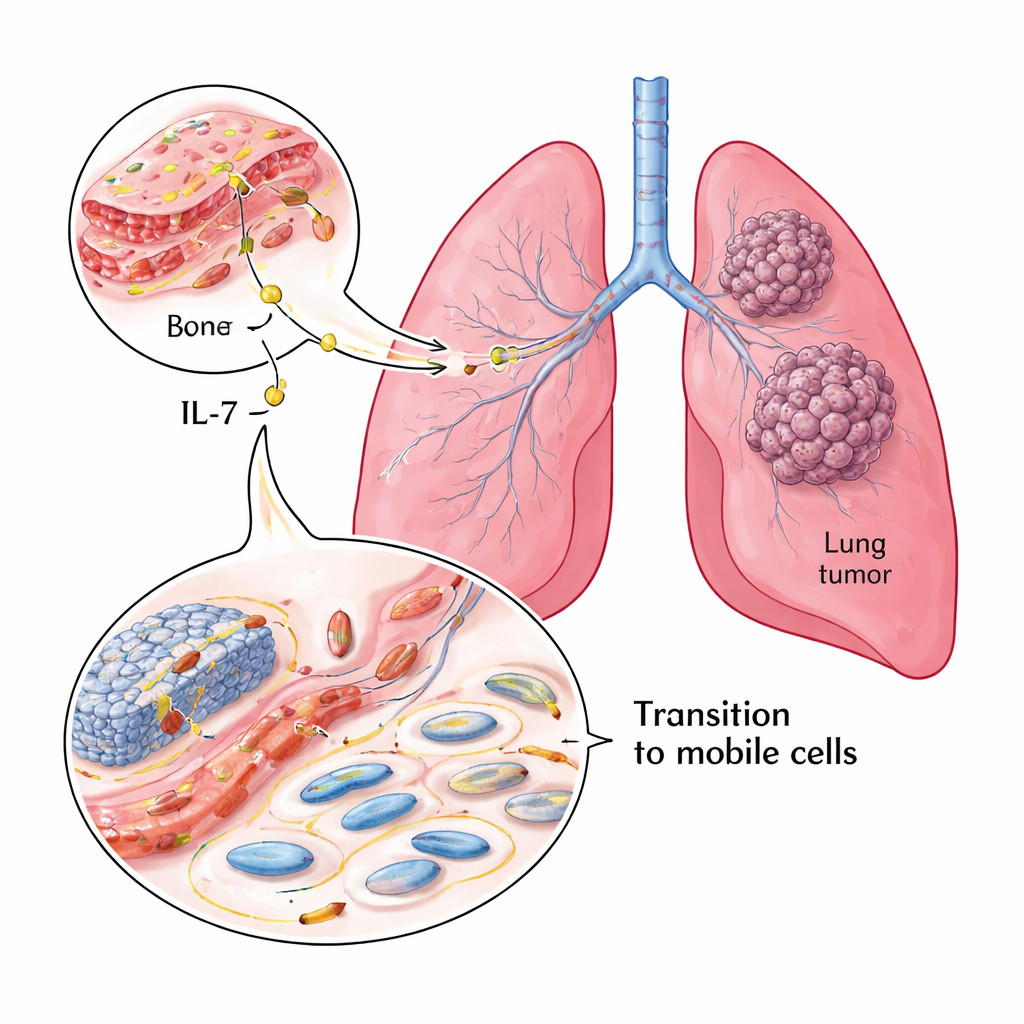
Ein genauerer Blick auf Tumoren und Patientenergebnisse
Das Team begann mit der Untersuchung von Tumorproben aus 119 NSCLC-Patienten. Mittels Färbetechniken an fixiertem Gewebe bestimmten sie die Mengen an IL‑7, dessen Rezeptor (IL‑7R) und zwei Schlüsselmarker, die beschreiben, wie "verankert" oder "beweglich" Krebszellen sind. E‑Cadherin steht für eng verbundene, weniger mobile Zellen, während Vimentin mit flexibleren, invasiven Zellen verknüpft ist. Die meisten Tumoren zeigten hohe IL‑7- und IL‑7R-Werte. Wo IL‑7 und IL‑7R reichlich vorhanden waren, war meist E‑Cadherin niedrig und Vimentin hoch — ein ungünstiges Muster. Patienten, deren Tumoren mehr E‑Cadherin aufwiesen, überlebten länger, während hohe IL‑7R-Spiegel mit schlechterem Überleben einhergingen, sodass IL‑7R ein starker Prädiktor für den Verlauf war.
Wie Krebszellen vom Verweilen zum Abwandern wechseln
Um über Korrelationen hinauszugehen, prüften die Forschenden, wie IL‑7 Zellen des Lungenkarzinoms direkt in vitro beeinflusst. Wurden zwei NSCLC-Zelllinien IL‑7 ausgesetzt, wandelte sich das Erscheinungsbild von kompakten, kopfsteinpflasterartigen Zellverbänden zu länglicheren, freier beweglichen Formen. Auf Proteinebene veränderten sich die Marker parallel: E‑Cadherin sank, während "Beweglichkeitsmarker" wie N‑Cadherin, Vimentin und Snail1 anstiegen. Das Aktin-Zytoskelett, das das Zellkriechen unterstützt, wurde ebenfalls prominenter und bildete Fortsätze. Die Blockade des IL‑7-Rezeptors kehrte diese Effekte um, was darauf hinweist, dass IL‑7 diesen Formwandel — die epithelial‑mesenchymale Transition (EMT) — über seinen eigenen Rezeptor auf Lungenkrebszellen antreibt.
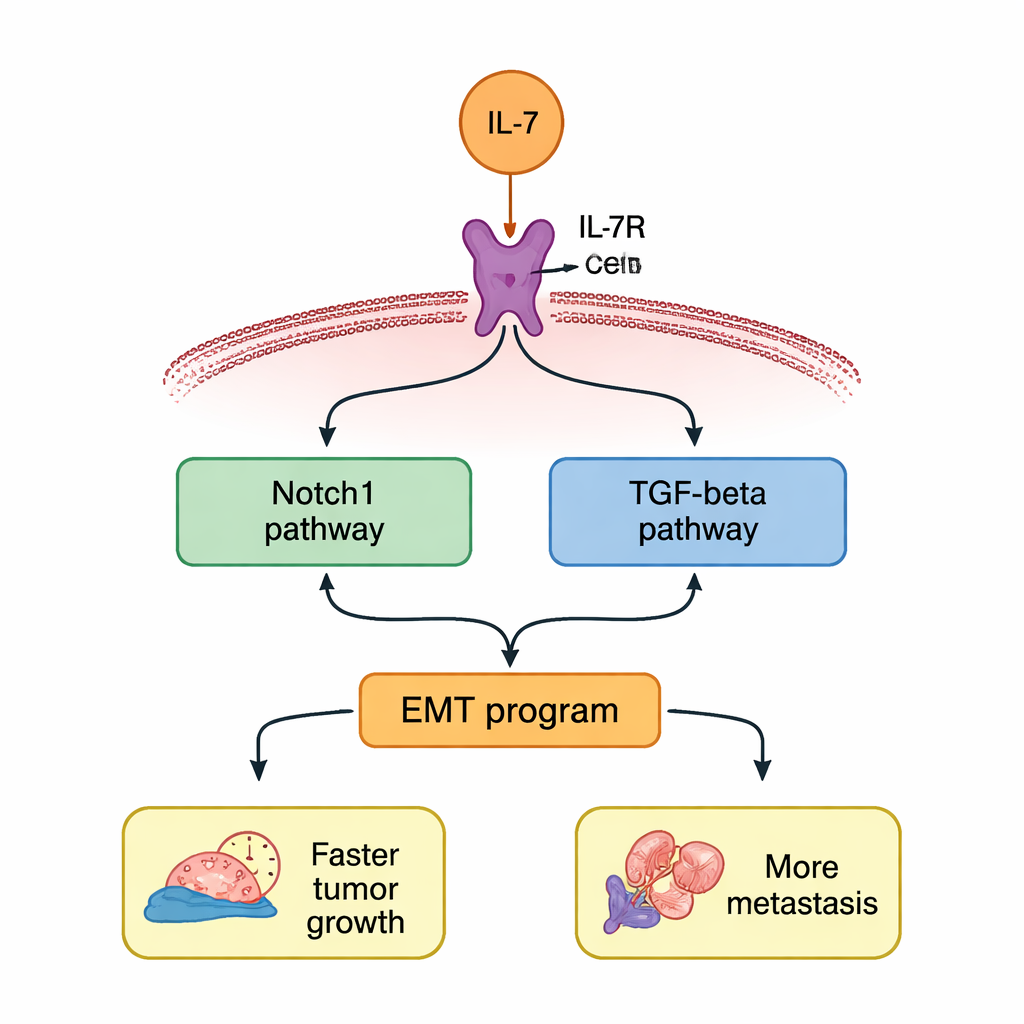
Zwei miteinander verbundene Wege, die die Gefahr verstärken
Die Studie fragte weiter, wie IL‑7 diese Signale innerhalb der Zelle übermittelt. Die Autorinnen und Autoren konzentrierten sich auf zwei bekannte Signalwege, die oft in aggressiven Tumoren aktiv sind: Notch1 und TGF‑β. Nach IL‑7‑Behandlung stiegen sowohl Notch1 als auch TGF‑β auf Gen‑ und Proteinebene in den Lungenkrebszellen an. Wurde IL‑7R blockiert, entfielen diese Anstiege. Setzten die Forschenden spezifische Inhibitoren gegen Notch1 oder TGF‑β ein, beruhigten sich beide Wege gleichzeitig, was auf eine Art positive Rückkopplung hindeutet, bei der jeder Weg den anderen stützt. Das Abschneiden eines der beiden Wege unterdrückte teilweise das EMT‑Programm und verringerte den durch IL‑7 verstärkten Zuwachs an Zellproliferation, Migration und Invasion.
Vom Petrischälchen zur lebenden Lunge
Um zu prüfen, ob die Laborbefunde in lebenden Organismen gelten, verwendete das Team Mausmodelle. In einer Versuchsreihe wurden Lungenkrebszellen subkutan implantiert. Mäuse, denen IL‑7 verabreicht wurde, entwickelten größere und schwerere Tumoren als Kontrollen. Tumorgewebe dieser Tiere zeigte niedrigere E‑Cadherin‑Werte, höhere Vimentin‑ und Snail1‑Werte sowie eine erhöhte Aktivität von Notch1 und TGF‑β. Erhielten die Mäuse zusätzlich Inhibitoren von Notch1 oder TGF‑β, waren Tumorwachstum und diese aggressiven Marker deutlich reduziert. In einem zweiten Modell wurden Krebszellen über die Schwanzvene in den Blutkreislauf injiziert. Hier entwickelten IL‑7‑behandelte Mäuse mehr Lungenmetastasen und schwerere Lungen, während die Wegblocker erneut die Ausbreitung eindämmten.
Was das für die zukünftige Behandlung von Lungenkrebs bedeutet
In der Summe zeichnet die Arbeit IL‑7 nicht als einfachen Immunhelfer, sondern als zweischneidiges Schwert beim NSCLC. In diesem Kontext scheint IL‑7 Tumorzellen dazu zu bringen, ihre Bindungen zu lockern, eine mobilere Identität anzunehmen und an neue Orte zu wandern — vermittelt durch ein verstärkendes Netzwerk, das auf Notch1 und TGF‑β zentriert ist. Für Patientinnen und Patienten deuten diese Befunde darauf hin, dass hoher IL‑7R‑Ausdruck in Tumoren eine ungünstigere Prognose signalisieren kann und dass gezielt entwickelte Therapien gegen IL‑7/IL‑7R oder deren nachgeschaltete Wege das Tumorwachstum und die Metastasierung verlangsamen könnten. Zwar sind weitere Studien nötig, um die genauen molekularen Verknüpfungen zu kartieren und die Sicherheit beim Menschen zu prüfen, doch die Studie hebt ein vielversprechendes Set von Hebeln hervor, um das Gleichgewicht gegen Lungenkrebs zu verschieben.
Zitation: Shao, Y., Cheng, H., Ni, W. et al. Interleukin-7 induces EMT to promote tumor growth and metastasis in NSCLC via Notch1/TGF-β pathway. Sci Rep 16, 7326 (2026). https://doi.org/10.1038/s41598-026-37876-2
Schlüsselwörter: nicht-kleinzelliges Lungenkarzinom, Interleukin-7, epithelial-mesenchymale Transition, Notch1-Signalweg, TGF-beta-Signalübertragung