Clear Sky Science · de
Das Nukleokapsidprotein von SARS-CoV-2 bildet Komplexe mit löslichen Komplementregulatoren, die an das Virion binden können
Warum dieser verborgene virale Trick wichtig ist
Die meisten von uns haben vom Coronavirus‑„Spike“-Protein gehört, weil es das Hauptziel der Impfstoffe ist. Im Inneren des Virus befindet sich jedoch ein anderes Protein, das Nukleokapsid‑ oder N‑Protein, das sich als weit mehr als eine strukturelle Verpackung erweist. Diese Studie zeigt, dass das N‑Protein an wichtige menschliche Immunregulatoren im Blut andocken und diese auf die Virusoberfläche transportieren kann. Dadurch könnte SARS‑CoV‑2 einen unserer frühesten Abwehrmechanismen – das Komplementsystem – teilweise ausschalten, dem Virus das Überleben erleichtern und möglicherweise zu schwerem COVID‑19 beitragen.
Ein genauerer Blick auf das innere Protein des Virus
Das N‑Protein ist die Genom‑„Hülle“ des Virus und hilft, seine RNA zu verpacken und zu stabilisieren. Ärztinnen und Ärzte finden hohe Konzentrationen des N‑Proteins im Blut von COVID‑19‑Patienten, insbesondere bei schweren Verläufen, und frühere Arbeiten deuten darauf hin, dass es entzündliche Signale verstärken kann. Die Autorinnen und Autoren fragten, ob N auch das Komplementsystem stören könnte, ein Netzwerk von Blutproteinen, das Eindringlinge markiert und zerstört und dabei Membranen perforieren kann. Viele Viren haben raffinierte Wege entwickelt, körpereigene Komplementregulatoren zu entleihen oder nachzuahmen, um Angriffen zu entgehen. Das Team stellte drei Fragen: Bindet N an das Spike‑Protein und an das Virus selbst, bindet es menschliche komplementregulatorische Proteine im Blut, und kann es diese Regulatoren auf die Virusoberfläche bringen?
Wie N und Spike auf dem Virus zusammentreffen
Mit mehreren Protein‑Bindungstests zeigten die Forschenden, dass das N‑Protein direkt an das Spike‑Protein binden kann, sowohl wenn Spike im Labor hergestellt wurde als auch wenn es auf echten SARS‑CoV‑2‑Partikeln vorliegt. Sie bestätigten diese Wechselwirkung in verschiedenen Versuchsaufbauten und quantifizierten ihre Stärke, wobei die Affinität der vieler Antikörper ähnelte. Durch Zerlegen des Spike‑Proteins in Fragmente und Bestimmen, welche Teile an N haften blieben, konnten sie wahrscheinliche Kontaktzonen hauptsächlich in der N‑terminalen Domäne des Spike lokalisieren, einer Region, die bereits als Hotspot für Antikörperbindung und für das Andocken bestimmter Wirtsmoleküle bekannt ist. Das deutet darauf hin, dass N eine feste, biologisch bedeutsame Brücke zu Spike auf tatsächlichen Virionen bilden kann.
Die Sicherheitsbremsen des Körpers kapern
Das Komplementsystem wird streng durch lösliche „Bremsen“ kontrolliert, sogenannte komplementregulatorische Proteine, die unsere eigenen Zellen vor Fehlangriffen schützen. Das Team konzentrierte sich auf vier dieser Proteine—C1‑Inhibitor, C4‑bindendes Protein, Faktor H und Vitronectin—weil sie an verschiedenen Stellen der Komplementkaskade wirken. In Seren‑basierten Tests und mit gereinigten Proteinen band das N‑Protein alle vier Regulatoren, während Spike unter denselben Bedingungen keines von ihnen anhing. Das bedeutet, dass N‑CRP‑Komplexe im Plasma entstehen können. Entscheidend ist, dass, wenn N zuvor mit menschlichem Serum vermischt und dann Viren ausgesetzt wurde, die Forschenden diese Regulatoren an den Virionen nachweisen konnten—aber nur, wenn N vorhanden war. Je mehr N eingesetzt wurde, desto mehr Komplementregulatoren traten am Virus auf, was auf einen dosisabhängigen Rekrutierungsmechanismus hinweist. 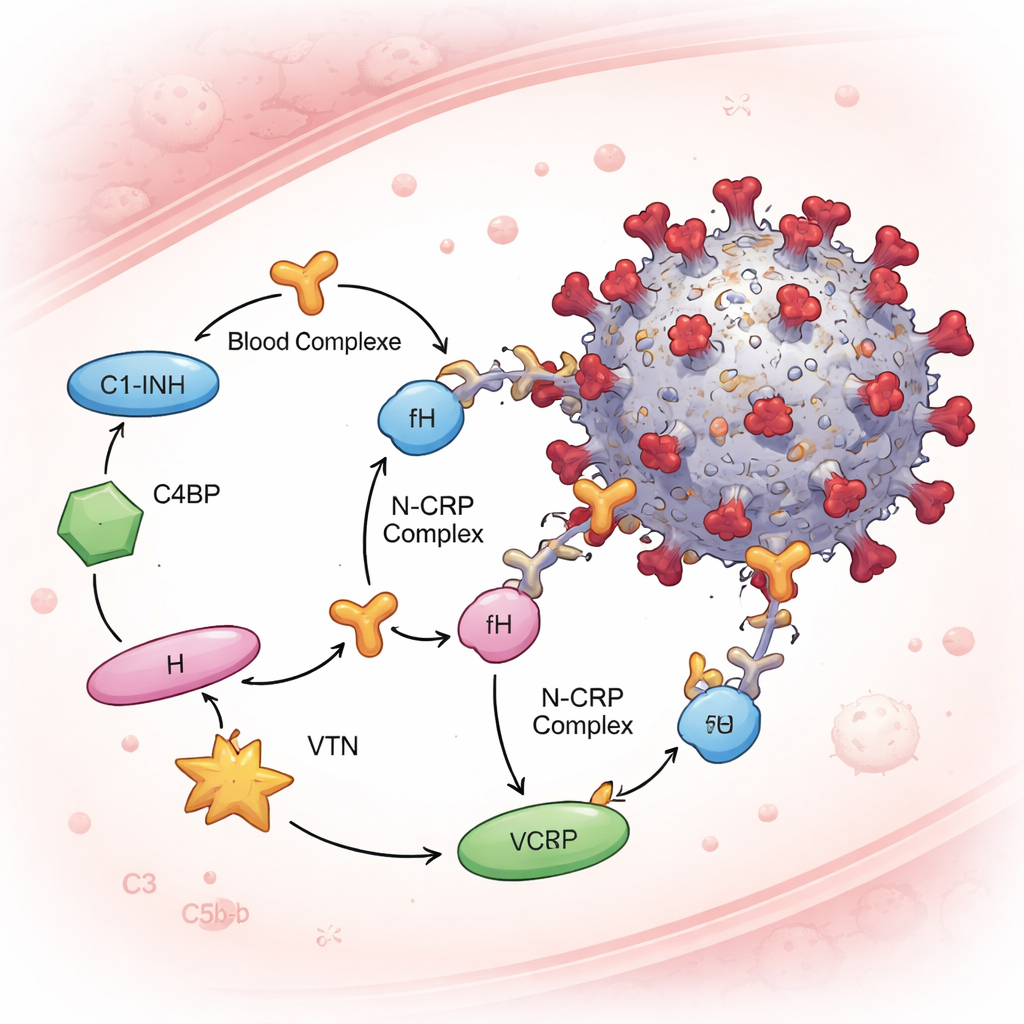
Den finalen Angriff abschwächen
Die ultimative Waffe des Komplementsystems ist der Membranangriffskomplex (MAC), eine ringförmige Struktur, die Poren in Zell‑ oder Virenhüllen bildet. Die Autorinnen und Autoren prüften, ob N die MAC‑Bildung auf SARS‑CoV‑2 verändern kann. Sie inkubierten gereinigte Viren mit humanem Serum, mit oder ohne zugesetztes N‑Protein, und maßen dann, wie viel des C5b‑9‑Komplexes des MAC auf den Virionen landete. Ohne N akkumulierte das Virus C5b‑9, was auf einen aktiven Komplementangriff hinweist. In Anwesenheit von N sank die MAC‑Ablagerung konzentrationsabhängig: mehr N bedeutete weniger C5b‑9 am Virus. Das passt zu der Idee, dass N durch das Dekorieren des Virions mit Komplementregulatoren dessen Perforation verhindert. 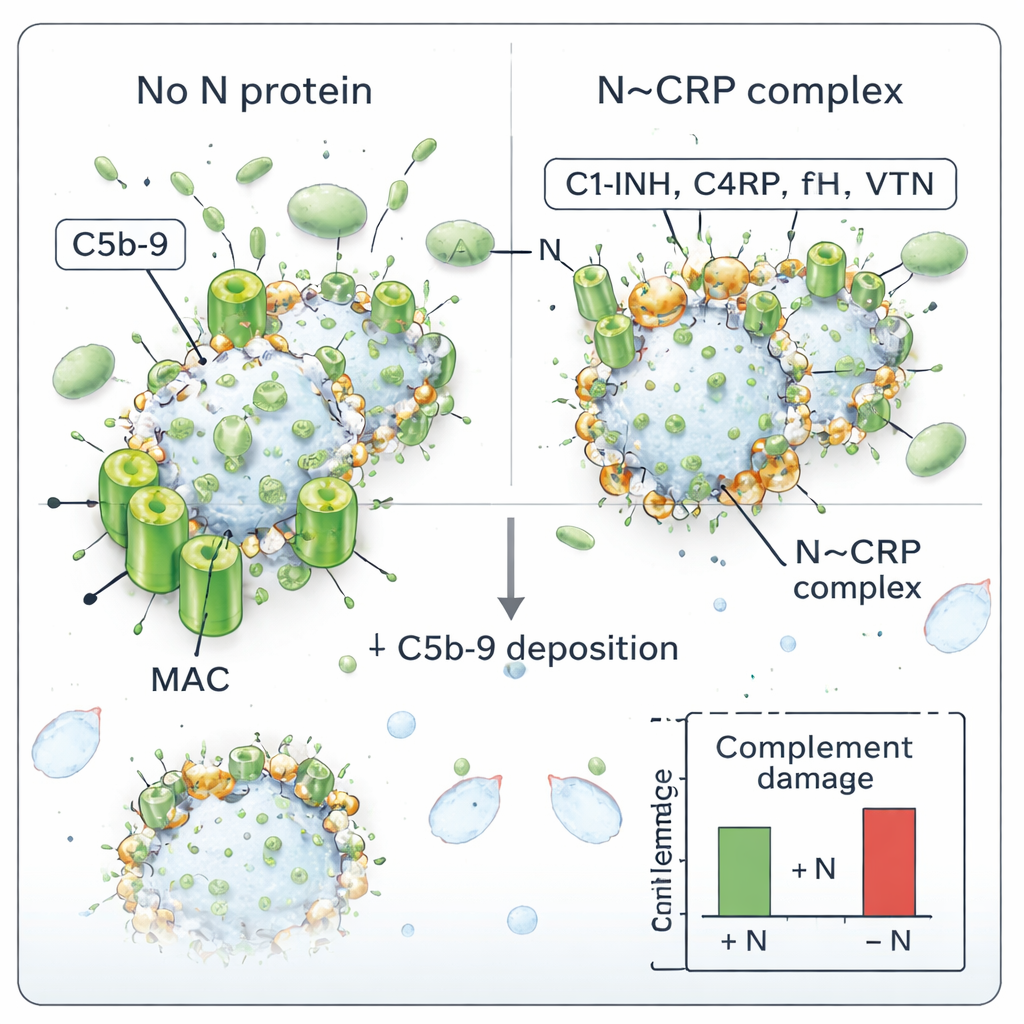
Was das für Patienten und künftige Therapien bedeutet
Für Nicht‑Fachleute ist die Kernbotschaft: SARS‑CoV‑2 verlässt sich nicht nur auf sein bekanntes Spike, um das Immunsystem auszutricksen. Sein internes N‑Protein kann ins Blut entweichen, die körpereigenen Komplement‑„Bremsen“ an sich binden und sie zurück auf die Virusoberfläche bringen. Dort können sie dem Virus helfen, sich vor einem mächtigen Teil der angeborenen Immunabwehr zu verbergen und direkte, komplementvermittelte Schäden zu verringern. Das könnte sowohl zu anhaltender Infektion als auch zu den komplexen Komplement‑Störungen beitragen, die bei schwerem COVID‑19 beobachtet werden. Zwar wurden diese Experimente unter kontrollierten Laborbedingungen durchgeführt, doch sie heben N‑Komplement‑Interaktionen als potenzielles neues Ziel hervor: Therapien, die die Bindung von N an diese Regulatoren blockieren oder die ein ausgewogeneres Komplementsystem wiederherstellen, könnten eines Tages helfen, das Kräfteverhältnis wieder zugunsten des Immunsystems zu verschieben.
Zitation: Víglaský, J., Bhide, K., Talpasova, L. et al. SARS-CoV-2 nucleocapsid protein forms complexes with soluble complement regulatory proteins that can bind to the virion. Sci Rep 16, 6599 (2026). https://doi.org/10.1038/s41598-026-37866-4
Schlüsselwörter: SARS-CoV-2 Nukleokapsid, Komplementsystem, Immunevasion, Komplementregulatorische Proteine, Schweregrad von COVID-19