Clear Sky Science · de
Der mTOR-Signalweg steuert zeitlich abgestimmt zentrale Schritte der Entstehung von Milchdrüsen-Organoiden
Warum winzige Brustmodelle wichtig sind
Unsere Brüste gehören zu den wenigen Organen, die sich wiederholt umbauen: Sie wachsen während der Pubertät und Schwangerschaft, produzieren Milch und schrumpfen nach dem Stillen wieder. Zu verstehen, wie dieses komplexe Remodelling gesteuert wird, ist entscheidend für die Gesundheit von Frauen — von erfolgreichem Stillen bis zum Krebsrisiko. Diese Studie nutzt dreidimensionale „Mini-Brüste“, sogenannte Organoide, die aus Maus-Zellen kultiviert werden, um zu zeigen, wie ein zellulärer Hauptwachstumsschalter, der mTOR-Weg, die zeitliche Abfolge und die Formung des Milchdrüsengewebes regelt.
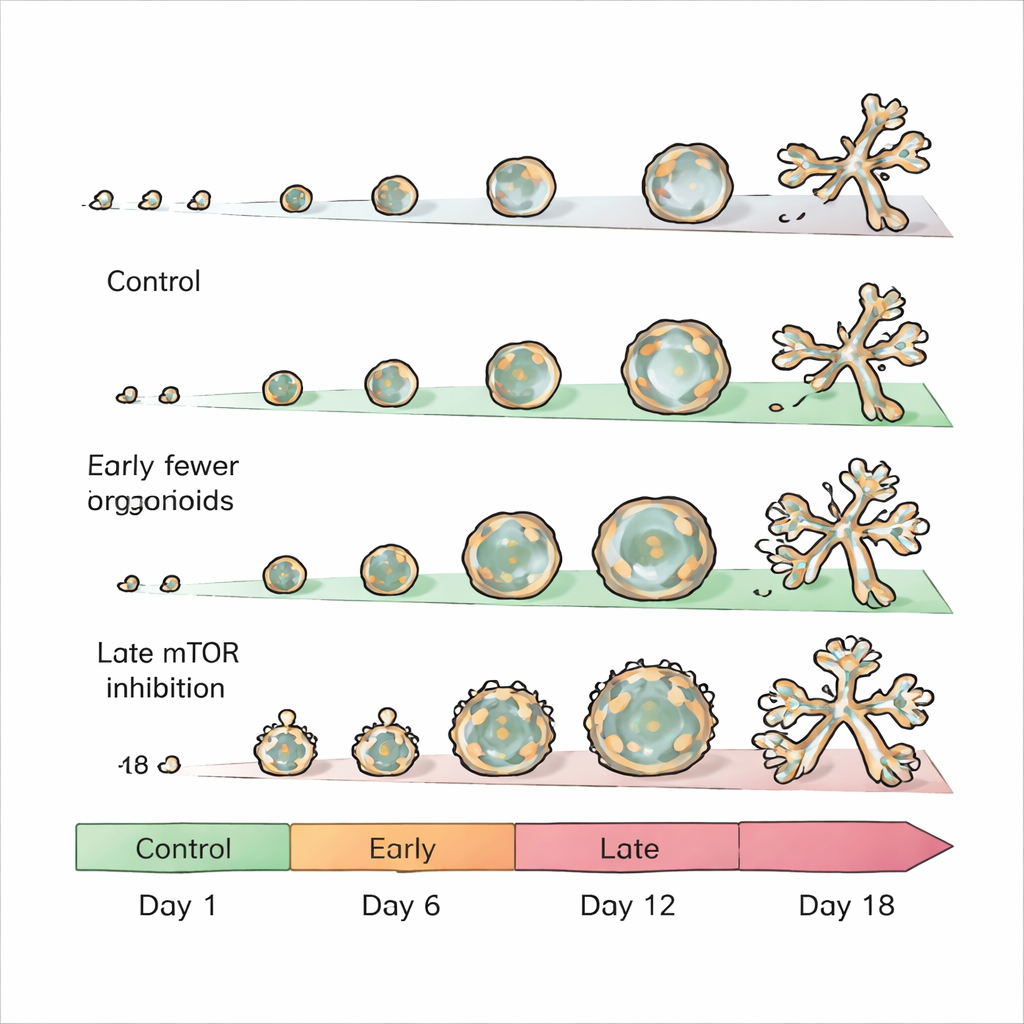
Eine zelluläre Ampel für Wachstum
mTOR ist ein zentraler Regulator, der Zellen hilft zu entscheiden, wann sie wachsen, sich teilen und ihren Stoffwechsel ändern sollen. Die Forschenden fragten, wie das Abschalten dieses Schalters zu unterschiedlichen Zeiten die Entwicklung der Organoide beeinflusst. Sie kultivierten murine epitheliale Zellen der Milchdrüse in einem Gel, das ihnen erlaubt, sich zu Strukturen zu organisieren, die winzigen Brustgängen mit einem Hohlraum und manchmal verzweigten „traubenartigen“ Ansammlungen ähneln. Anschließend setzten sie die bekannten mTOR-Hemmer Rapamycin und Torin 1 entweder sehr früh, mittig im Wachstumsverlauf oder später zu, genau zu dem Zeitpunkt, an dem normalerweise die Verzweigung beginnt.
Frühe Störung: Mini-Organe, die nie richtig entstehen
Wurde mTOR bereits ab dem ersten Tag blockiert, wuchsen die Organoide kaum. Ihr Durchmesser wurde um etwa zwei Drittel oder mehr reduziert, was zeigt, dass aktives mTOR für die frühe Expansion des Milchdrüsengewebes unerlässlich ist. Das entspricht mTORs Ruf als Treiber von Zellwachstum und Proteinproduktion. Da diese Organoide so klein und unterentwickelt blieben, konzentrierte sich das Team auf spätere Behandlungsfenster, in denen die Effekte nuancierter waren und besser aufzeigten, wie die interne Architektur des Gewebes gesteuert wird.
Änderung mittendrin: hohle Kugeln und verlorene Flexibilität
Eine Blockade von mTOR ab etwa Tag 6 — nachdem erste Strukturen gebildet, aber vor der Verzweigung — erzeugte unerwartet große, überwiegend hohle Organoide. Diese bestanden vorwiegend aus Lumen-Zellen, den inneren Zellen, die normalerweise die milchabsondernden Gänge auskleiden, während die äußere Basalschicht nahezu vollständig verloren ging. In der gesunden Entwicklung können sowohl einzelne luminale als auch basale Zellen Organoide hervorbringen, die beide Zelltypen enthalten — eine Eigenschaft, die als Linienplasticity bekannt ist. Eine mTOR-Hemmung in diesem mittleren Stadium schien diese Flexibilität praktisch einzufrieren, zwang die Zellen in eine luminale Identität und verhinderte das übliche Gleichgewicht der Schichten. Molekulare Analysen zeigten weitreichende Veränderungen in Gen- und Proteinniveaus, insbesondere Reduktionen in Komponenten der zellulären Stoffwechselmaschinerie und in Proteinen, die beim Umbau der umgebenden Matrix helfen — Befunde, die die veränderte Form und Zellzusammensetzung erklären helfen.
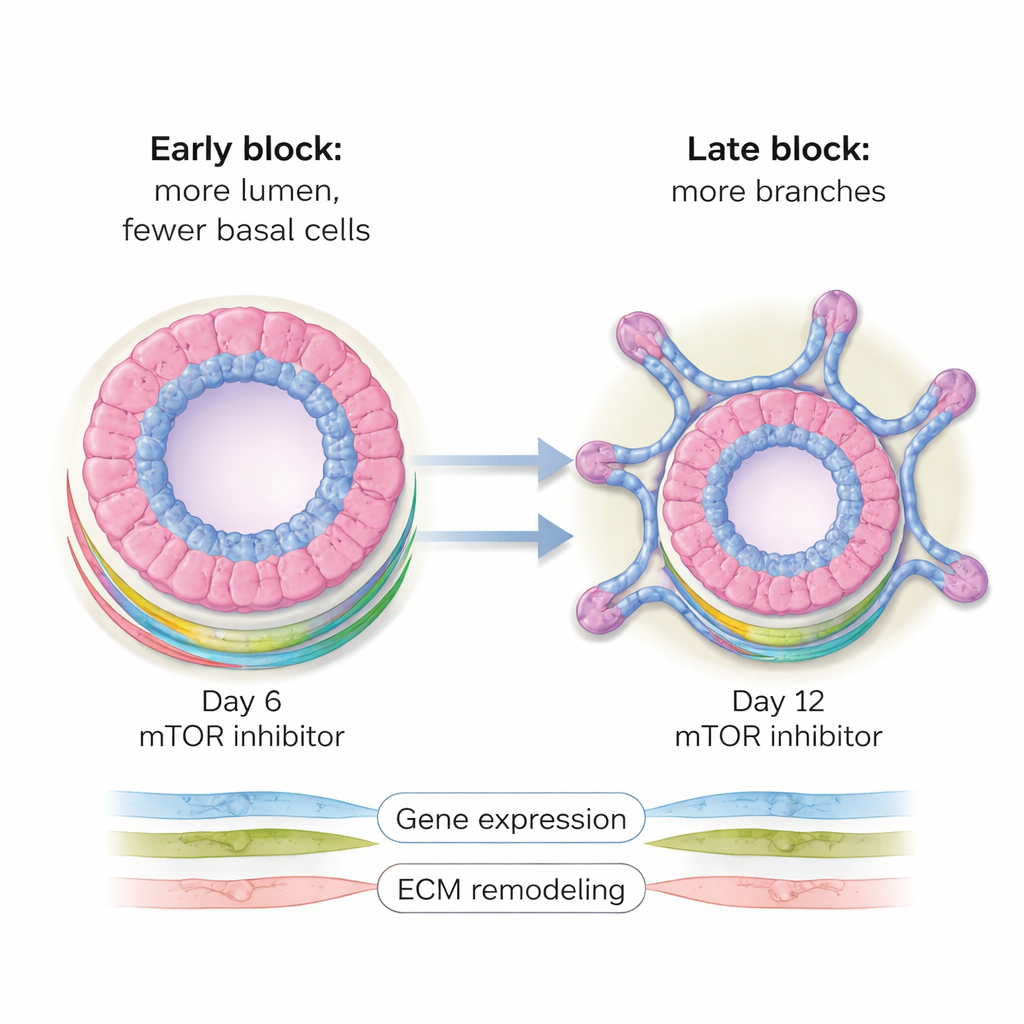
Späte Unterbrechung: mehr Verzweigungen, andere Vernetzung
Wurden die gleichen Wirkstoffe später zugegeben, etwa um Tag 12, genau wenn die Verzweigung typischerweise beginnt, kehrte sich das Ergebnis um. Statt vergrößerter, hohler Kugeln bildeten die Organoide nun mehr — und komplexere — verzweigte, knopfähnliche Strukturen, die den kleinen Säckchen ähneln, in denen Milch produziert wird. In diesem Setting blieb das Gleichgewicht zwischen luminalen und basalen Zellen weitgehend erhalten, aber die Anzahl der Verzweigungen und Knospen nahm im Vergleich zu unbehandelten Kontrollen deutlich zu. Muster der Genaktivität spiegelten diese Verschiebung wider: Viele Gene, die mit Gewebeformung und Verzweigung verbunden sind, wurden hochreguliert, während zahlreiche Gene des Stoffwechsels herunterreguliert wurden. Proteinmessungen bestätigten diese Ergebnisse und hoben Veränderungen in Komponenten der extrazellulären Matrix sowie in Stoffwechselwegen hervor, insbesondere in der Aminosäure- und Energieverarbeitung.
Was das für echte Brüste bedeutet
In der Summe zeigt die Arbeit, dass mTOR kein einfacher Ein-/Ausschalter für Wachstum ist, sondern ein zeitabhängiger Koordinator sowohl der Zellidentität als auch der Gewebe-Architektur in der Milchdrüse. Frühzeitig ist aktives mTOR nötig, damit Zellen wachsen und die Flexibilität bewahren, entweder zu luminalen oder zu basalen Zellen zu werden. Später verändert eine Modulation der mTOR-Aktivität, wie Zellen mit ihrer Umgebung interagieren, und kann so die Bildung verzweigter milchproduzierender Strukturen entweder dämpfen oder verstärken. Für Laien lautet die Kernaussage: Derselbe molekulare Weg kann je nach Zeitpunkt ganz unterschiedliche Aufgaben erfüllen — zuerst beim Aufbau der richtigen Zelltypen, später beim Formen dieser Zellen in die korrekte dreidimensionale Gestalt. Diese nuancierte Sicht ist wichtig, um normale Brustentwicklung, die Wirkung von mTOR-gerichteten Medikamenten und möglicherweise den Beitrag früher Veränderungen in diesem Weg zu Brustkrankheiten besser zu verstehen.
Zitation: Lacouture, A., Sylla, M.S., Germain, L. et al. The mTOR signaling pathway regulates key steps of mammary gland organoid genesis in a temporal manner. Sci Rep 16, 6751 (2026). https://doi.org/10.1038/s41598-026-37825-z
Schlüsselwörter: Entwicklung der Milchdrüse, mTOR-Signalgebung, Organoide, Verzweigungs-Morphogenese, Brustbiologie