Clear Sky Science · de
Berechnungsstrategien zum Entschlüsseln von Erkenntnissen aus bekannten Inhibitoren für die weitere Leitoptmierung: Eine Fallstudie zu Celecoxib‑Analoga
Warum winzige Änderungen in Schmerzmitteln wichtig sind
Moderne Schmerzmittel betäuben nicht nur Schmerzen; sie beeinflussen die Biochemie des Körpers auf sehr präzise Weise. Celecoxib, ein verbreitetes Entzündungshemmer, zielt auf ein Enzym ab, das an Schmerz und Schwellung beteiligt ist, und schont weitgehend ein Schwesterenzym, das die Magenschleimhaut schützt. Dennoch verhalten sich Dutzende chemisch nahe Verwandte von Celecoxib im Körper sehr unterschiedlich. Diese Studie nutzt Computermodelle, um eine auf den ersten Blick einfache, aber weitreichende Frage zu stellen: Wie viel bewirkt eine einzelne kleine Änderung in einem Molekül?
Das Enzym, das Schmerz einschaltet
Bei Gewebeschädigung oder Entzündung setzt der Körper ein Fettsäuremolekül namens Arachidonsäure frei. Ein Enzym namens COX‑2 wandelt dieses Molekül in Prostaglandine um, die Schmerzen, Fieber und Schwellungen auslösen. Ein verwandtes Enzym, COX‑1, trägt zum Schutz der Magenschleimhaut und der Blutplättchen bei. Ältere Schmerzmittel wie Ibuprofen hemmen beide Enzyme, lindern zwar Schmerzen, reizen dabei aber oft den Magen. Celecoxib wurde so entworfen, dass es in eine etwas größere Tasche passt, die vorwiegend in COX‑2 vorkommt, und so Schmerzs Signale blockiert, während die schützende Funktion von COX‑1 weitgehend erhalten bleibt. Das genaue Verständnis der Form dieser Tasche und wie Wirkstoffmoleküle sich in ihr platzieren, ist zentral für die Entwicklung neuer Medikamente, die sowohl wirksam als auch sicher sind.
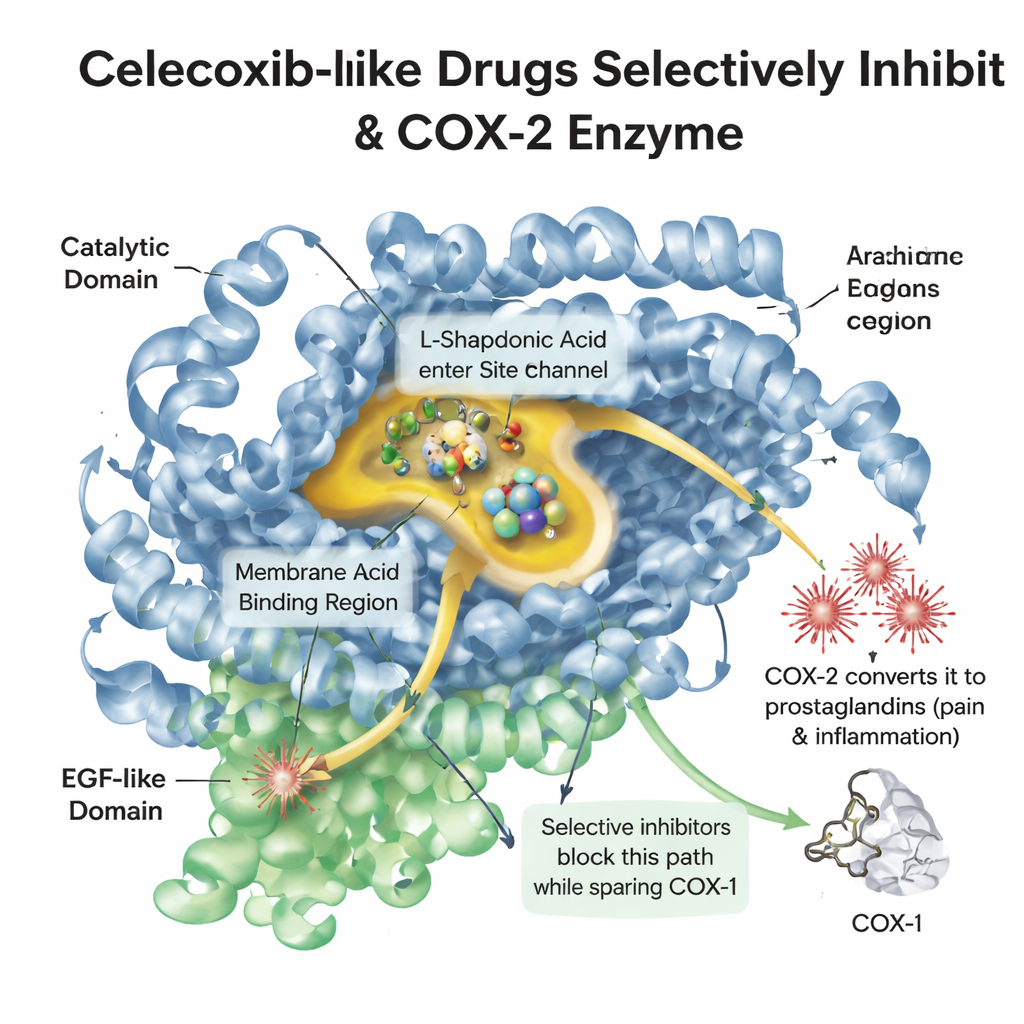
Eine digitale Bibliothek ähnlicher Wirkstoffe
Die Forscher stellten einen Satz von 375 Molekülen zusammen, die alle das grundlegende drei‑Ring‑Gerüst von Celecoxib teilen, sich aber in kleinen Details unterscheiden, etwa durch den Austausch eines einzelnen Atoms oder einer Seitenkette. Sie entnahmen diese Strukturen und ihre gemessenen COX‑2‑Hemmkraftwerte einer öffentlichen Wirkstoffdatenbank. Mit Chemie‑Software erzeugten sie 3D‑Modelle jedes Moleküls, berechneten fast 2.000 numerische Deskriptoren zu Form und Eigenschaften und setzten die Moleküle dann in eine hochaufgelöste Struktur des COX‑2‑Enzyms ein (Docking). Beim Docking schiebt der Computer ein Molekül auf viele Arten in die Tasche des Enzyms und bewertet, wie gut jede Lage passt.
Was wirklich Potenz und Selektivität steuert
Das Team fokussierte sich auf drei Schlüsselregionen von Celecoxib. „Site‑1“ ist ein Ring, der in einer fettigen Zone der Tasche sitzt; „Site‑2“ ist ein Ring mit einem fluorreicheren Schwanz; und „Site‑3“ ist ein Ring mit einer Sulfonamid‑Gruppe, die starke Wasserstoffbrücken bildet. Ihre Analyse zeigte, dass Site‑1 kleine, unpolare Gruppen bevorzugt, die hydrophobe Kontakte erhalten; macht man diesen Bereich etwa durch Hinzufügen einer –OH‑ oder einer Säuregruppe wasserliebender, schwächt das in der Regel das Medikament. An Site‑2 schärften kleine elektronegative Gruppen wie Fluor häufig die Potenz, indem sie Interaktionen in einer engen Tasche verbesserten, während voluminösere oder polarere Enden tendenziell die Aktivität schadeten. An Site‑3 war Stickstoff der Sulfonamid‑Gruppe, der eine Wasserstoffbrücke spenden kann, entscheidend; sein Ersetzen durch eine nicht‑bindende Variante reduzierte die Bindung spürbar.
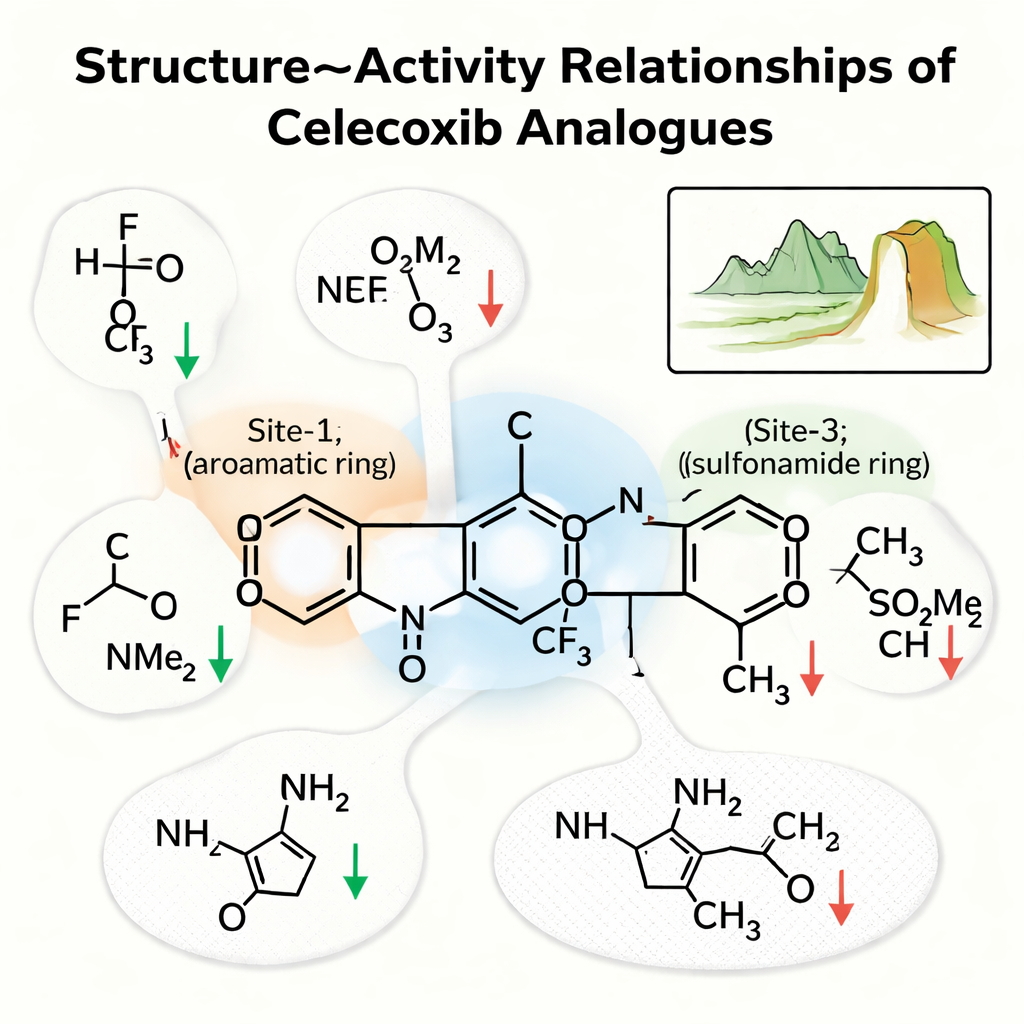
Klippen in der chemischen Landschaft
Um über einfache Trends hinauszugehen, bauten die Autoren eine „Struktur–Aktivitäts‑Landschaft“ auf, die fragt, wie stark die Wirksamkeit springt, wenn sich die Struktur nur wenig ändert. In dieser Darstellung liegen die meisten Celecoxib‑artigen Verbindungen auf sanften Hügeln: Feine Anpassungen — etwa das Verschieben eines Halogens oder das Hinzufügen einer kleinen flexiblen Gruppe — verändern die Potenz vorhersehbar etwas nach oben oder unten. Einige Paare bilden jedoch scharfe „Aktivitätsklippen“, bei denen eine winzige Änderung, wie der Austausch einer Methylgruppe gegen eine Trifluormethylgruppe oder das Hinzufügen eines einzelnen Fluoratoms, einen dramatischen Gewinn oder Verlust an Aktivität verursacht. Die Studie führte außerdem vollständige molekulare Dynamik‑Simulationen durch — virtuelle Filme von Wirkstoff‑Enzym‑Komplexen in Bewegung — die bestätigten, dass die besten Analoga über Hunderttausende von Nanosekunden stabil in der Tasche sitzen.
Wegweiser für die nächste Generation sicherer Schmerzmittel
Für Nicht‑Spezialisten lautet die Kernbotschaft: In der Wirkstoffentwicklung zählen kleine Details enorm. Zwei Verbindungen, die auf dem Papier fast identisch aussehen, können sich darin unterscheiden, wie stark sie COX‑2 hemmen — um das Tausendfache — einfach weil ein zusätzliches Atom die Passform in einer mikroskopischen Tasche verbessert oder einen wichtigen Kontakt stört. Indem diese Berechnungsarbeit systematisch kartiert, welche Änderungen an jedem der drei Schlüssel‑Sites von Celecoxib helfen oder schaden, und indem sie die gefährlichen „Klippen“ hervorhebt, an denen winzige Änderungen überproportionale Effekte haben, liefert sie Chemikern eine Roadmap. Sie weist in Richtung neuer entzündungshemmender Medikamente, die die schmerzlindernde Wirkung von Celecoxib bewahren und gleichzeitig Sicherheit und Selektivität weiter verbessern.
Zitation: Grewal, S., Ghosh, B., Narayan, U. et al. Computational strategies for unraveling insights from known inhibitors for further lead optimization: A case study on Celecoxib analogues. Sci Rep 16, 6720 (2026). https://doi.org/10.1038/s41598-026-37798-z
Schlüsselwörter: COX‑2‑Inhibitoren, Celecoxib‑Analoga, entzündungshemmende Arzneimittel, computergestützte Wirkstoffentwicklung, Struktur‑Aktivitäts‑Beziehungen