Clear Sky Science · de
Vorläufige Bewertung von Biodistribution und Zielgenauigkeit der fluoreszierenden molekularen Sonde Cy7-SYL3C in einem EpCAM-positiven kolorektalen Krebs-Mausmodell
Warum das für die Krebsfrüherkennung wichtig ist
Kolorektaler Krebs gehört zu den weltweit tödlichsten Krebsarten, teilweise weil viele Tumoren spät entdeckt werden. Das derzeit wichtigste Screening-Instrument, die Koloskopie, ist zwar wirksam, aber invasiv und unangenehm, weshalb viele Menschen sie vermeiden. Diese Studie untersucht eine neue Art von leuchtendem „intelligenten Tracer“, der Ärzten eines Tages helfen könnte, Darmtumoren früher und klarer zu sehen – mit Licht statt mit Skalpell oder langem Schlauch.
Ein leuchtender Marker, der Tumorzellen erkennt
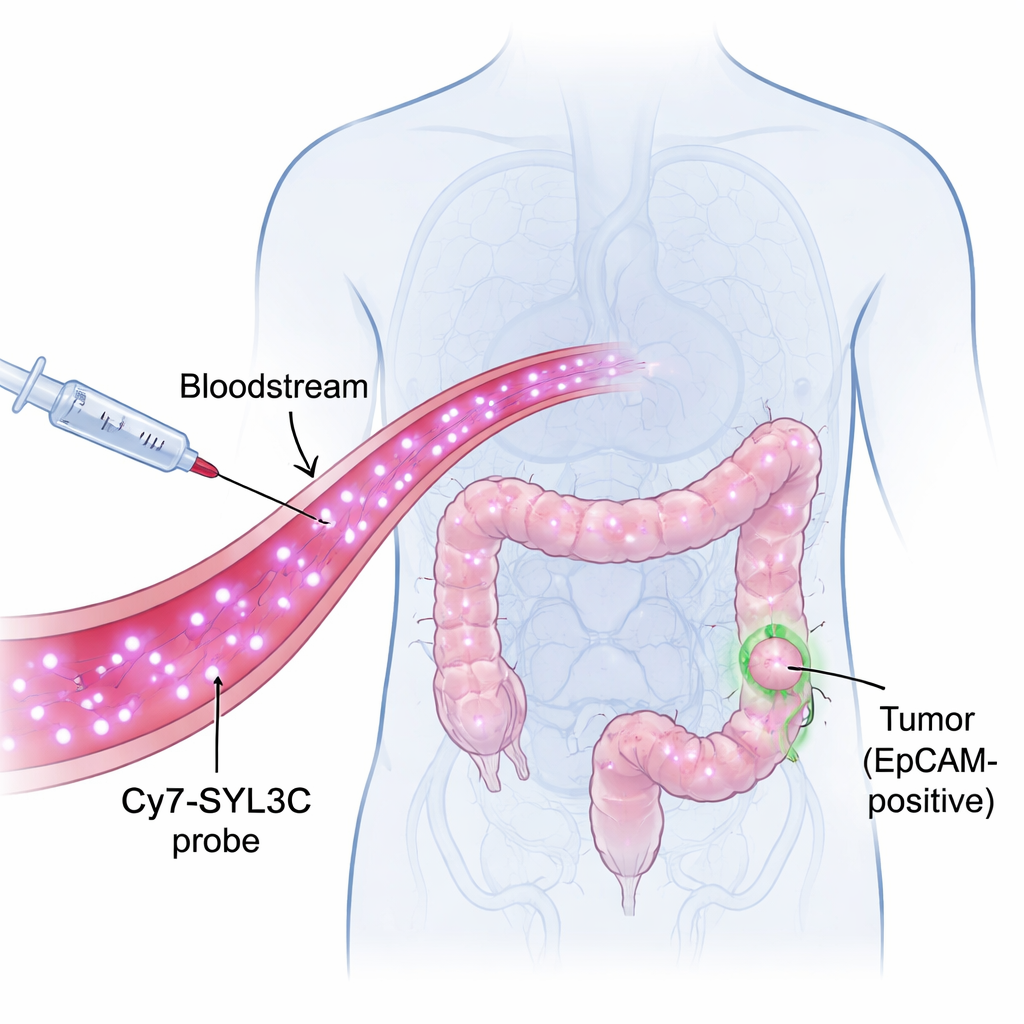
Die Forscher konzentrierten sich auf ein Molekül namens EpCAM, das auf der Oberfläche vieler kolorektaler Krebszellen sitzt, aber in gesundem Gewebe selten vorkommt. Sie entwickelten eine Sonde namens Cy7-SYL3C, indem sie einen nahinfraroten Farbstoff (Cy7) an einen kurzen DNA-Strang namens Aptamer (SYL3C) hängten, der EpCAM erkennen kann – ähnlich wie ein Schlüssel, der in ein Schloss passt. Nahinfrarotes Licht ist für das Auge unsichtbar, kann aber einige Millimeter in Gewebe eindringen, sodass Kameras Signale aus dem Körperinneren mit hohem Kontrast erfassen können. Die Idee ist einfach: Cy7-SYL3C in den Blutkreislauf injizieren, die Sonde EpCAM-reiche Tumorzellen aufsuchen lassen und dann mit einer speziellen Kamera diese Zellen auf dunklem Hintergrund aufleuchten sehen.
Sicherheits- und Stabilitätstests im Labor
Bevor die Sonde in lebenden Tieren getestet wurde, prüfte das Team, ob sie stabil und sicher ist. Sie mischten Cy7-SYL3C mit Blutserum von Mäusen und Rindern und stellten fest, dass der Großteil der Sonde mindestens acht Stunden lang intakt blieb, also lange genug für bildgebende Verfahren während eines medizinischen Eingriffs. Anschließend setzten sie menschliche kolorektale Krebszellen und normale Darmzellen verschiedenen Sondenkonzentrationen aus. Das Zellwachstum blieb im Wesentlichen unverändert, und beim Mischen der Sonde mit roten Blutkörperchen kam es nicht zu einer Auflösung dieser Zellen. Diese Tests deuten darauf hin, dass Cy7-SYL3C sowohl chemisch stabil als auch zellschonend ist – wichtige Anforderungen für jeden Bildgebungsstoff, der bei Patienten eingesetzt werden könnte.
Wohin die Sonde im Körper gelangt
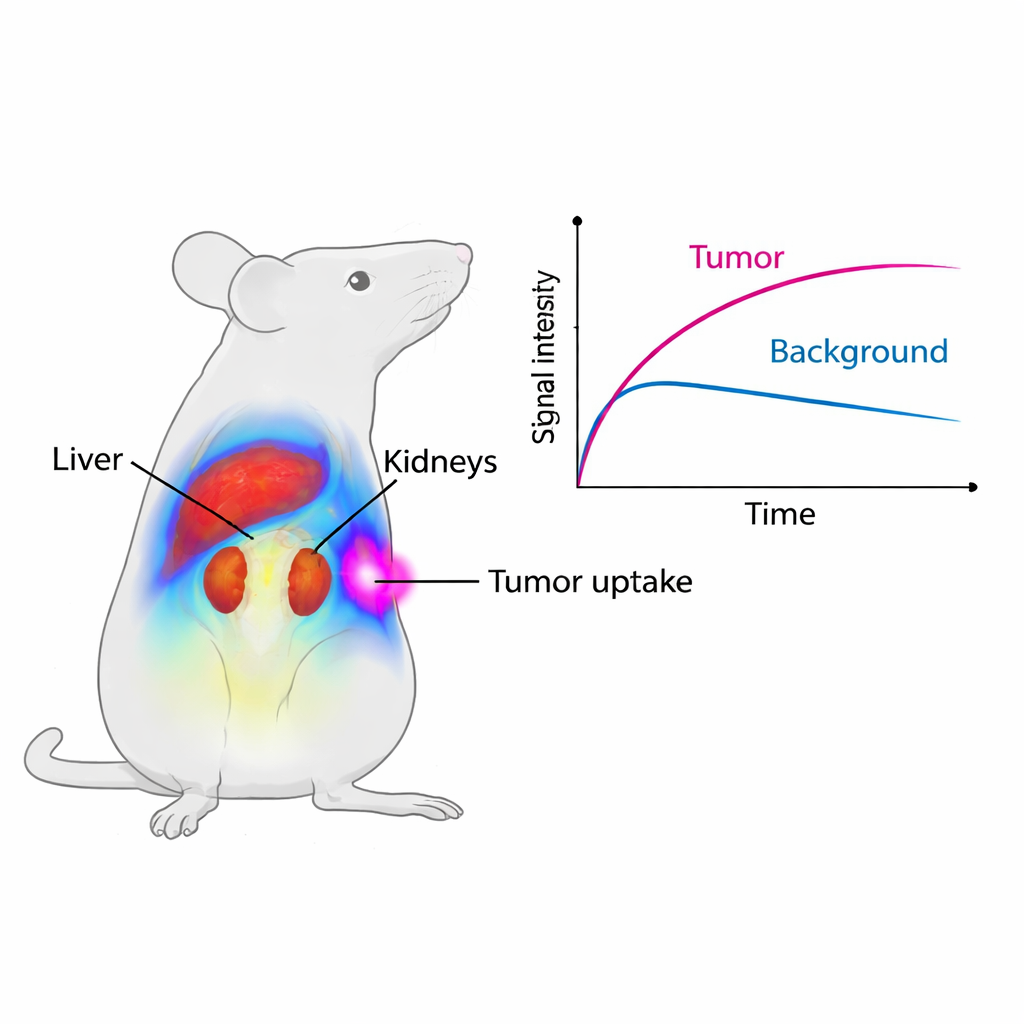
Die Wissenschaftler verfolgten anschließend den Weg von Cy7-SYL3C in gesunden Mäusen mithilfe eines Klein-Tier-Bildgebungssystems. Kurz nach der Injektion zeigte sich das stärkste Signal in Leber und Nieren, Organen, die Substanzen aus dem Blut filtern und ausscheiden. Das Lebersignal erreichte etwa nach einer Stunde seinen Höhepunkt und verblasste dann, während die Nieren länger leuchteten, was auf den Urin als Hauptexkretionsweg der Sonde hinweist. Nach zwei Tagen blieb nur ein kleiner Bruchteil des ursprünglichen Signals übrig, und die mikroskopische Untersuchung der wichtigsten Organe zeigte keine offensichtlichen Gewebeschäden. Das bedeutet, dass die Sonde relativ schnell ausgeschieden wird und in dieser Kurzzeitstudie keine sichtbaren Schäden an lebenswichtigen Organen verursacht.
Gezielte Anreicherung in kolorektalen Tumoren
Um zu prüfen, ob Cy7-SYL3C wirklich Tumoren ansteuert, verwendete das Team Mäuse mit implantierten menschlichen kolorektalen Tumoren, die EpCAM exprimieren. Bereits fünf Minuten nach der Injektion begannen die Tumoren im Bildgebungssystem zu leuchten. In den ersten vier Stunden war das mittlere Signal in den Tumoren fast doppelt so stark wie in Mäusen, deren Tumoren zuvor mit einem Überschuss an unlabeled SYL3C „vorab blockiert“ worden waren, wodurch die EpCAM-Stellen vorübergehend besetzt und die Anlagerung der leuchtenden Sonde verhindert wurde. Das Verhältnis von Tumorsignal zu angrenzendem Muskel stieg über den Wert eins und erreichte um etwa acht Stunden seinen Höhepunkt, was bedeutet, dass die Tumoren über ein praktisches Zeitfenster deutlich heller als ihre Umgebung waren. Detaillierte mikroskopische Untersuchungen bestätigten, dass die fluoreszierende Sonde mit der EpCAM-Färbung der Tumorzellen überlappt, während normale Organe wenig bis kein EpCAM zeigten.
Wie dies zukünftige Operationen und Diagnosen lenken könnte
Für Laien lautet die Hauptaussage: Cy7-SYL3C verhält sich wie ein intelligenter Farbstoff, der kolorektale Krebszellen aufsucht und anschließend größtenteils über die Nieren ausgeschieden wird. Die Sonde scheint stabil, zellverträglich und in der Lage zu sein, Tumoren schnell und für mehrere Stunden zum Leuchten zu bringen. Das könnte Chirurgen helfen, Tumorränder in Echtzeit klarer zu sehen, oder Radiologen unterstützen, verdächtige Bereiche bei minimalinvasiven Eingriffen zu erkennen. Obwohl diese Ergebnisse aus frühen Mausexperimenten stammen und vor einer Anwendung beim Menschen weitere Arbeiten nötig sind, legt die Studie wichtige Grundlagen für eine neue Klasse lichtbasierter Tracer, die die Entdeckung und Operation von kolorektalem Krebs präziser und weniger invasiv machen könnten.
Zitation: Li, Y., Li, M., Li, P. et al. Preliminary assessment of biodistribution and targeting of the fluorescent molecular probe Cy7-SYL3C in an EpCAM-positive colorectal cancer mouse model. Sci Rep 16, 6589 (2026). https://doi.org/10.1038/s41598-026-37787-2
Schlüsselwörter: Bildgebung bei kolorektalem Krebs, Nahinfrarot-Fluoreszenz, EpCAM-Zielsteuerung, Aptamer-Sonde, Leitung von Tumoroperationen