Clear Sky Science · de
SIRT3 unterdrückt das Fortschreiten von Nierenkrebs durch Regulation der Acetylierung von IDH2
Warum diese Studie zu Nierenkrebs wichtig ist
Nierenkrebs, insbesondere eine Form namens Nierenzellkarzinom, wird immer häufiger und ist oft schwer zu behandeln, sobald er metastasiert. Diese Studie schaut in die Mechanik der Krebszellen, um zu verstehen, wie kleine Veränderungen in ihren Energiezentralen, den Mitochondrien, das Tumorwachstum fördern — und wie eine natürliche Pflanzenverbindung, Honokiol, dieses Wachstum möglicherweise verlangsamen kann. Für Leser liefert sie einen Einblick, wie das Verständnis der zellulären „Haushaltung“ neue Optionen jenseits der aktuellen Medikamente eröffnen könnte.
Eine verborgene Bremse in Nierenzellen
Unsere Zellen steuern ständig Energieproduktion und schädliche Nebenprodukte. In gesunden Nierenzellen wirkt ein Protein namens SIRT3 wie ein Wartungsleiter in den Mitochondrien und hält andere Proteine funktionsfähig. Die Autorinnen und Autoren werteten große öffentliche Krebsdatenbanken und Patientenproben aus und fanden, dass SIRT3-Spiegel in Nierentumoren durchgängig niedriger waren als im umliegenden Normalgewebe. Tumoren mit besonders wenig SIRT3 zeigten Genmuster, die mit schnellerem Wachstum und erhöhter Beweglichkeit verknüpft sind, was darauf hindeutet, dass mit dem Verlust dieser zellulären Bremse Krebszellen aggressiver werden.
Wie Krebszellen ihr Energiegleichgewicht verdrehen
Um zu prüfen, ob der Verlust von SIRT3 tatsächlich krebsfördernd ist, reduzierten die Forschenden SIRT3 in in Zelllinien von Nierenkrebs, die im Labor gezüchtet wurden. Zellen mit weniger SIRT3 teilten sich schneller und bildeten deutlich mehr Kolonien — ein Zeichen für gesteigertes Überleben und Wachstum. Wurden diese veränderten Zellen in Mäuse implantiert, entstanden größere und schwerere Tumoren als bei Kontrollzellen. Zusammen zeigen diese Experimente, dass SIRT3 in Nierenkrebs nicht nur fehlt, sondern aktiv das Tumorwachstum bremst, wenn es vorhanden ist.
Ein Schlüsselenzym und das Problem des zellulären „Rosts"
Das Team richtete dann den Fokus auf ein anderes mitochondriales Protein, IDH2, das bei der Produktion von NADPH hilft — einem Molekül, das Entgiftungssysteme für reaktive Sauerstoffspezies (ROS) antreibt, also schädliche Chemikalien, die man als zellulären „Rost“ ansehen kann. Das Verhalten von IDH2 kann durch eine kleine chemische Markierung, eine Acetylgruppe, verändert werden. SIRT3 ist dafür bekannt, solche Markierungen zu entfernen. In Nierenkrebszellen band SIRT3 physisch an IDH2 und entfernte Acetylgruppen an einer spezifischen Position (K413). Wenn SIRT3 reduziert war, häufte sich diese Acetylmarke, IDH2 arbeitete weniger effizient, NADPH-Werte fielen und ROS stiegen. Mitochondrien verloren einen Teil ihres Membranpotenzials, ein Hinweis auf beeinträchtigte Funktion. Mit gentechnisch veränderten IDH2-Varianten, die entweder den acetylierten oder deacetylierten Zustand nachahmten, zeigten die Autorinnen und Autoren, dass die acetylierte Form SIRT3s wachstumshemmende Wirkung außer Kraft setzen konnte — und verbanden so die Tumorbremse direkt mit diesem einzelnen chemischen Schalter.
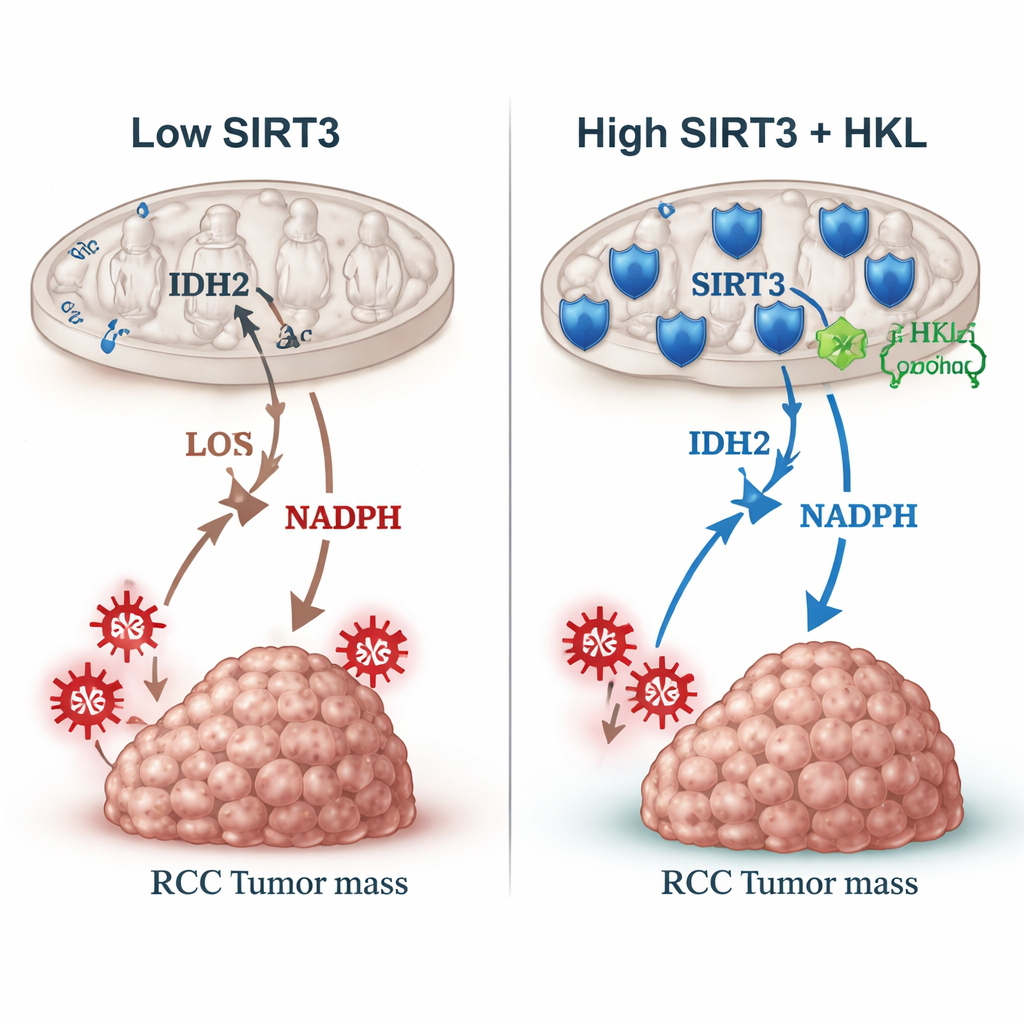
Die Bremse mit einer Pflanzenverbindung wieder einschalten
Weil SIRT3 schützend zu sein scheint, fragten die Forschenden, ob man es mit einem Wirkstoff stärken könnte. Sie testeten Honokiol, ein natürliches Molekül aus Magnolienrinde, das bereits dafür bekannt ist, mehrere Krebswege zu beeinflussen. In einer sorgfältig gewählten Dosis, die die Zellen nicht einfach abtötete, erhöhte Honokiol im Laufe der Zeit die SIRT3-Spiegel in Nierenkrebszellen, zusammen mit verwandten Regulatoren (p-AMPK und PGC-1α). Mit steigendem SIRT3 verlor IDH2 seine Acetylmarke, ROS sanken, und Zellen wuchsen und bildeten Kolonien langsamer. In Kombination mit Sunitinib, einem Standardmedikament gegen Nierenkrebs, unterdrückte die Kombination das Wachstum stärker als Sunitinib allein, teilweise indem sie das überschüssige ROS abschwächte, das Sunitinib selbst induzieren kann. Ähnliche Effekte zeigten sich, wenn die Forschenden ein klassisches Antioxidans einsetzten, was die Idee stützt, dass die Kontrolle des oxidativen Stresses bestehende Behandlungen wirksamer machen kann.
Was das für zukünftige Behandlungen bedeuten könnte
Für Nicht-Fachleute lautet die Kernaussage: Diese Studie identifiziert SIRT3 als natürliche Tumorbremse bei Nierenkrebs, die über die feine Kontrolle von IDH2 und das Gleichgewicht zwischen schützenden und schädlichen Molekülen in den Mitochondrien wirkt. Bei niedrigem SIRT3 häufen sich schädigende ROS an und Zellen erlangen einen Wachstumsvorteil. Die Wiederherstellung der SIRT3-Aktivität — möglicherweise mit Honokiol oder künftigen, präziseren Wirkstoffen — könnte das Tumorwachstum verlangsamen und bestehende Therapien verbessern. Obwohl Honokiol selbst noch Hürden hat, etwa bei der Resorption und seinen multiplen Zielstrukturen, weist die Arbeit auf einen klaren Weg hin — die SIRT3–IDH2–Redox-Achse — den Arzneimittelentwickler nun anvisieren können, um intelligentere, stoffwechselbasierte Behandlungen für das Nierenzellkarzinom zu entwickeln.
Zitation: Li, L., Tian, Y., Chen, S. et al. SIRT3 suppresses renal cancer progression by regulating IDH2 acetylation. Sci Rep 16, 7619 (2026). https://doi.org/10.1038/s41598-026-37783-6
Schlüsselwörter: Nierenkrebs, SIRT3, Mitochondrien, oxidativer Stress, Honokiol