Clear Sky Science · de
Krebsklassifikation mit Radiomics in kontrollierten präklinischen Modellen
Krebs aus Scans und Blut lesen
Die moderne Krebsversorgung verlässt sich zunehmend auf Computer, die medizinische Bilder und Laborwerte nach Mustern durchsuchen, die Menschen kaum erkennen können. Diese Studie stellt eine einfache, aber wichtige Frage: Wenn wir feststellen wollen, um welche Krebsart es sich handelt, ist es besser, versteckte Informationen aus den Scans oder aus dem Blut zu lesen? Anhand sorgfältig kontrollierter Experimente an Mäusen verglichen die Forschenden diese beiden Ansätze direkt, um herauszufinden, welcher von ihnen verlässlichere Antworten liefert.
Was es bedeutet, eine „virtuelle Biopsie“ zu nehmen
Radiomics ist eine schnell wachsende Technik, die jeden medizinischen Scan als reichhaltige Datenquelle statt nur als Bild betrachtet. Spezielle Software durchsucht dreidimensionale CT-Aufnahmen eines Tumors und wandelt sie in Hunderte numerischer Merkmale um, die Form, Helligkeit und feine Texturmuster beschreiben. Grundsätzlich könnten diese Muster die Biologie des Tumors ähnlich wie eine Biopsie widerspiegeln, aber ohne Nadeln oder Operation — eine sogenannte „virtuelle Biopsie“. Befürworter hoffen, dass Radiomics dabei hilft, Tumoren zu klassifizieren, ihre Aggressivität einzuschätzen und Behandlungsentscheidungen zu leiten. Es gibt jedoch Bedenken: Ergebnisse lassen sich oft schwer reproduzieren, sind leicht durch technische Eigenheiten verfälschbar und für Ärztinnen und Ärzte schwer zu interpretieren.
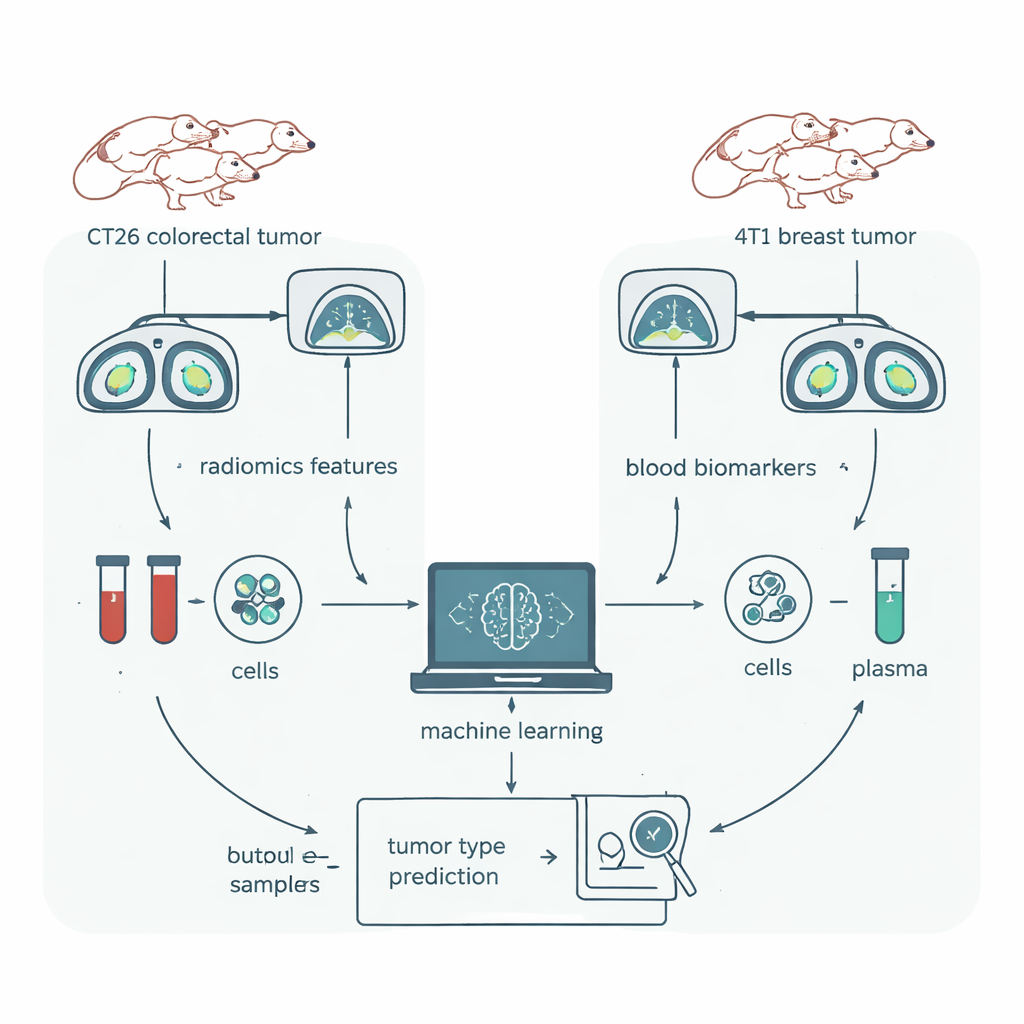
Ein fairer Kopf‑an‑Kopf‑Vergleich in Mäusen
Um Radiomics einem rigorosen Test zu unterziehen, verwendete das Team ein Mausmodell, in dem nahezu alles kontrolliert werden konnte. Gruppen genetisch identischer Mäuse wurden mit einem von zwei Tumortypen implantiert: CT26, ein Modell für kolorektalen Krebs, und 4T1, ein Modell für Brustkrebs. Alle Tiere gehörten derselben Stammlinie an, waren gleiches Geschlechts und ähnlichen Alters, wurden in derselben Umgebung gehalten und auf derselben CT‑Maschine gescannt. Tumoren wurden in einer 3D‑Software sorgfältig umrandet, und ein verbreitetes Radiomics‑Paket extrahierte 1.409 numerische Merkmale aus jedem Scan. Parallel dazu entnahmen die Forschenden Blut aus denselben Tieren und bestimmten Immunzelltypen sowie Dutzende Proteine — Biomarker, die in früheren Arbeiten bereits gezeigt hatten, dass sie diese Krebsmodelle nahezu perfekt unterscheiden können.
Tausende Bilddetails zu einem nutzbaren Signal verdichten
Die meisten Rohbildmerkmale erwiesen sich als wenig hilfreich: Einige variierten kaum von Maus zu Maus, viele waren nahezu Duplikate voneinander. Nach mehreren Runden statistischer Filter blieben nur 18 nicht‑redundante Radiomics‑Merkmale übrig, die überwiegend subtile Texturmuster statt einfacher Größen‑ oder Formmerkmale beschrieben. Das Team nutzte dann ein standardmäßiges Machine‑Learning‑Verfahren, Random Forest, um zu prüfen, wie gut sich diese verfeinerten Bildmerkmale zur Unterscheidung der beiden Tumortypen eignen. Zusätzlich wurden Visualisierungsmethoden angewandt, um zu sehen, ob die Daten ohne Vorwissen natürliche Cluster für die einzelnen Krebsarten bilden.
Blutsignale schlagen Bildsignale
Der Kontrast zwischen Blut- und Bilddaten war auffällig. Als die Forschenden die Daten zu Blutzellen und Plasmaproteinen auf zwei Dimensionen reduzierten, bildeten die beiden Tumortypen klar getrennte Cluster, was bestätigte, dass das Blut starke, tumorspezifische Signale enthielt. In den Radiomics‑Daten dagegen erschienen drei gemischte Cluster, die jeweils eine Mischung aus beiden Krebsarten enthielten und nahelegten, dass andere, unbekannte Faktoren die Bildgebung mitprägten. In überwachten Tests klassifizierte Radiomics allein den Tumortyp mit einer Genauigkeit von etwa 87 Prozent — gut, aber deutlich schlechter als die 96 Prozent Genauigkeit durch Immunzellzählungen und die 99 Prozent Genauigkeit durch Plasmaproteine. Die Hinzunahme von Radiomics zu den Blutmarkern verbesserte die Leistung nicht; in einigen Kombinationen verringerte sie die Genauigkeit sogar leicht. Ein weiterer Versuch zeigte, dass die Verwendung nur einer kleinen kugelförmigen Region innerhalb des Tumors statt der vollständigen Umrandung die Radiomics‑Leistung noch weiter verschlechterte, was unterstreicht, wie empfindlich diese Merkmale gegenüber der Tumorsegmentation sind.
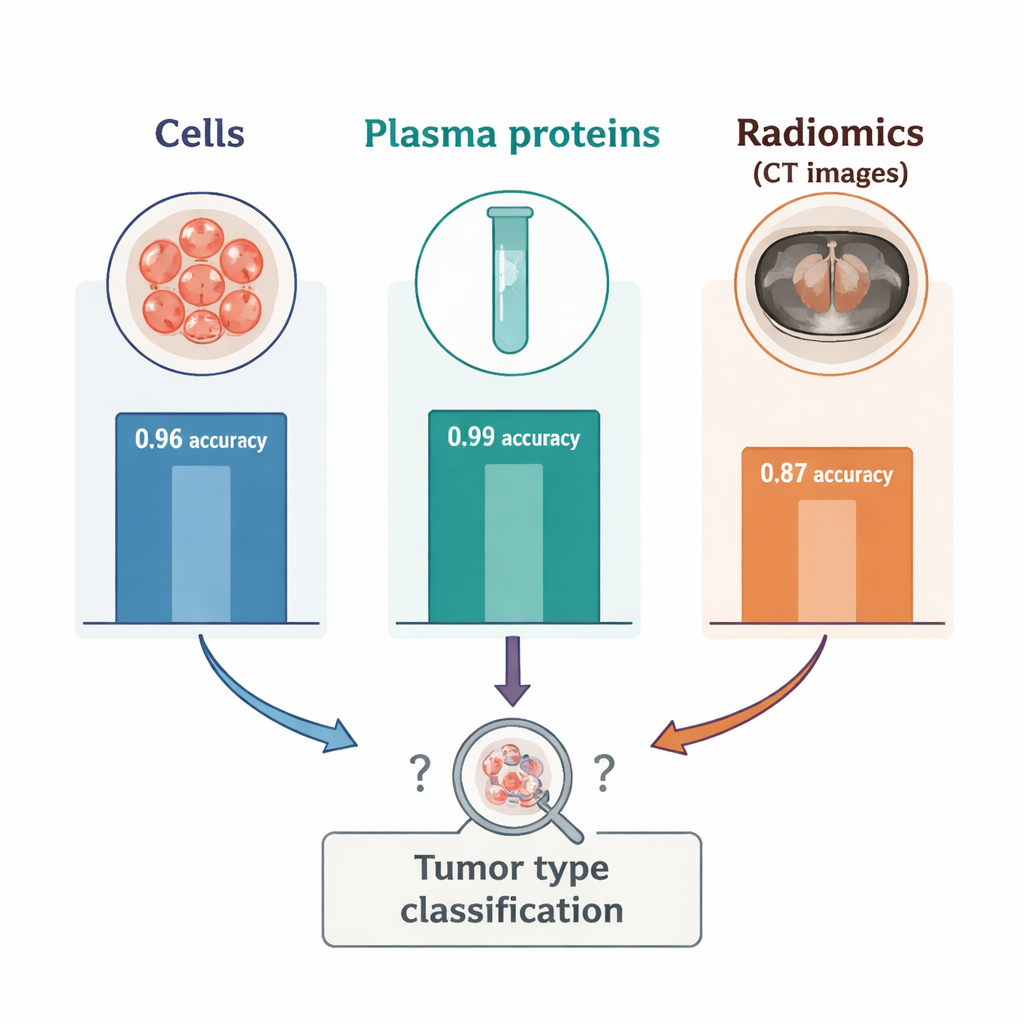
Was das für künftige Krebs‑Tests bedeutet
Für eine allgemeine Leserschaft ist die Erkenntnis klar: Während fortgeschrittene Bildanalyse einige nützliche Hinweise liefern kann, wurde sie in dieser Studie von vergleichsweise einfachen Bluttests beim Unterscheiden zweier Krebsarten übertroffen. Selbst unter streng kontrollierten Laborbedingungen mit identischen Mäusen und standardisierter Bildgebung schienen kleine technische Unterschiede und die Komplexität der Bildverarbeitung das radiomische Signal zu verwischen. Die Autorinnen und Autoren folgern, dass Radiomics noch nicht bereit ist, als eigenständiger, hoch verlässlicher Krebsklassifikator zu dienen. Stattdessen plädieren sie für stärkere Standardisierung der Bildgebung, bessere Konturierungswerkzeuge und klarere Verknüpfungen zwischen Bildmustern und zugrunde liegender Biologie, bevor virtuelle Biopsien zuverlässig klinische Entscheidungen ergänzen oder anstelle bewährter Blutbiomarker treffen können.
Zitation: Drover, K., Davis, D.A.S., Gosling, K. et al. Cancer classification with radiomics in controlled preclinical models. Sci Rep 16, 6647 (2026). https://doi.org/10.1038/s41598-026-37757-8
Schlüsselwörter: Radiomics, Krebs-Biomarker, medizinische Bildgebung, Maschinelles Lernen in der Onkologie, Bluttests für Krebs