Clear Sky Science · de
Multidimensionale Strategie ermöglicht skalierbare Metabolom‑Diversität in mikrobiellen Fermentationen
Warum winzige Fabrik‑Anpassungen für neue Medikamente wichtig sind
Viele der heutigen Medikamente stammen von natürlichen Verbindungen, die Bakterien und Pilze produzieren. Doch aus einem vielversprechenden Fund im Labor einen echten Arzneistoffkandidaten zu machen scheitert oft an einem überraschend banalen Schritt: dem Kultivieren desselben Mikroorganismus in einem anderen Gefäß oder im größeren Maßstab. Diese Studie stellt eine einfache, aber entscheidende Frage – wie lässt sich die chemische Produktion eines Mikrobenstamms stabil und vielfältig halten, wenn man von kleinen Testplatten auf größere Schalen und Bioreaktoren umsteigt? Die Antwort könnte die Suche nach der nächsten Generation von Antibiotika und anderen Therapien beschleunigen.
Drei Wege, denselben Mikroben zu züchten
Die Forschenden konzentrierten sich auf ein Bodenbakterium, Streptomyces griseochromogenes, das dafür bekannt ist, viele „Sekundärmetabolite“ zu produzieren – kleine Moleküle mit Potential als Wirkstoffe. Sie verglichen drei gängige Kultivierungssysteme, die in der frühen Entdeckung verwendet werden: baffle‑Schüttelkolben, 48‑Well‑„Flower“‑Mikrotiterplatten und einen Rührbehälter‑Bioreaktor. In jedem System maßen sie Wachstum, Zellform und -struktur und, entscheidend, das Muster chemischer Signale, detektiert mittels Massenspektrometrie, die hier als Fingerabdruck des sezernierten Metaboloms dient. Zunächst wendeten sie eine klassische ingenieurwissenschaftliche Regel an: gleiche Sauerstoffverfügbarkeit über alle Systeme hinweg und ähnliches Verhalten erwarten. Stattdessen fanden sie, dass Wachstumskurven, Zellformen und chemische Fingerabdrücke von Gefäß zu Gefäß stark unterschiedlich waren.
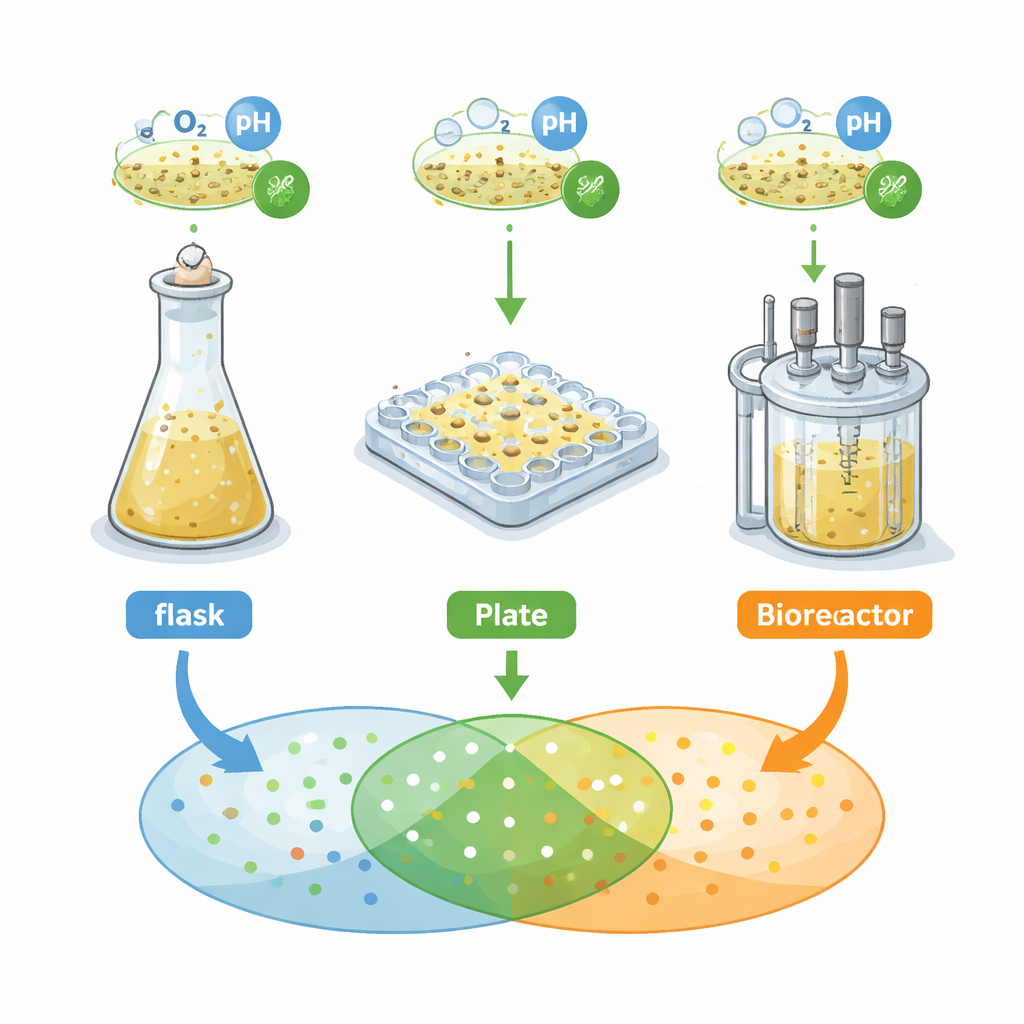
Wenn eine Regel nicht ausreicht
Allein das Angleichen des Sauerstoffs erzeugte sehr unterschiedliche „metabolische Fußabdrücke“ – die Mengen an Massensignalen, die einzelnen Molekülen entsprechen. Nur etwa 18 Prozent dieser Merkmale fanden sich in allen drei Systemen. Die Mikrotiterplatten erzeugten deutlich mehr unterschiedliche Signale als Kolben oder der Bioreaktor. Das Team probierte daraufhin einen anderen eindimensionalen Ansatz, indem es entweder die Menge an Ethanol im Medium veränderte (ein kleines Molekül, das Bakterien zur Bildung bestimmter Metabolite anregen kann) oder die Rührgeschwindigkeit anpasste, die die Sauerstoffzufuhr verändert. Diese eindimensionalen Anpassungen verbesserten die Überschneidung der chemischen Fußabdrücke nur moderat, um etwa weitere 18 Prozent. Anders gesagt: Einfache Rezepte wie „mehr Sauerstoff“ oder „mehr Ethanol“ garantieren nicht, dass ein in einer winzigen Vertiefung entdecktes Metabolit zuverlässig in einem größeren Fermenter auftaucht.
Wie Zellform die chemische Vielfalt lenkt
Um zu ergründen, was wirklich wichtig ist, bündelten die Autorinnen und Autoren Daten aus 80 verschiedenen Kultivierungen und verwendeten eine statistische Methode, die nach verborgenen Einflussfaktoren sucht. Diese Analyse hob zwei zentrale Aspekte hervor: das Kultivierungssystem selbst und die Morphologie der Zellen – ob die Bakterien als kompakte Pellet‑Strukturen, lockere mycelartige Matten oder fein dispergierte Filamente wuchsen. Bedingungen, die ähnliche Morphologien erzeugten, führten tendenziell zu ähnlicheren metabolischen Fußabdrücken und erleichterten das „Hochskalieren“ von Molekülen von kleinen Systemen in den Rührbehälter. Durch die gezielte Auswahl von Bedingungen, die in allen drei Systemen vergleichbare Zellformen erzeugten, erhöhten die Forschenden die Überschneidung der chemischen Merkmale um etwa 50 Prozent gegenüber dem klassischen reinen Sauerstoff‑Abgleich.
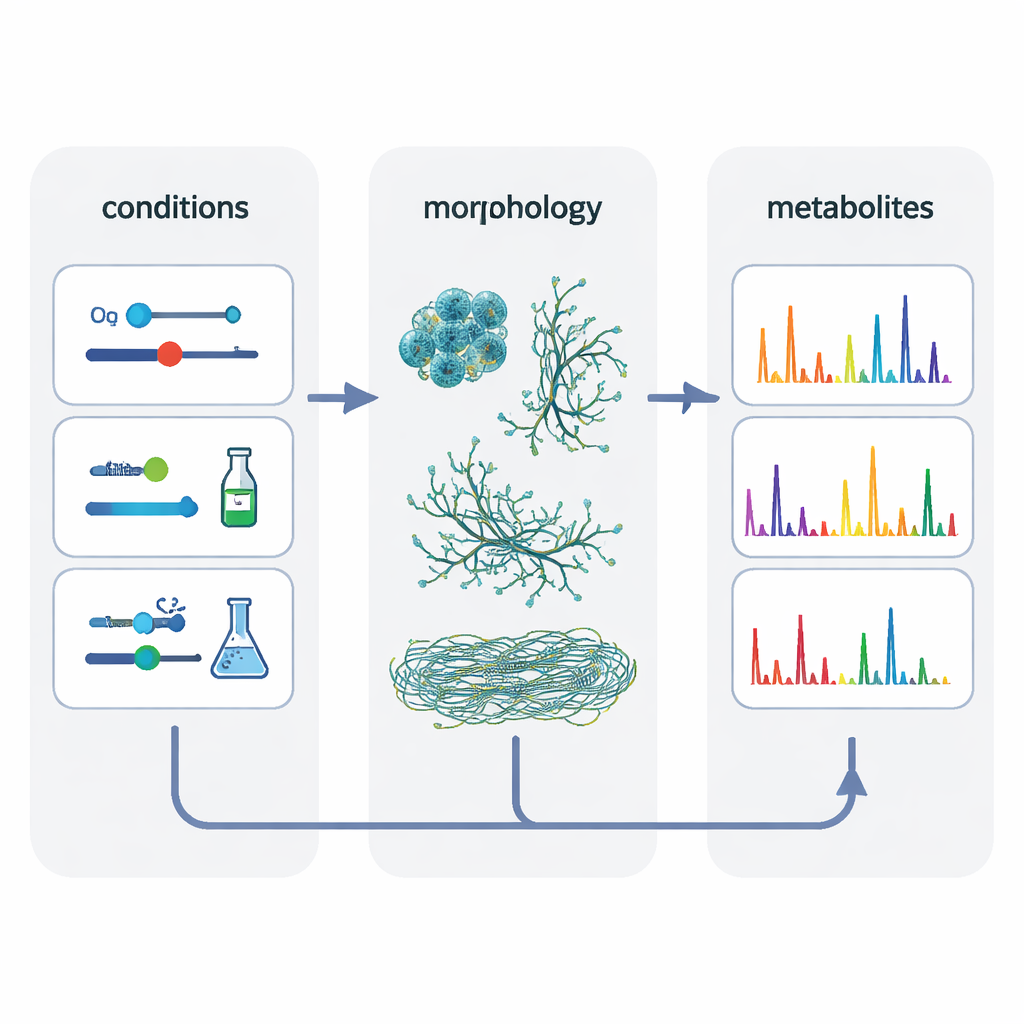
Verborgene chemische Familien und systemspezifische Moleküle
Über einfache Signalzählungen hinaus erstellte das Team molekulare Netzwerke, die verwandte Massensignale in Familien strukturell ähnlicher Metabolite gruppierten. Große Familien enthielten häufig mindestens ein Mitglied, das in jedem Kultivierungssystem vorkam, was auf eine Kernchemie hindeutet, die gegenüber Skalierungsänderungen robust ist. Viele kleinere Familien – und einige einzelne Moleküle – traten jedoch nur in einem Gefäßtyp auf. Die Polystyrol‑Mikrotiterplatten lieferten besonders die reichhaltigste Vielfalt an Verbindungen, einschließlich vieler Varianten von eisenbindenden Siderophoren namens Desferrioxamine und mehrerer non‑ribosomaler Peptide. Die Autorinnen und Autoren vermuten, dass subtile Stressfaktoren in diesen Platten, etwa erhöhte Spiegel reaktiver Sauerstoffspezies, die Bakterien zu einer größeren chemischen Diversifizierung treiben, während der gut durchmischte Bioreaktor eine kleinere Menge „kerniger“ Strukturen begünstigt.
Was das für die Suche nach neuen Naturstoffen bedeutet
Für Teams in der Wirkstoffsuche ist die Botschaft klar: Man kann sich nicht auf eine einzige ingenieurtechnische Regel oder eine „optimale“ Bedingung verlassen, wenn man sowohl große chemische Vielfalt als auch verlässliche Hochskalierung erreichen will. Stattdessen braucht es eine multidimensionale Strategie, die Gefäßtyp, Sauerstofftransfer, Zusätze wie Ethanol und – wichtig – die Echtzeitüberwachung der Zellmorphologie berücksichtigt. Die Verwendung von Mikrotiterplatten, die Schlüsselfeatures von Bioreaktoren nachbilden, und das Abstimmen der Bedingungen, um ähnliche Wachstumsformen zu erzeugen, erhöhen die Wahrscheinlichkeit, dass vielversprechende Moleküle, die im Mikrolitermaßstab entdeckt wurden, auch im Litermaßstab wieder auftreten. Dieser Ansatz hilft, fragile frühe Treffer in robuste, reproduzierbare Kandidaten zu verwandeln und erhöht die Chancen, dass neuartige Naturstoffe den Weg vom Labor bis zur Apotheke überstehen.
Zitation: Lindig, A., Fataeri, M., Hubmann, G. et al. Multidimensional strategy enables scalable metabolome diversity in microbial fermentations. Sci Rep 16, 4084 (2026). https://doi.org/10.1038/s41598-026-37748-9
Schlüsselwörter: Entdeckung natürlicher Produkte, Streptomyces‑Fermentation, Metabolomik, Hochskalierung im Bioreaktor, Sekundärmetabolite