Clear Sky Science · de
Synergistische Zielsteuerung der ARID2–MYC‑Achse durch Pomalidomid und Panobinostat überwindet intrinsische IMiD‑Resistenz beim multiplen Myelom
Warum diese Forschung für Patienten wichtig ist
Das multiple Myelom ist eine Krebsform der antikörperproduzierenden Zellen im Knochenmark, die heute zwar besser behandelbar, aber selten heilbar ist. Viele Patienten sprechen mit der Zeit nicht mehr auf Standardmedikamente an, sodass Ärzten weniger Optionen bleiben. Diese Studie untersucht, warum die Kombination zweier vorhandener Medikamententypen — sogenannter IMiDs wie Pomalidomid und Arzneimittel, die die DNA‑Packung beeinflussen, sogenannte Histon‑Deacetylase(HDAC)‑Inhibitoren wie Panobinostat — zusammenwirken kann, um Myelomzellen zu töten, selbst wenn der Krebs bereits gegen IMiDs allein resistent ist. Das Verständnis dieser Kooperation auf molekularer Ebene könnte bessere Kombinationstherapien leiten und mehr Patienten helfen, von bereits verfügbaren Medikamenten zu profitieren.
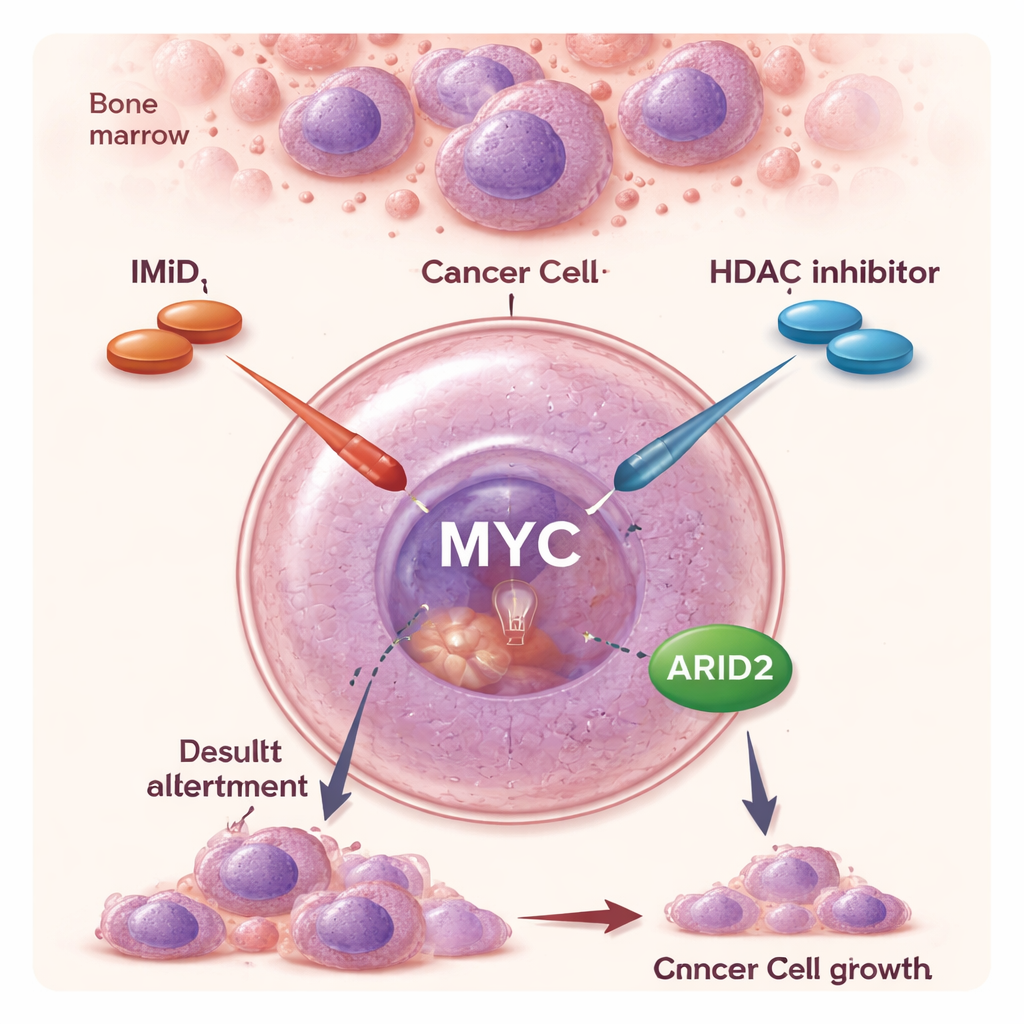
Zwei ältere Wirkstoffklassen, eine neue Partnerschaft
In den vergangenen zwei Jahrzehnten haben IMiDs und andere zielgerichtete Wirkstoffe das Überleben von Menschen mit multiplem Myelom deutlich verlängert. IMiDs wirken auf ungewöhnliche Weise: Anstatt einfach ein Protein zu blockieren, veranlassen sie, dass bestimmte Proteine für den Abbau markiert werden, wodurch sie effektiv aus der Zelle entfernt werden. Dadurch werden zentrale Überlebenssignale, auf die Myelomzellen angewiesen sind, geschwächt. HDAC‑Inhibitoren wie Panobinostat wirken anders: Sie lockern die enge DNA‑Packung und verändern breit, welche Gene ein‑ oder ausgeschaltet sind. Als Einzelsubstanzen haben HDAC‑Inhibitoren nur moderate Effekte und können Nebenwirkungen verursachen, doch klinische Studien deuteten bereits an, dass ihre Kombination mit IMiDs eine deutlich stärkere Anti‑Tumor‑Wirkung erzielt — auch bei Patienten, deren Erkrankung nicht mehr auf IMiDs allein anspricht. Der molekulare Grund für diese Synergie war jedoch lange unklar.
Ein gemeinsamer Druckpunkt: MYC herunterfahren
Die Forschenden testeten systematisch Kombinationen mehrerer IMiDs mit verschiedenen HDAC‑Inhibitoren in einer Reihe von Myelomzelllinien und verwendeten ein standardisiertes Bewertungssystem, um zu messen, wie viel leistungsstärker die Kombinationen im Vergleich zu jedem Einzelmedikament waren. Sie fanden heraus, dass Pomalidomid plus Panobinostat in den meisten Zellmodellen besonders starke Synergie zeigte und dass dieser Effekt von einem Protein namens Cereblon abhing, das IMiDs nutzen, um ihre Zielproteine für den Abbau zu markieren. Durch die Analyse der globalen Genaktivität entdeckte das Team, dass Panobinostat und ein verwandter breitwirkender HDAC‑Inhibitor MYC, ein zentrales Wachstumsgen, das oft als „onkogenes Triebwerk“ in Krebszellen beschrieben wird, stark herunterregulierten, und dass IMiDs zusätzlichen Druck auf denselben Knoten ausübten. Wenn die Wissenschaftler die Myelomzellen zwangen, MYC aus einer gegen das Medikament unempfindlichen Quelle weiter zu produzieren, verschwand der starke Effekt des Wirkstoffpaars größtenteils — ein Hinweis darauf, dass die Abschaltung von MYC zentral für ihre Kooperation ist.
Resistenz durch eine alternative Route knacken
Manche Myelomzellen sind intrinsisch gegen IMiDs resistent: Obwohl die erwarteten frühen Zielproteine abgebaut werden, werden MYC und andere Überlebenssignale nicht ausreichend stillgelegt, sodass die Zellen weiter wachsen. In einem solchen resistenten Modell war der normale IMiD‑Weg, der frühe Ziele mit MYC verbindet, „entkoppelt“. Das Team fragte, ob eine alternative Route IMiDs dennoch mit MYC verbinden könnte. Sie konzentrierten sich auf ARID2, einen Bestandteil einer großen DNA‑Remodelling‑Maschine namens SWI/SNF‑Komplex. Frühere Arbeiten hatten gezeigt, dass Pomalidomid ARID2 markiert und dessen Abbau fördert, was zur Senkung von MYC beiträgt. In resistenten Zellen verringerte Pomalidomid ARID2 nur moderat, teilweise weil die Zelle als Reaktion ihre ARID2‑Produktion hochfuhr. Wurde Panobinostat hinzugefügt, unterdrückte es das ARID2‑Gen selbst und überwand diese Rückkopplungsschleife. Gemeinsam verringerten die beiden Medikamente ARID2‑Protein und anschließend MYC stark, was zu einer potenten Abtötung der Krebszellen auch in IMiD‑resistenten Zelllinien führte.
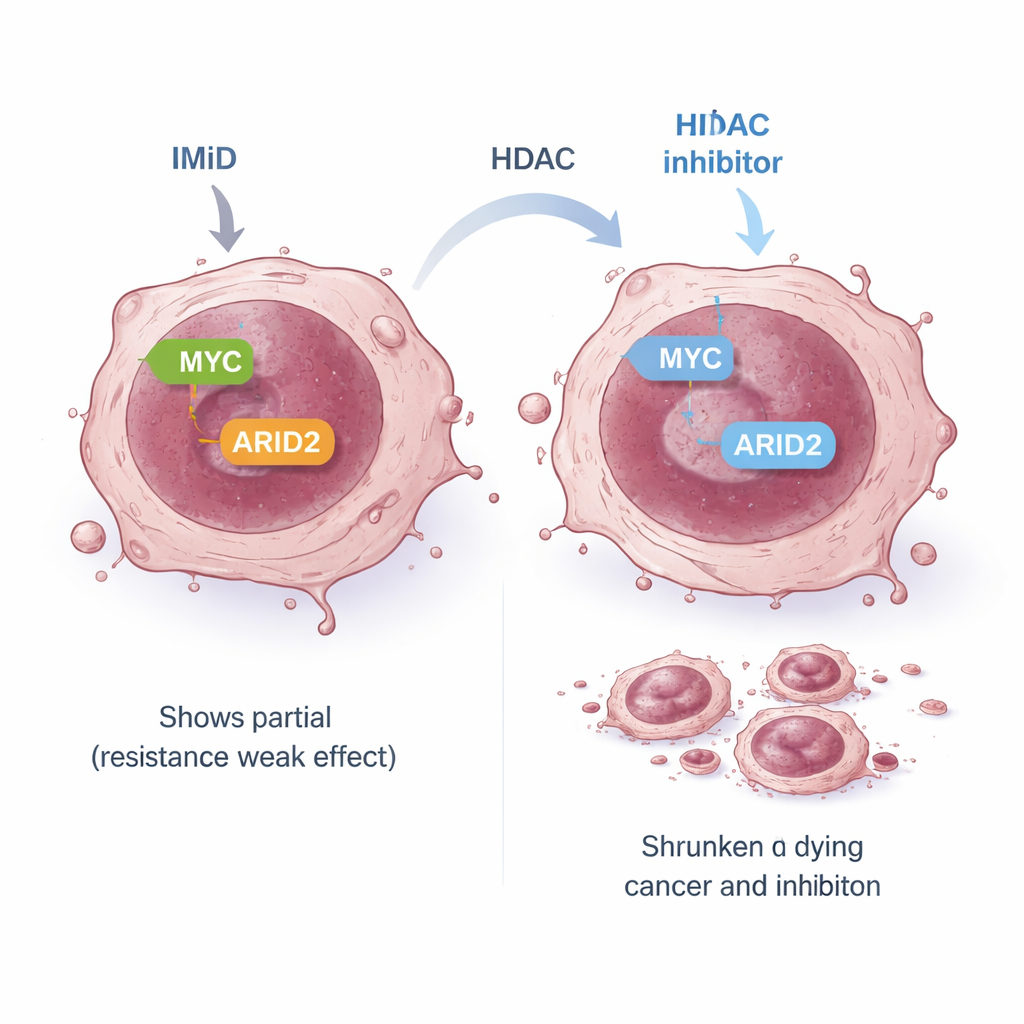
Eine breitere Schwachstelle in Krebszellen offenlegen
Da ARID2 nur ein Mitglied des SWI/SNF‑Komplexes ist, fragten die Autorinnen und Autoren, ob der gesamte Komplex eine therapeutische Schwachstelle sein könnte. Sie fanden heraus, dass HDAC‑Inhibitoren die Spiegel mehrerer SWI/SNF‑Komponenten senken und dass ein separates niedermolekulares Medikament, das darauf abzielt, die Kernmotoren des Komplexes (BRG1/BRM) zu blockieren, allein das Wachstum von Myelomzellen verlangsamen und MYC reduzieren kann. Wichtig ist, dass dieser SWI/SNF‑Inhibitor auch synergetisch mit sowohl Pomalidomid als auch Panobinostat wirkte, und eine Drei‑Medikamenten‑Kombination drückte ARID2 und MYC noch weiter nach unten, während sie die Zellproliferation stark unterdrückte. Durch die Untersuchung, welche spezifischen HDAC‑Enzyme beteiligt sind, hoben die Forschenden HDAC1 als wichtigen Faktor hervor, der die ARID2–MYC‑Achse aufrechterhält, während andere HDACs offenbar MYC über parallele Wege beeinflussen.
Was das für die zukünftige Myelom‑Therapie bedeutet
Für Nicht‑Spezialisten lautet die zentrale Botschaft, dass Myelomzellen offenbar von einem gemeinsamen „Wachstumssteuerungs‑Knoten“ rund um MYC abhängen und dass es mehr als einen Weg gibt, der in diesen Knoten führt. Die Standard‑IMiD‑Therapie trifft hauptsächlich einen dieser Wege; in manchen resistenten Tumoren ist dieser Weg blockiert, sodass MYC aktiv bleibt. Diese Studie zeigt, dass eine alternative Route — über ARID2 und den SWI/SNF‑Komplex — offen bleibt und dass die Kombination von Panobinostat mit Pomalidomid sie schließen kann. Durch gezielte Kombination von Medikamenten, die MYC aus mehreren Richtungen unter Druck setzen, könnten Kliniker einige Formen angeborener Medikamentenresistenz überwinden und möglicherweise niedrigere Dosen der einzelnen Wirkstoffe einsetzen. Obwohl weitere präklinische und klinische Studien nötig sind, liefern die Befunde eine klarere Vorlage für die Entwicklung klügerer, mechanismusbasierter Kombinationen für Patienten mit schwer behandelbarem multiplem Myelom.
Zitation: Yamamoto, J., Asatsuma-Okumura, T., Ito, T. et al. Synergistic targeting of the ARID2–MYC axis by pomalidomide and panobinostat overcomes intrinsic IMiD resistance in multiple myeloma. Sci Rep 16, 7375 (2026). https://doi.org/10.1038/s41598-026-37740-3
Schlüsselwörter: multiples Myelom, Medikamentenresistenz, Pomalidomid, Panobinostat, MYC