Clear Sky Science · de
Mechanismus und evolutionäre Divergenz eines neuartigen oxidierten Polyvinylalkohol-Hydrolase in Stenotrophomonas rhizophila QL-P4
Warum ein vermeintlich „grüner“ Kunststoff trotzdem in der Natur verbleibt
Polyvinylalkohol, kurz PVA, findet sich in allem von Waschmittelkapseln bis zu Textilbeschichtungen und Papier. Er wird oft als umweltfreundlich beworben, weil Mikroben ihn theoretisch abbauen können. In echten Flüssen, Böden und Meeren zerfällt dieses kunststoffähnliche Material jedoch sehr langsam und kann als Mikro- und Nanoplastikfragmente jahrzehntelang bestehen bleiben. Diese Studie betrachtet eines der natürlichen Werkzeuge gegen PVA genauer: ein neu entdecktes Enzym aus einem Bodenbakterium, das dieses hartnäckige Polymer in kleinere, weniger schädliche Stücke zerlegen kann.
Ein kleiner Helfer aus dem Boden mit großer Aufgabe
Forscher isolierten zuvor das Bakterium Stenotrophomonas rhizophila QL-P4 aus Bergboden in China und stellten fest, dass es mit PVA als Nahrungsquelle wachsen kann. In der neuen Arbeit konzentrierten sie sich auf ein einzelnes Verdächtigen-Gen, BAY15_0160, das so aussah, als könne es für ein Enzym kodieren, das oxidierten PVA spaltet. Durch gezieltes Entfernen dieses Gens, Wiedereinfügen und Überexpression zeigten sie, dass BAY15_0160 für einen effizienten PVA-Abbau unerlässlich ist. Beim Entfernen des Gens verlor das Mikroorganismus etwa 40 % seiner Fähigkeit, PVA zu verwerten; das Wiederherstellen des Gens brachte die Leistung zurück und bestätigte, dass sein Produkt eine Schlüsselrolle im Abbauweg spielt.
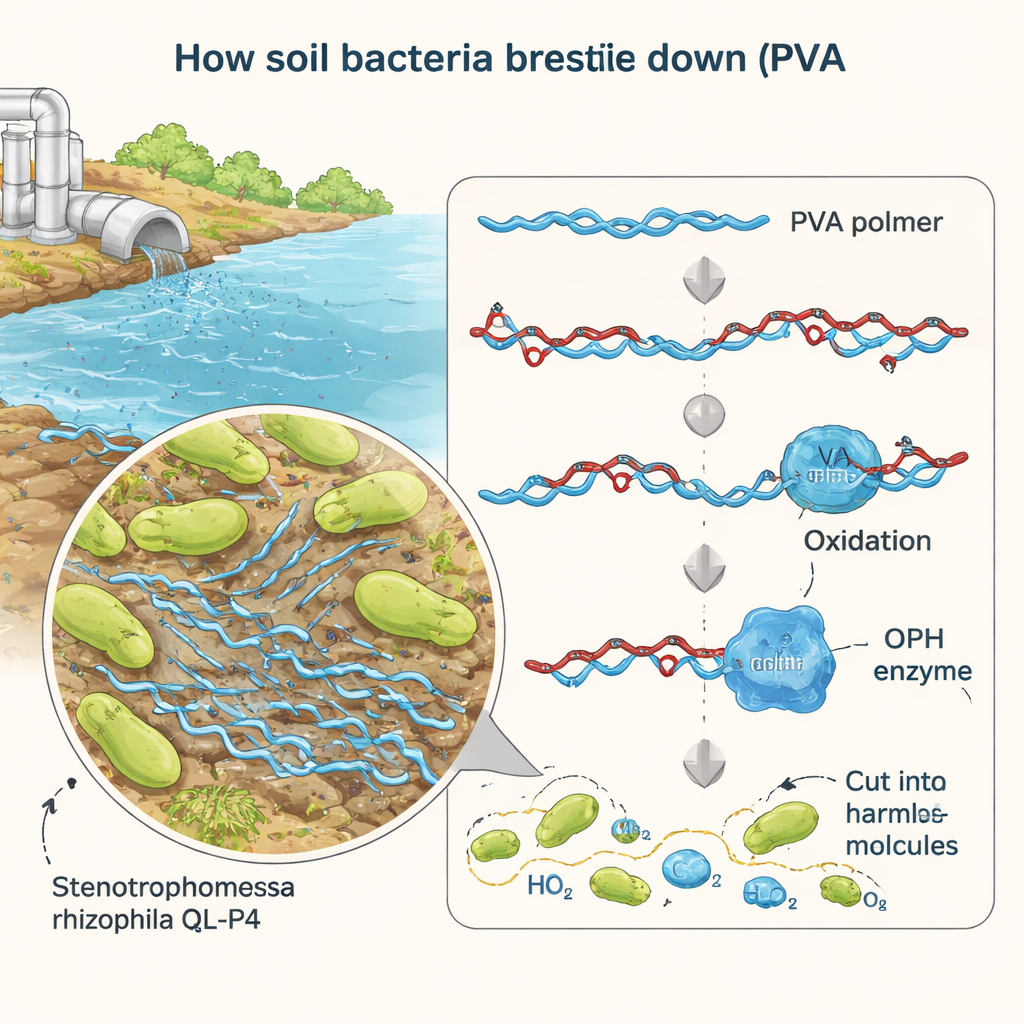
Wie das Enzym seine Arbeit misst
Um das Enzym im Detail zu untersuchen, stellten die Forscher es in großen Mengen mithilfe von Laborstämmen von Escherichia coli her. Sie reinigten das Protein, das sich als etwa 35 Kilodalton groß erwies, und testeten seine Aktivität unter verschiedenen Bedingungen. Mit einem einfachen Testsubstrat, das bei Spaltung einen gelben Farbstoff freisetzt, verfolgten sie, wie schnell das Enzym bei unterschiedlichen Temperaturen und pH-Werten arbeitet. Das Enzym war am aktivsten bei rund Raumtemperatur (30 °C) und bei neutralem pH, ähnlich dem vieler natürlicher Gewässer. Unter diesen milden Bedingungen zeigte es eine hohe katalytische Effizienz, das heißt, jedes Enzymmolekül kann pro Sekunde viele Substratmoleküle verarbeiten — ermutigende Nachrichten für mögliche praktische Reinigungsanwendungen.
Ein Blick auf die molekularen Scheren
Enzyme sind die winzigen Maschinen der Natur, und ihre Form bestimmt, was sie leisten können. Die Forscher nutzten moderne Vorhersageprogramme, RoseTTAFold und AlphaFold, um dreidimensionale Modelle des PVA-spaltenden Enzyms zu erstellen, das nun als neuartige oxidierte PVA-Hydrolase (OPH) anerkannt ist. Beide Werkzeuge kamen zu dem Ergebnis, dass das Enzym die klassische „Alpha/Beta-Hydrolase“-Faltung besitzt, die bei vielen biologischen Scheren zu finden ist. Im Zentrum liegt ein kurzes Motiv — häufig als Gly–X–Ser–X–Gly angegeben — das hilft, ein Trio von Aminosäuren (Serin, Asparat und Histidin) so zu positionieren, dass sie chemische Bindungen angreifen. Computersimulationen zeigten, wie oxidierte PVA-Fragmente in diese Rinne passen, wobei das Schlüsselserin wahrscheinlich den ersten Schnitt in der Kette vornimmt.
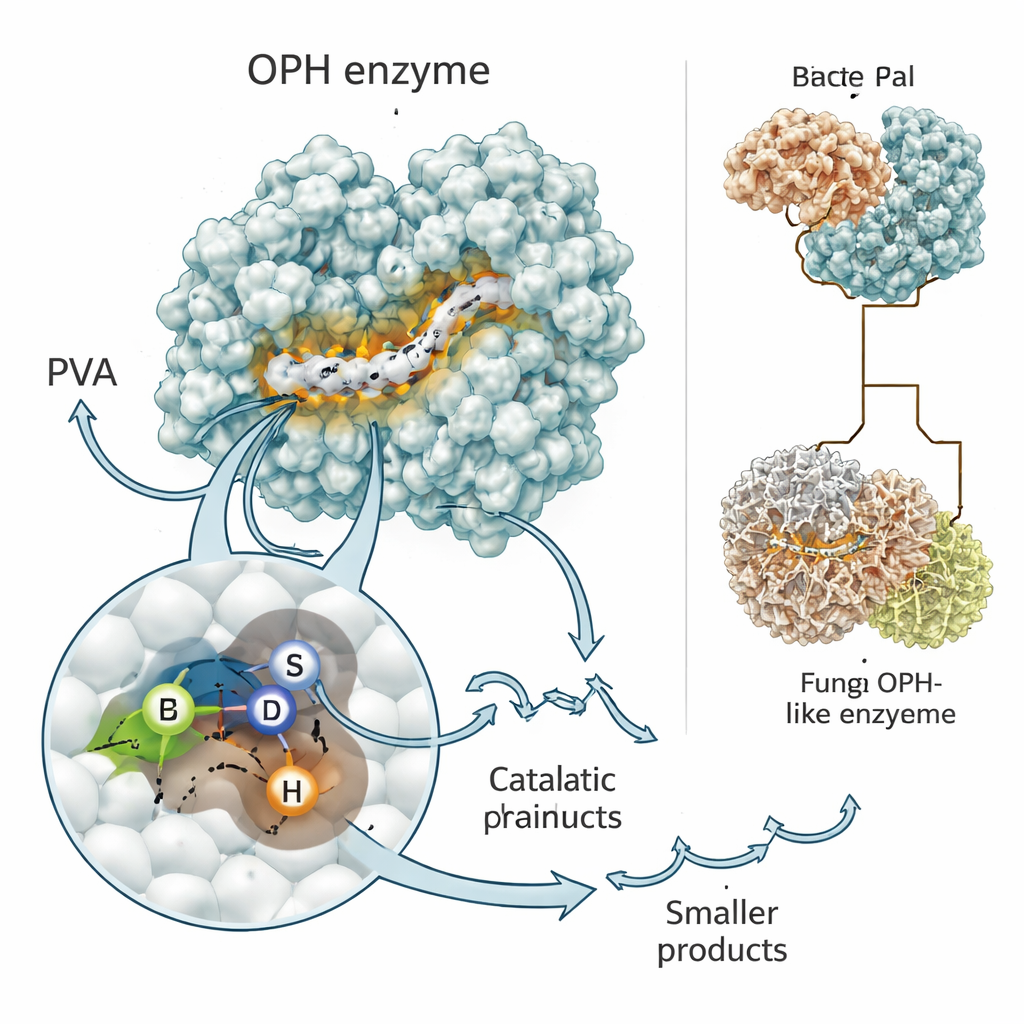
Signale, Schalter und evolutionäre Wendungen
Das Team untersuchte außerdem, welche Bereiche des Enzyms für seine Funktion im Bakterium absolut notwendig sind. Ein Abschnitt nahe dem N‑Termin des Proteins wirkt wie ein Postleitzahl-Code und leitet das Enzym aus der Zelle nach außen, wo das PVA‑Polymer liegt. Ein anderer Abschnitt enthält das aktive Motiv, das die Kohlenstoff‑Kohlenstoff‑Bindungen des Kunststoffs greift und spaltet. Als die Wissenschaftler Genversionen konstruierten, denen entweder das Signalsegment oder das aktive Motiv fehlte, produzierte das Bakterium zwar weiterhin RNA von dem Gen, konnte PVA aber nicht mehr effizient verdauen. Beim Vergleich mit vielen Bakterien und Pilzen fanden sie Verwandte dieses Enzyms, die dieselbe Kern‑„Schnitt“-Region teilen, sich aber in zusätzlichen Teilen unterscheiden — darunter eine auffällige Pilzversion, die die Schnittdomäne mit einem eingebauten Transporter verbindet und auf eine noch effizientere Import‑und‑Verdauungsstrategie in extremen Lebensräumen wie antarktischen Gesteinen hindeutet.
Was das für die Beseitigung von Plastikverschmutzung bedeutet
Für Nicht‑Fachleute ist die wichtigste Botschaft, dass Forscher verstehen, wie manche Mikroben einen vermeintlich biologisch abbaubaren Kunststoff abbauen, der sonst viel zu lange bestehen bleibt. Diese Studie identifiziert ein einzelnes Enzym, OPH aus S. rhizophila QL‑P4, als kraftvolle molekulare Schere, die unter milden Bedingungen arbeitet und einen entscheidenden Schritt beim PVA‑Abbau angreift. Durch das Verständnis seiner Struktur, seiner Arbeitsbedingungen und seiner evolutionären Verwandten können Forschende beginnen, bessere mikrobielle Stämme oder Enzymmischungen für Kläranlagen, industrielle Abwässer oder kontaminierte Böden zu entwickeln. Langfristig bringen solche Erkenntnisse uns näher an praktikable, biologiegestützte Lösungen zur Verwaltung von Kunststoffabfällen, anstatt sie in der Umwelt ansammeln zu lassen.
Zitation: Zhou, Y., Bold, N., Feng, J. et al. Mechanism and evolutionary divergence of a novel oxidized polyvinyl alcohol hydrolase in Stenotrophomonas rhizophila QL-P4. Sci Rep 16, 6411 (2026). https://doi.org/10.1038/s41598-026-37715-4
Schlüsselwörter: Polyvinylalkohol, Biodegradation, Plastikverschmutzung, mikrobielle Enzyme, Bioremediation