Clear Sky Science · de
Klassifizierung von Gliomen nach Lipidstoffwechsel
Warum Fette in Hirntumoren wichtig sind
Hirntumoren, die als Gliome bezeichnet werden, gehören zu den gefährlichsten Krebsarten; dennoch können Patientinnen und Patienten mit scheinbar derselben Diagnose sehr unterschiedliche Verläufe haben. Diese Studie stellt eine auf den ersten Blick einfache, aber weitreichende Frage: Wie beeinflusst die Art und Weise, wie Tumoren Fette – also Lipide des Körpers – nutzen, ihre Aggressivität, ihre Therapierbarkeit und unsere Fähigkeit, diese Unterschiede in Standard-Hirnuntersuchungen zu erkennen? Durch die Nachverfolgung des Lipidstoffwechsels in Hunderten von Tumoren decken die Autorinnen und Autoren verborgene Subtypen von Gliomen auf, die die Prognoseabschätzung und die Therapieplanung verändern könnten.
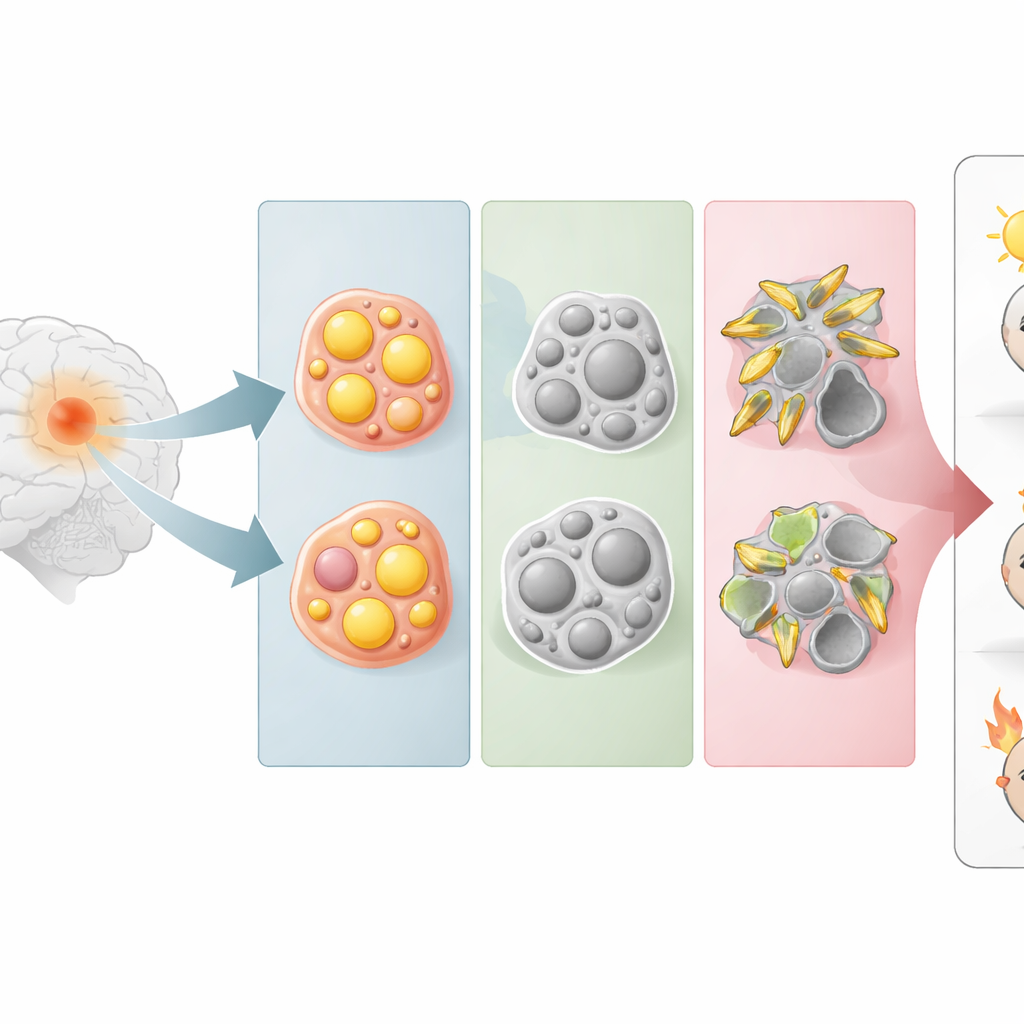
Drei verborgene Gesichter desselben Hirntumors
Anstatt sich von der mikroskopischen Zellgestalt leiten zu lassen, gruppierten die Forschenden Gliome nach der Stärke ihrer Aktivierung von fünf wichtigen Lipidwegen, einschließlich solcher für Steroidfette, Triglyceride und Sphingolipide (wichtige Bausteine von Zellmembranen). Anhand von Genaktivitätsprofilen aus großen öffentlichen Tumordatenbanken stellten sie fest, dass Gliome natürlicherweise in drei Gruppen fallen. Eine Gruppe setzte stark auf Steroidstoffwechsel (ST‑Typ), eine andere auf Triglyceridstoffwechsel (TC‑Typ) und eine dritte auf Sphingolipidstoffwechsel (SP‑Typ). Diese metabolischen Einteilungen verlaufen unabhängig von klassischen Tumorkategorien und zeigen, dass Zellen mit ähnlichen Lipidgewohnheiten in sonst unterschiedlich erscheinenden Gliomen vorkommen können.
Vom Stoffwechsel zur Patientenprognose
Die Forscherinnen und Forscher untersuchten dann, wie diese drei Fettnutzungsstile mit realen klinischen Ergebnissen zusammenhängen. Patientinnen und Patienten mit ST‑Typ‑Tumoren hatten im Allgemeinen die längste Überlebenszeit; ihre Tumoren waren häufiger niedriggradig und trugen bekannte günstige genetische Veränderungen. Am anderen Ende der Skala waren SP‑Typ‑Tumoren meist hochgradige Glioblastome ohne schützende Mutationen und traten häufiger bei älteren Patientinnen und Patienten auf. Selbst nach statistischer Anpassung für Tumorgrad und wichtige genetische Marker sagte die Zugehörigkeit zum SP‑Typ weiterhin eine deutlich schlechtere Prognose voraus, was darauf hindeutet, dass der Umgang des Tumors mit Sphingolipiden eine unabhängige Gefährdungsdimension erfasst, die Standardtests übersehen.
Eine feindliche Nachbarschaft im Gehirn
Bei tiefergehenden Analysen betrachteten die Autorinnen und Autoren die Tumormikroumgebung – das Gemisch aus Immunzellen, Blutgefäßen und Stützgewebe rund um den Krebs. SP‑Typ‑Tumoren zeigten eine überfüllte und konfliktgeladene Immunlandschaft, mit zugleich angreifenden und unterdrückenden Immunzellen und starken Signalen, die effektive Anti-Tumor‑Antworten dämpfen. Signalwege, die mit schnellem Zellwachstum, Invasion, Neubildung von Blutgefäßen, Vernarbung und Entzündung verbunden sind, waren in diesem Subtyp verstärkt aktiv. Abschätzungen zur Strahlenempfindlichkeit deuteten darauf hin, dass SP‑Typ‑Gliome am resistentesten gegen Strahlentherapie sind, was mit ihrem schlechteren Überleben übereinstimmt. Im Gegensatz dazu wirkten ST‑Typ‑Tumoren eher „ruhig“, mit niedrigeren Ausprägungen dieser aggressiven Merkmale.
Metabolismus des Tumors aus MRTs ablesen
Da die chirurgische Entnahme von Tumorgewebe invasiv ist und nicht immer möglich, prüften die Forschenden, ob Standard-Magnetresonanztomographie (MRT) Hinweise auf das Lipidverhalten eines Tumors liefern kann. Sie extrahierten mehr als zweitausend subtile Textur‑ und Formmerkmale aus zwei gängigen MRT-Sequenzen und trainierten ein Machine‑Learning‑Modell, um SP‑Typ von allen anderen Tumoren zu unterscheiden. Das Modell zeigte gute Leistung sowohl in einem klinikbasierten Trainingsdatensatz als auch in einem unabhängigen öffentlichen Validierungsdatensatz und separierte SP‑Typ‑Tumoren deutlich häufiger als im Zufallsfall. Dies legt nahe, dass der metabolische Fingerabdruck eines besonders aggressiven Gliomsubtyps auf routinemäßigen Hirnscans nachweisbare Spuren hinterlässt.
Ein Schlüsselfaktor im Zentrum eines aggressiven Netzwerks
Um von breiten Pathways zu konkreten Angriffspunkten zu gelangen, suchte das Team nach Genen, die zentral in lipidbezogenen Netzwerken stehen, in SP‑Typ‑Tumoren stark überaktiv sind, mit schlechterem Überleben verknüpft sind und SP‑Typ‑Tumoren zuverlässig von anderen unterscheiden. Drei Gene – GLA, GLB1 und HSD3B7 – erfüllten alle Kriterien. Alle waren in SP‑Typ‑Gliomen stärker aktiv und bildeten zusammen eine starke diagnostische Signatur. Die Autorinnen und Autoren konzentrierten sich auf HSD3B7, dessen Rolle bei Hirntumoren bislang weitgehend unerforscht war. Gewebeuntersuchungen von 100 Gliompatientinnen und -patienten zeigten, dass das HSD3B7‑Protein in fortgeschritteneren und bösartigeren Tumoren höher war und dass Patientinnen und Patienten mit hohen Proteinniveaus deutlich kürzer lebten.
Wie ein Lipidgen das Tumorökosystem umgestaltet
Einzelzellanalysen, die einzelne Zellen innerhalb von Tumoren profilieren, zeigten, dass HSD3B7 nicht nur in Krebszellen aktiv ist, sondern auch in mehreren Typen von Immun‑ und Stützzellen. Hohe Expressionswerte dieses Gens standen in Zusammenhang mit einem Netzwerk von Signalen, das Gefäßneubildung, chronische Entzündung und Immunflucht fördert. Die Kommunikation zwischen bestimmten schützenden Zelltypen schien geschwächt, während sich selbstverstärkende Schleifen innerhalb tumorunterstützender Zellen verstärkten. Zusammen deuten diese Muster darauf hin, dass erhöhte HSD3B7‑Aktivität eine feindliche Mikroumgebung schafft und erhält, die Tumorwachstum und Therapieresistenz begünstigt.
Was das für Patientinnen, Patienten und die zukünftige Versorgung bedeutet
Praktisch zeigt diese Arbeit, dass Gliome sinnvoll in drei lipidbasierte Subtypen unterteilt werden können, wobei der sphingolipiddominierte SP‑Typ als besonders gefährlich und therapieresistent hervorsticht. Diese Unterschiede sind nicht nur akademisch: Sie lassen sich mithilfe fortgeschrittener Bildanalyse aus routinemäßigen MRTs ablesen und lassen sich auf spezifische Gene wie HSD3B7 zurückführen, die potenziell zukünftige Arzneizielkandidaten sein könnten. Zwar sind weitere experimentelle Studien nötig, um zu prüfen, ob das Blockieren dieser Lipidwege Tumoren verlangsamen oder die Strahlentherapie verbessern kann, doch die Studie bietet eine neue metabolische Perspektive auf Hirnkrebs und bringt die Forschung einen Schritt näher zu stärker personalisierten, biologisch informierten Behandlungsentscheidungen.
Zitation: Tu, S., Zhang, P., Chi, X. et al. Lipid metabolism classification of gliomas. Sci Rep 16, 8219 (2026). https://doi.org/10.1038/s41598-026-37697-3
Schlüsselwörter: Gliom, Lipidstoffwechsel, Hirntumor-Bildgebung, Radiomics, Tumormikroumgebung