Clear Sky Science · de
Eine fettreiche Ernährung verändert die Genregulationsnetzwerke im präoptischen Areal
Warum Ihr Gehirn bei Diabetes eine Rolle spielt
Die meisten Menschen denken bei Diabetes an die Bauchspeicheldrüse und den Blutzucker, doch das Gehirn ist ebenfalls stark beteiligt. Diese Studie untersucht, wie eine fettreiche Ernährung und eine potente experimentelle Behandlung die Genaktivität in einer kleinen, aber wichtigen Hirnregion namens präoptisches Areal verändern. Indem die Forschenden kartieren, welche Gehirnzellen sich „zurücksetzen“, wenn Diabetes in Remission geht, hoffen sie, Wege zu neuen Therapien aufzuzeigen, die die körpereigene Fähigkeit des Gehirns nutzen, den Blutzucker mitzuverwalten.
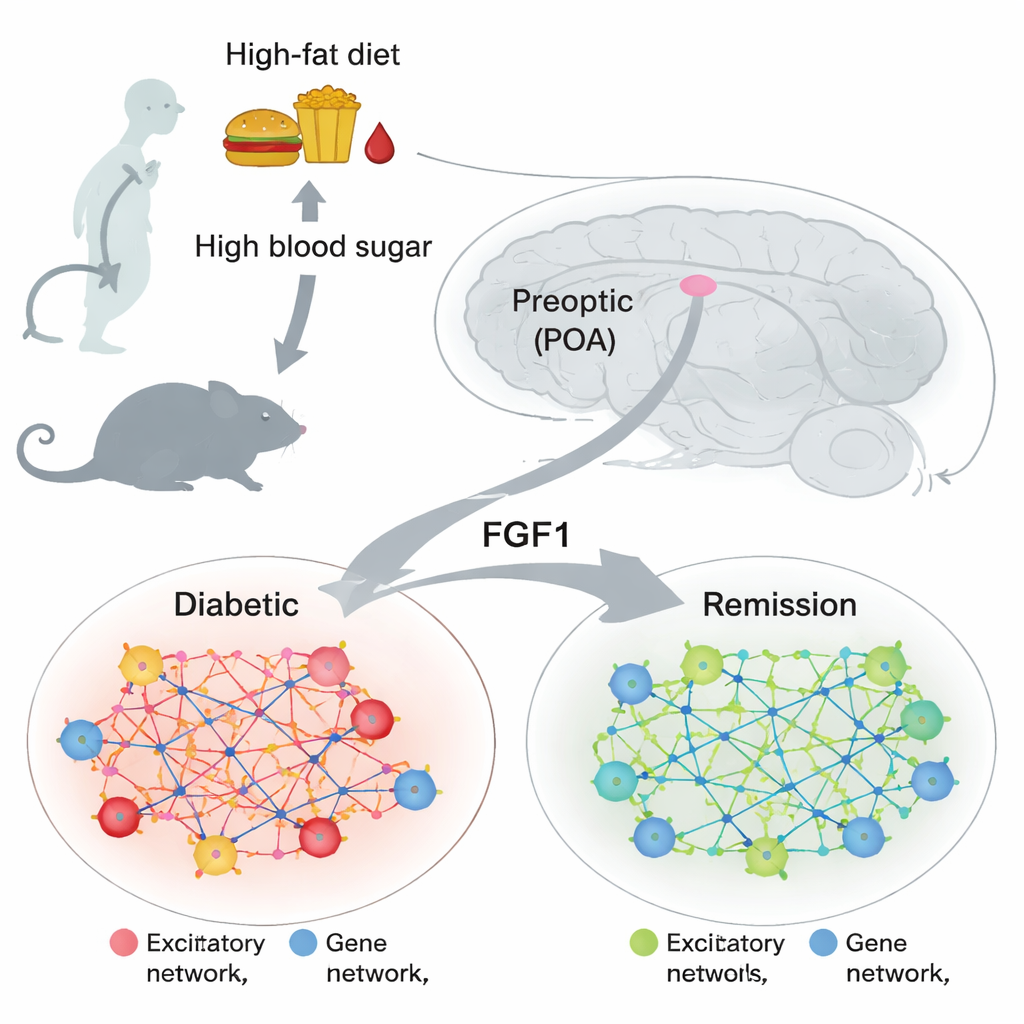
Ein kleines Hirnzentrum mit großer metabolischer Wirkung
Das präoptische Areal liegt vorn im Hypothalamus, einem Abschnitt des Gehirns, der die Körpertemperatur, den Schlaf, die Nahrungsaufnahme und hormonelle Signale reguliert. Frühere Arbeiten zeigten, dass Zellen in dieser Region beeinflussen können, wie der Körper Glukose verarbeitet und auf Wärme reagiert, doch ihre Rolle bei Diabetes war wenig verstanden. Gleichzeitig fanden andere Studien, dass eine Einzeldosis eines Proteins namens fibroblast growth factor 1 (FGF1), ins Gehirn verabreicht, adipöse diabetische Mäuse in eine langanhaltende Remission versetzen kann. Das warf eine zentrale Frage auf: Welche Gehirnzellen und Genprogramme ändern sich, wenn der Blutzucker normalisiert wird, und zeigen sich ähnliche Veränderungen im präoptischen Areal?
Genaktivität Zelle für Zelle lesen
Um das zu beantworten, nutzte das Team single-cell RNA-Sequenzierung, eine Technik, die misst, welche Gene in tausenden einzelner Zellen gleichzeitig aktiviert sind. Sie reanalysierten einen vorhandenen Datensatz von Mäusen, deren Diabetes nach FGF1-Behandlung in Remission gegangen war, und konzentrierten sich auf Nervenzellen im Hypothalamus. Mit statistischen Werkzeugen identifizierten sie Gruppen von Genen, die gemeinsam anstiegen oder sanken, als die Tiere vom diabetischen Zustand in die Remission übergingen. Diese „Remissionsmodule“ funktionieren wie Fingerabdrücke der Erholung: Statt ein einzelnes Gen zu verfolgen, erfassen sie koordinierte Verschiebungen über viele Gene hinweg in bestimmten Neuronentypen.
Fettreiche Ernährung, Gehirnzellen und gedrosselter Energieverbrauch
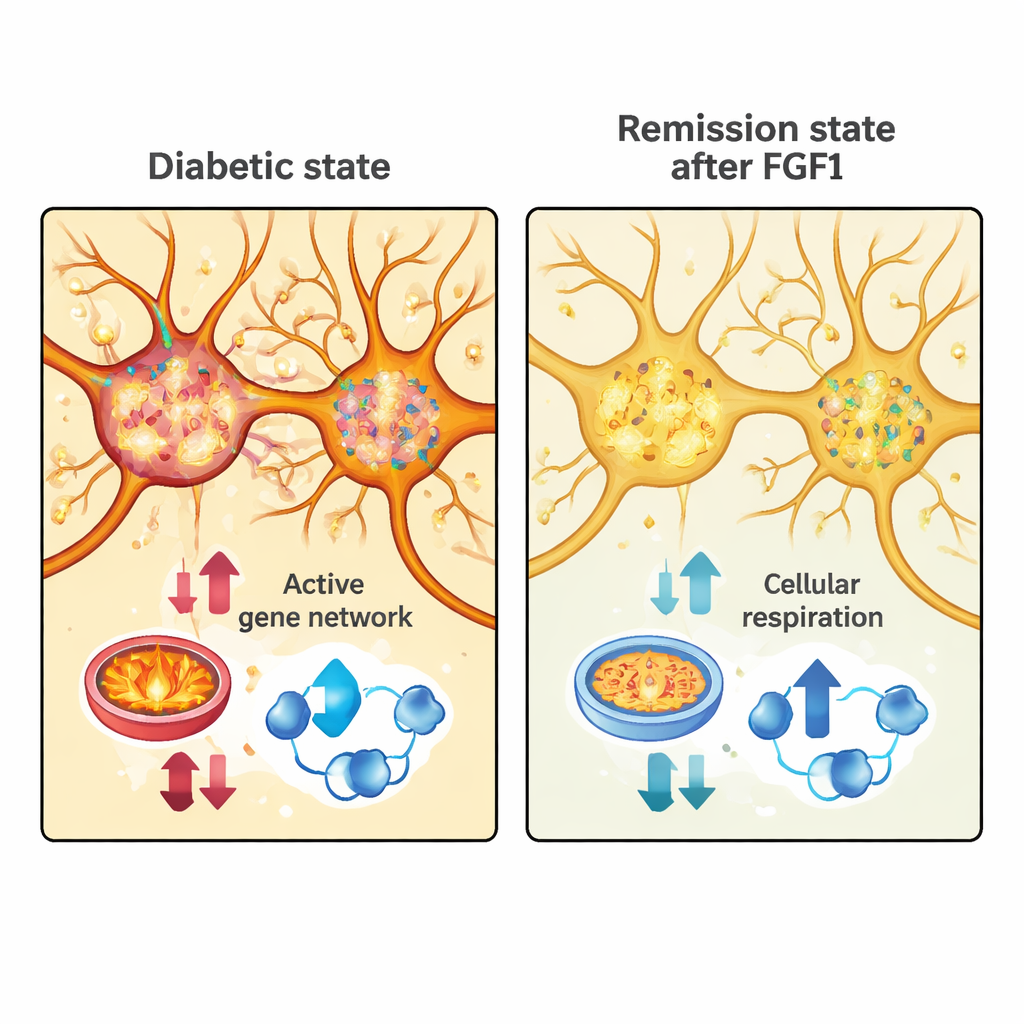
Die Forschenden verglichen diese Remissionsmodule anschließend mit der Genaktivität in einem anderen Datensatz, der Zellen aus dem präoptischen Areal normaler Mäuse erfasste. Zunächst teilten sie Neurone in zwei grobe Klassen: exzitatorische Zellen, die die Aktivität in ihren Schaltkreisen tendenziell erhöhen, und inhibitorische Zellen, die sie dämpfen. Bei diabetischen Mäusen, die mit FGF1 behandelt wurden, zeigten beide Neuronentypen weitreichende Reduktionen von Genen, die mit Energieproduktion verbunden sind – insbesondere solchen, die an der oxidativen Phosphorylierung, der zellulären Atmung und der mitochondrialen Maschinerie beteiligt sind, die aktive Zellen antreibt. In exzitatorischen Neuronen wurde ein großes „türkis“-Genmodul, das mit Energieverbrauch und synaptischer Aktivität verknüpft ist, in der Remission stark heruntergefahren, was darauf hindeutet, dass diese Zellen weniger metabolisch anspruchsvoll werden, wenn der Blutzucker kontrolliert wird.
Remissionssignaturen bestimmten Neuronengruppen zuordnen
Als Nächstes fragten die Forschenden, ob diese remissionsbezogenen Genmuster mit bestimmten Zellpopulationen im präoptischen Areal übereinstimmen. Durch das rechnerische Zusammenführen der beiden Datensätze fanden sie, dass einige präoptische Neuronencluster viele der gleichen Gene exprimierten, die sich bei der durch FGF1 ausgelösten Remission verändert hatten. Sie hoben mehrere Gene hervor – etwa Trpc4, Dgkg und Ryr3 –, die im Schnittpunkt dieser Analysen standen. Mit einer hochsensitiven Mikroskopiemethode namens RNAscope zeigten sie, dass diese Gene tatsächlich in definierten Zonen des präoptischen Areals von Mäusen exprimiert werden, vorwiegend in dorsalen Unterregionen. Das bestätigt sie als echte Marker spezifischer Neuronengruppen, die an der Gehirnantwort auf Stoffwechselerkrankungen beteiligt sein könnten.
Was das für künftige Diabetesbehandlungen bedeutet
Für Nichtfachleute ist die Quintessenz: Diabetes ist nicht nur ein Problem des Blutzuckers – es ist auch ein Problem neuronaler Netzwerke. Die Studie zeigt, dass, wenn Diabetes bei Mäusen in Remission geht, bestimmte präoptische Neurone in einen energieärmeren Zustand wechseln und ihre Genaktivität auf koordinierte Weise verändern. Indem die Arbeit diese Remissionsmodule definiert und sie mit konkreten Zelltypen und Markergenenn verknüpft, liefert sie eine Roadmap für künftige Experimente: Forschende können nun gezielt diese spezifischen Neurone ansprechen, um zu testen, wie sie die Glukosekontrolle, Adipositas und verwandte Komplikationen beeinflussen. Langfristig könnte ein besseres Verständnis dieser Hirnschaltungen helfen, Behandlungen zu entwickeln, die versagende Organe ergänzen oder umgehen, indem sie die eingebaute Kontrolle des Gehirns über den Stoffwechsel nutzen.
Zitation: Lazaro, O., Beimfohr, C., App, B. et al. High fat diet remodels the gene regulatory networks in the preoptic area. Sci Rep 16, 7042 (2026). https://doi.org/10.1038/s41598-026-37692-8
Schlüsselwörter: Gehirn und Diabetes, präoptisches Areal, fettreiche Ernährung, Gen-Netzwerke, FGF1-Remission