Clear Sky Science · de
Ganze-Transkriptom-Identifikation schädlicher Varianten in Kandidatengenen, die mit boviner Paratuberkulose in Verbindung stehen
Verborgene Gene hinter einer teuren Rinderkrankheit
Bovine Paratuberkulose, auch bekannt als Johne-Krankheit, schwächt still und leise die Gesundheit und Leistungsfähigkeit von Milchrinderbeständen weltweit, verursacht Landwirten jährlich Verluste in Höhe von mehreren hundert Millionen Dollar und weckt Bedenken wegen möglicher Zusammenhänge mit menschlichen Darmerkrankungen. Diese Studie blickt unter die genetische Haube von Holsteinkühen und stellt eine einfache, aber zentrale Frage: Welche genetischen Unterschiede könnten einigen Tieren helfen, dieser Infektion zu widerstehen, während andere daran zugrunde gehen? Indem die Forschenden die RNA — die arbeitenden Kopien der Gene — im Blut und im Darm lesen, verfolgten sie, wie subtile DNA-Veränderungen in Schlüsselgenen des Immunsystems den Krankheitsverlauf beeinflussen könnten.
Warum diese Rinderkrankheit wichtig ist
Paratuberkulose wird durch das Bakterium Mycobacterium avium Unterart paratuberculosis (MAP) verursacht. Kühe infizieren sich typischerweise früh im Leben, doch die Symptome treten oft erst Jahre später auf. In den stillen und subklinischen Stadien wirken die Tiere gesund, können jedoch geringe Mengen Bakterien ausscheiden und weniger Milch produzieren. In klinischen Stadien entwickeln sie chronischen Durchfall, starken Gewichtsverlust und erhebliche Einbußen bei der Milchleistung. Die Infektionsraten auf Bestandsniveau können in vielen Regionen, einschließlich Teilen Europas und Nordamerikas, über 50 % liegen, was ein wirtschaftliches wie auch ein Tierschutzproblem darstellt. Da das Bakterium auch als Umweltfaktor für menschliche Entzündungskrankheiten wie Morbus Crohn diskutiert wird, wächst der Druck, die Kontrollstrategien bei Rindern zu verbessern.
Das arbeitende Genom lesen
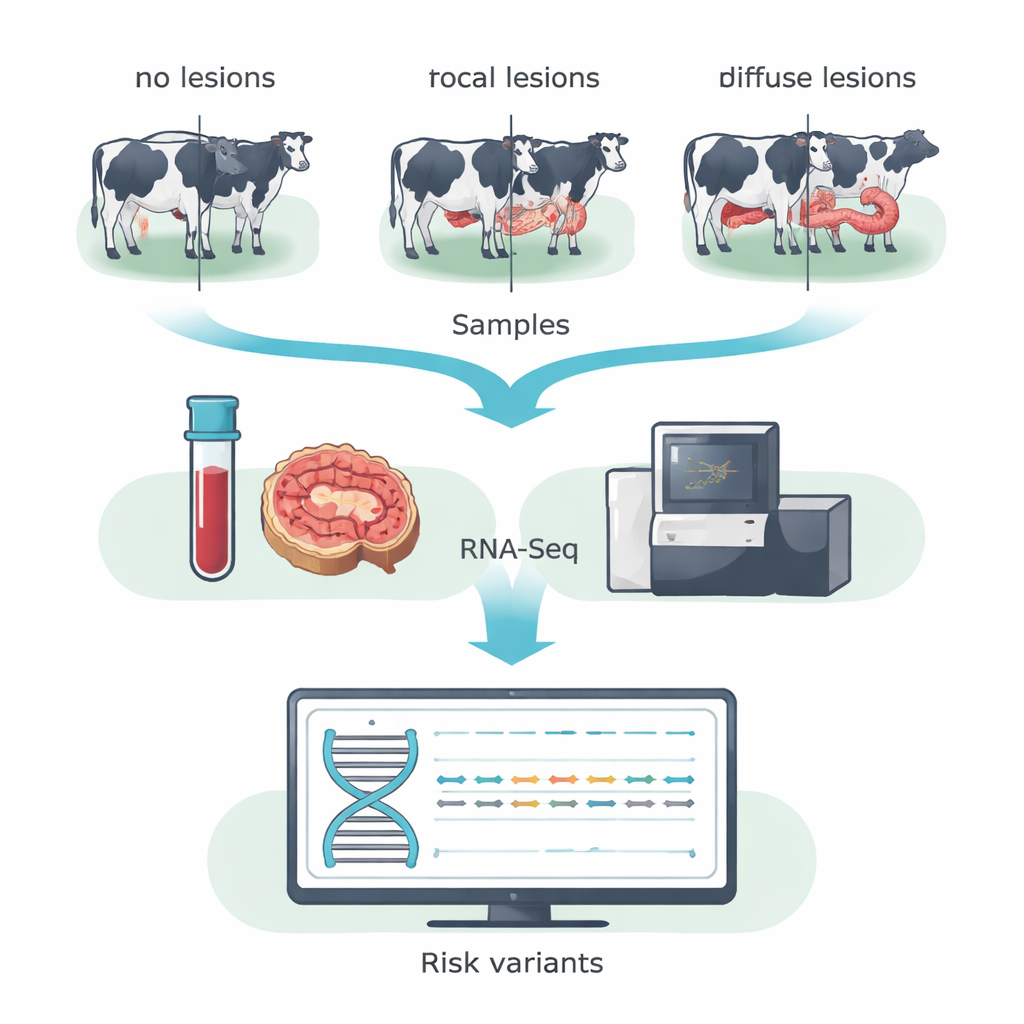
Anstatt die gesamte DNA-Sequenz zu scannen, nutzte das Team RNA-Sequenzierung (RNA-Seq), um sich auf Gene zu konzentrieren, die im Tier tatsächlich aktiv sind. Sie sammelten Blut und Proben von der Ileozäkalklappe — einem Darmbereich, der stark von MAP betroffen ist — von 14 Holsteinkühen aus einem spanischen Milchbetrieb. Auf der Grundlage mikroskopischer Untersuchungen des Darmgewebes wurden die Kühe in drei Kategorien eingeteilt: Tiere ohne nachweisbare Läsionen, Tiere mit kleinen, lokalisierten (fokalen) Läsionen, wie sie für lange subklinische Infektionen typisch sind, und Tiere mit schweren, weitverbreiteten (diffusen) Läsionen, die mit klinischer Krankheit einhergehen. Durch das Zusammenführen der Daten aus Blut und Darm innerhalb jeder Gruppe erhöhten die Forschenden ihre Fähigkeit, Einzelbuchstabenänderungen in exprimierten Genen — sogenannte kodierende SNPs — zu erkennen.
Schädliche Veränderungen in wichtigen Immungenen finden
Aus Hunderttausenden von Varianten konzentrierte sich das Team auf solche, die die Proteinsequenz verändern und voraussichtlich die Proteinfunktion schädigen — sogenannte deleterische Varianten. Sie wendeten strenge Filter an, um hohe Zuverlässigkeit zu gewährleisten, und nutzten etablierte Vorhersagetools, um riskante Veränderungen zu kennzeichnen. Dieser Ausleseprozess ergab 31 derartige Varianten, die nur bei Kühen ohne Läsionen vorkamen, 15, die ausschließlich bei Kühen mit fokalen Läsionen gefunden wurden, und 31, die nur bei Kühen mit diffusen Läsionen auftraten. Viele dieser Varianten lagen in Genen, die steuern, wie Immunzellen Infektionen erkennen und beseitigen, den programmierten Zelltod regulieren und den Stoffwechsel steuern. Besonders auffällig war die BOLA-Genfamilie, die bovine Version des Haupthistokompatibilitätskomplexes Klasse II, die Immunzellen dabei hilft, bakterielle Fragmente T-Zellen zu präsentieren. Unterschiedliche potenziell schädliche Varianten in BOLA wurden in allen drei Kuhgruppen gefunden, was darauf hindeutet, dass spezifische BOLA-Formen Tiere in Richtung Resistenz, kontrollierte Infektion oder schädliche Entzündung neigen lassen könnten.
Von DNA-Varianten zu Krankheitswegen
Um zu verstehen, welche praktischen Folgen diese Genveränderungen haben könnten, untersuchten die Forschenden, welche biologischen Signalwege in den einzelnen Gruppen angereichert waren. Kühe ohne Läsionen zeigten veränderte Varianten in Genen, die mit Antigenverarbeitung, Vesikeltransport und intestinalem Immungleichgewicht verbunden sind, darunter BOLA, AP3B1 und CHGA. Diese Veränderungen könnten eine effiziente Verdauung von Bakterien innerhalb von Immunzellen und ein stabiles Darmmilieu fördern, das Schäden begrenzt. Bei Kühen mit fokalen Läsionen konzentrierten sich schädliche Varianten in Genen (ORMDL3 und KANK2), die den programmierten Zelltod abschwächen und den zellulären Stoffwechsel feinjustieren, was dem Wirt möglicherweise hilft, die Bakterienzahl während einer langen, subklinischen Phase gering zu halten. Bei Kühen mit diffusen Läsionen zeigten die betroffenen Gene auf überaktive Immunwege wie Th1/Th2-Zellendifferenzierung und Antigenpräsentation sowie auf Gallen- und Arzneimitteltransportwege. Hier könnten veränderte BOLA-Familiengene eine starke, mitunter selbstschädigende Entzündungsreaktion antreiben, ein Muster, das auch bei vielen menschlichen Autoimmun- und Entzündungskrankheiten beobachtet wird.
Anhaltspunkte für die Zucht widerstandsfähigerer Bestände
Über die Aufklärung, wie verschiedene genetische Varianten die Immunantwort auf MAP formen, hinaus verband die Studie diese riskanten Veränderungen mit bekannten Regionen des bovinen Genoms, die mit Gesundheitseigenschaften assoziiert sind, einschließlich der Anfälligkeit für Paratuberkulose und andere Infektionen. Obwohl diese Ergebnisse noch in größeren Beständen validiert werden müssen und derzeit nicht als alleinige diagnostische Marker verwendet werden können, bieten sie ein vielversprechendes Verzeichnis von Kandidatenvarianten und -genen. Einfach ausgedrückt legt die Arbeit nahe, dass einige Kühe Genvarianten tragen, die ihnen helfen, Infektionen still zu kontrollieren, während andere Varianten eine unkontrollierte Entzündung und schwere Krankheit begünstigen. Zukünftig könnten solche Informationen die selektive Zucht und genetische Tests unterstützen, um Bestände in Richtung größerer natürlicher Resistenz zu verschieben und dadurch sowohl wirtschaftliche Verluste als auch den Bedarf an intensiven Kontrollmaßnahmen zu verringern.
Zitation: Badia-Bringué, G., Lam, S., Cánovas, Á. et al. Whole-transcriptome identification of deleterious variants in candidate genes linked to bovine paratuberculosis. Sci Rep 16, 6243 (2026). https://doi.org/10.1038/s41598-026-37675-9
Schlüsselwörter: bovine Paratuberkulose, Genetik der Johne-Krankheit, Immunsystem von Milchrindern, RNA-Sequenzierung, Zucht auf Krankheitsresistenz