Clear Sky Science · de
Medizinische Bildgebung und Deep Learning für die Diagnose von Brustkrebs anhand histopathologischer Bilder nutzen
Warum Früherkennung wichtig ist
Brustkrebs ist weltweit eine der häufigsten krebsbedingten Todesursachen bei Frauen, doch die Prognose verbessert sich erheblich, wenn die Erkrankung früh erkannt wird. Ärztinnen und Ärzte stellen die Diagnose meist, indem sie sehr dünne Gewebeschnitte unter dem Mikroskop untersuchen – ein Verfahren, das als Histopathologie bezeichnet wird. Diese Bilder enthalten viele Informationen darüber, ob Zellen harmlos oder gefährlich sind, doch das Lesen ist zeitaufwändig und kann zwischen Spezialisten variieren. Diese Studie untersucht, wie moderne künstliche Intelligenz Pathologen dabei unterstützen kann, Brustkrebs schneller und konstanter zu erkennen und so Patientinnen schnellere Antworten und effektivere Behandlungsoptionen zu ermöglichen.
Ein genauerer Blick auf Gewebebilder
Unter dem Mikroskop trennt sich Brustgewebe nicht sauber in „gesund“ und „krebsartig“. Zellen überlappen, Färbungen variieren von Labor zu Labor, und subtile Veränderungen in Form oder Textur können lebenswichtige Bedeutung haben. Traditionelle computerunterstützte Systeme hatten mit dieser Komplexität zu kämpfen, weil Ingenieure die Merkmale, nach denen der Rechner suchen soll, von Hand definieren mussten – und kleine Änderungen in der Färbung oder Bildqualität sie aus dem Tritt bringen konnten. Deep Learning, ein Teilbereich der künstlichen Intelligenz, der Muster direkt aus Daten lernt, hat kürzlich die Bildinterpretation, auch bei medizinischen Scans, grundlegend verändert. Die Autorinnen und Autoren bauen auf diesem Fortschritt auf, um ein System zu entwerfen, das auf die unordentliche Realität von Brustgewebe-Schnitten zugeschnitten ist.
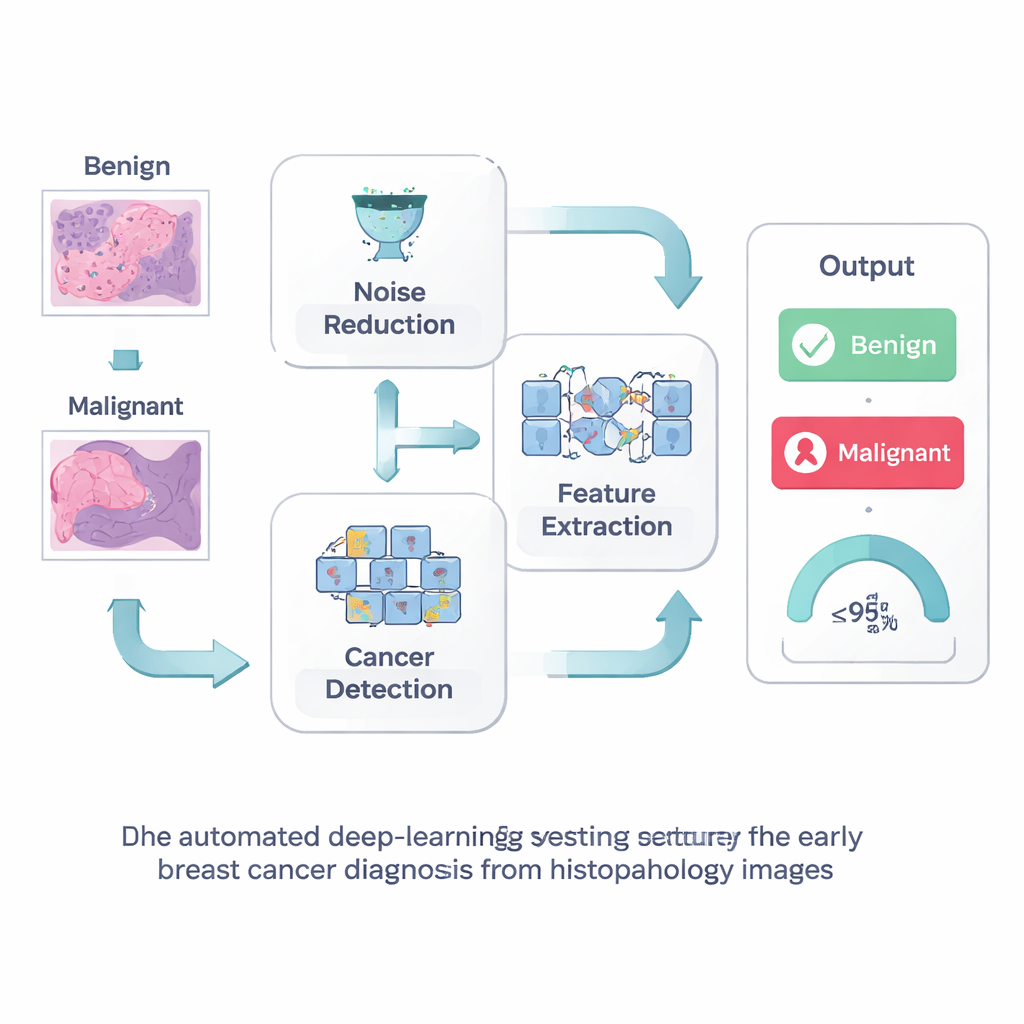
Das Bild vor dem Lesen bereinigen
Der erste Schritt ihres Ansatzes ist einfach, aber wirkungsvoll: das Bild säubern, bevor der Rechner es analysiert. Histopathologische Schnitte enthalten oft visuelles „Rauschen“ durch Färbung und Aufnahmeverfahren, das feine Strukturen verschleiern kann, die frühe Krebsanzeichen tragen. Die Forschenden verwenden eine Technik namens Wiener-Filterung, die zufällige Sprenkel glättet und gleichzeitig scharfe Kanten und winzige Details wie Zellgrenzen und kleine Zellverbände erhält. Indem ein klareres Bild vorgelegt wird, hilft dieser Schritt, sowohl übersehene Krebserkrankungen als auch Fehlalarme zu vermeiden, die Patientinnen zu unnötigen Untersuchungen schicken könnten.
Dem Computer beibringen, worauf er achten soll
Als Nächstes setzen die Forscherinnen und Forscher ein ausgereiftes Deep-Learning-Modell namens SE-ResNet ein, um die bereinigten Bilder zu analysieren. Vereinfacht gesagt scannt dieses Modell den Schnitt Stück für Stück und baut nach und nach ein internes „Vokabular“ visueller Muster auf: wie normale Gänge aussehen, wie Tumorzellen sich zusammenlagern und wie sich Texturen verändern, wenn der Krebs aggressiver wird. Ein eingebauter Aufmerksamkeitsmechanismus hilft dem Netzwerk, die informativsten Bildkanäle hervorzuheben und irrelevanten Hintergrund abzuschwächen. Das macht das Modell empfindlicher für subtile, krankheitsbezogene Muster und hält gleichzeitig den Rechenaufwand niedrig genug, dass es auf realer Krankenhaushardware laufen könnte.
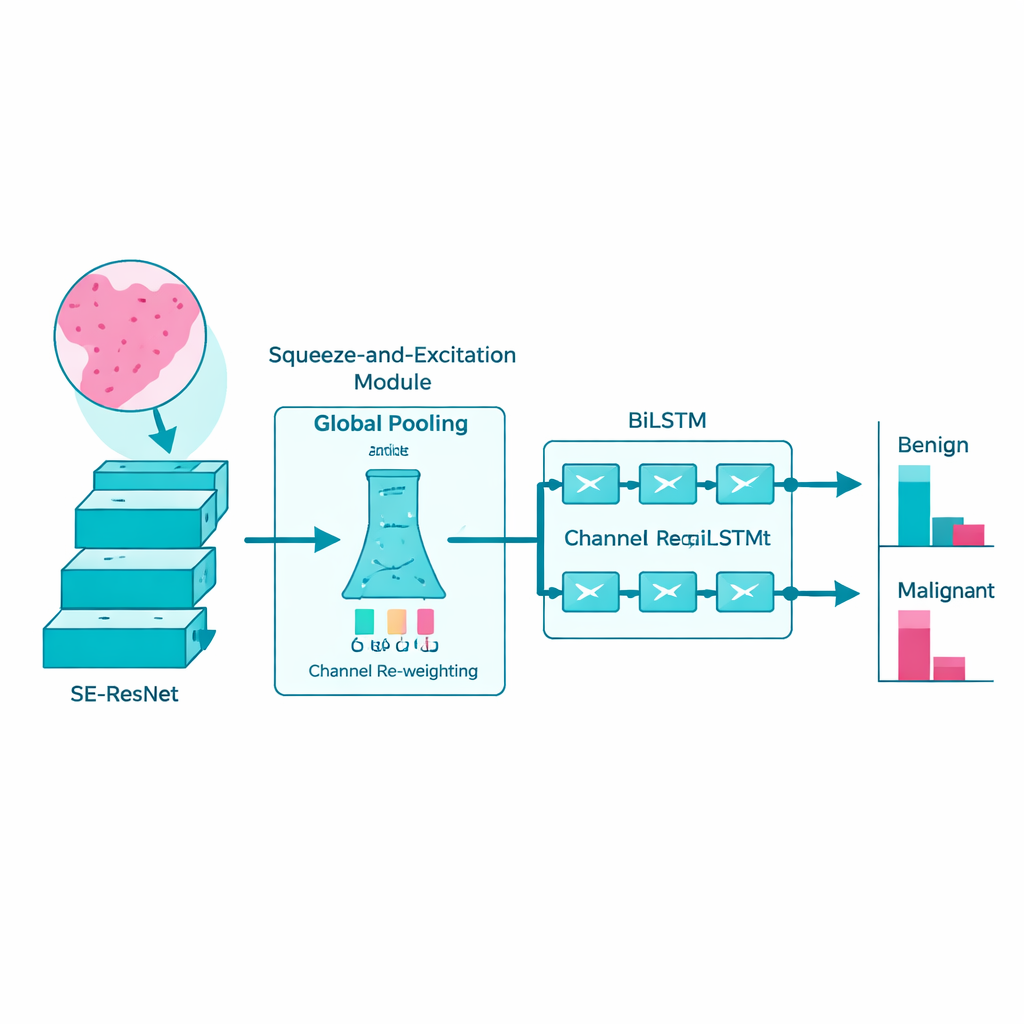
Muster räumlich wie eine Geschichte folgen
Anstatt jeden Bildausschnitt als isolierte Momentaufnahme zu behandeln, erkennen die Forschenden, dass sich Krankheitsanzeichen oft wie eine Geschichte über den Schnitt hinweg entfalten. Um dies zu erfassen, führen sie die von SE-ResNet extrahierten Merkmale in ein bidirektionales Long Short-Term Memory-Netzwerk, kurz BiLSTM. Dieser Modelltyp ist darauf ausgelegt, Sequenzen zu verstehen: Er betrachtet, wie sich Muster von einer Region zur nächsten verändern, vorwärts und rückwärts, ähnlich wie beim Lesen eines Satzes in beide Richtungen, um seine volle Bedeutung zu erfassen. Durch das Lernen dieser räumlichen Beziehungen wird das BiLSTM besser darin, gutartige Veränderungen von wirklich bösartigen zu unterscheiden.
Wie gut das System in der Praxis funktioniert
Die Autorinnen und Autoren testeten ihre gesamte Pipeline – Rauschreduzierung, Merkmalslernen und Sequenzmodellierung – an großen öffentlichen Sammlungen von Brustgewebebildern, darunter das häufig verwendete BreakHis-Dataset. Sie teilten die Daten in Trainings- und Testgruppen in unterschiedlichen Verhältnissen auf und verglichen ihre Methode mit vielen etablierten Deep-Learning-Modellen. In diesen Experimenten klassifizierte ihr System gutartige gegen bösartige Proben in nahezu 99 % der Fälle korrekt und übertraf konkurrierende Methoden bei gleichzeitig höherer Geschwindigkeit. Das Modell blieb über verschiedene Vergrößerungen des Gewebes hinweg robust, was darauf hindeutet, dass es sich an unter unterschiedlichen Bedingungen vorbereitete Schnitte anpassen kann. Die Studie weist jedoch auch auf Einschränkungen hin: Die Datensätze sind noch moderat in der Größe, das Modell konzentriert sich auf eine einfache Zwei-Klassen-Entscheidung statt auf detaillierte Tumoruntertypen, und es wurde noch nicht in realen klinischen Arbeitsabläufen erprobt.
Was das für Patientinnen und Ärztinnen bedeutet
Für Laien lautet die Kernbotschaft: Computer werden deutlich besser darin, mikroskopische Bilder von Brustgewebe zu lesen und verdächtige Bereiche zu markieren. Das vorgeschlagene System ersetzt die Pathologin bzw. den Pathologen nicht; vielmehr fungiert es wie eine besonders aufmerksame Assistenz, die Regionen hervorhebt, die wahrscheinlich krebsartig sind, und eine sehr genaue Zweitmeinung liefert. Wenn es in größeren und vielfältigeren Patientengruppen validiert wird, könnten solche Werkzeuge die Zeit bis zur Diagnose verkürzen, die Wahrscheinlichkeit verringern, dass ein kleiner Krebs übersehen wird, und überlasteten Kliniken helfen, steigende Fallzahlen zu bewältigen. Zukünftige Arbeiten müssen die Methode an noch unterschiedlicheren Schnitten testen und in den Alltag der Labore integrieren, aber diese Studie zeigt, dass sorgfältig entworfene Deep-Learning-Systeme ein starker Verbündeter im Kampf gegen Brustkrebs sein können.
Zitation: Nagalakshmi, V., Ahammad, S.H. Leveraging medical imaging and deep learning for diagnosis of breast cancer using histopathological images. Sci Rep 16, 6236 (2026). https://doi.org/10.1038/s41598-026-37663-z
Schlüsselwörter: Brustkrebsdiagnose, histopathologische Bilder, Deep Learning, medizinische Bildgebung, computerassistierte Detektion