Clear Sky Science · de
Typ-I-Interferon-Signalgebung definiert eine neuartige Krankheitssignatur in menschlichen Keratinozyten mit Xeroderma pigmentosum C
Warum Sonnenlicht für manche Menschen so gefährlich sein kann
Für die meisten von uns bedeutet Sonnenlicht Wärme und Vitamin D. Für Menschen mit einer seltenen genetischen Erkrankung namens Xeroderma pigmentosum C (XP-C) kann schon mäßiges Tageslicht jedoch schwere Hautschäden und ein extrem erhöhtes Hautkrebsrisiko auslösen. Diese Studie geht über das bekannte Problem der gestörten DNA-Reparatur bei XP-C hinaus und legt eine verborgene Ebene überaktiver, immunähnlicher Signalgebung in ihren Hautzellen offen, die neue Hinweise darauf liefert, warum ihre Haut nach Sonnenexposition so anfällig und entzündet ist.
Wenn die DNA-Reparatur in der Haut versagt
Unsere Hautzellen reparieren ständig DNA-Schäden, die durch ultraviolette B-(UVB)-Strahlung der Sonne entstehen. Ein Protein namens XPC ist einer der ersten „Sensoren“, die UV-induzierte Läsionen erkennen und ein großes Reparaturteam aktivieren. Bei XP-C zerstören Mutationen im XPC-Gen diesen Frühwarnschritt, sodass sich UV-Schäden anhäufen, anstatt behoben zu werden. Patienten mit XP-C entwickeln Tausende Male häufiger Hautkrebs als die Allgemeinbevölkerung und müssen Sonnenlicht rigoros meiden. Während dieser Defekt in der DNA-Reparatur gut bekannt ist, war viel weniger klar, wie er die internen Kommunikationswege der Zellen — insbesondere die, die die Entzündung steuern — umprogrammiert.
Signalwege in den Zellen zeitlich verfolgen
Um dieses Problem anzugehen, erzeugten die Forschenden menschliche Keratinozyten — die Hauptzellen der äußeren Hautschicht —, die vollständig auf XPC verzichteten, und verglichen sie mit ansonsten identischen normalen Zellen. Beide Zelltypen wurden einer sorgfältig gewählten, realitätsnahen UVB-Dosis ausgesetzt, die einer mäßigen Sonnenbranddosis ähnelt. Danach untersuchten sie die Zellen in zwei Stadien. Eine Stunde nach Bestrahlung erfassten sie die Aktivität zahlreicher Enzyme, sogenannter Protein-Tyrosin-Kinasen, die Signale durch Anfügen kleiner Phosphatgruppen ein- und ausschalten. Vierundzwanzig Stunden später nutzten sie hochauflösende Massenspektrometrie, um einen breiten Überblick über Tausende Proteine zu gewinnen und zu sehen, welche in ihrer Menge zu- oder abnahmen. Dieser zweistufige Ansatz erlaubte es, sowohl die frühen „Alarmglocken“ als auch die späteren „nachgelagerten Reaktionen“ innerhalb der Zellen nachzuvollziehen.
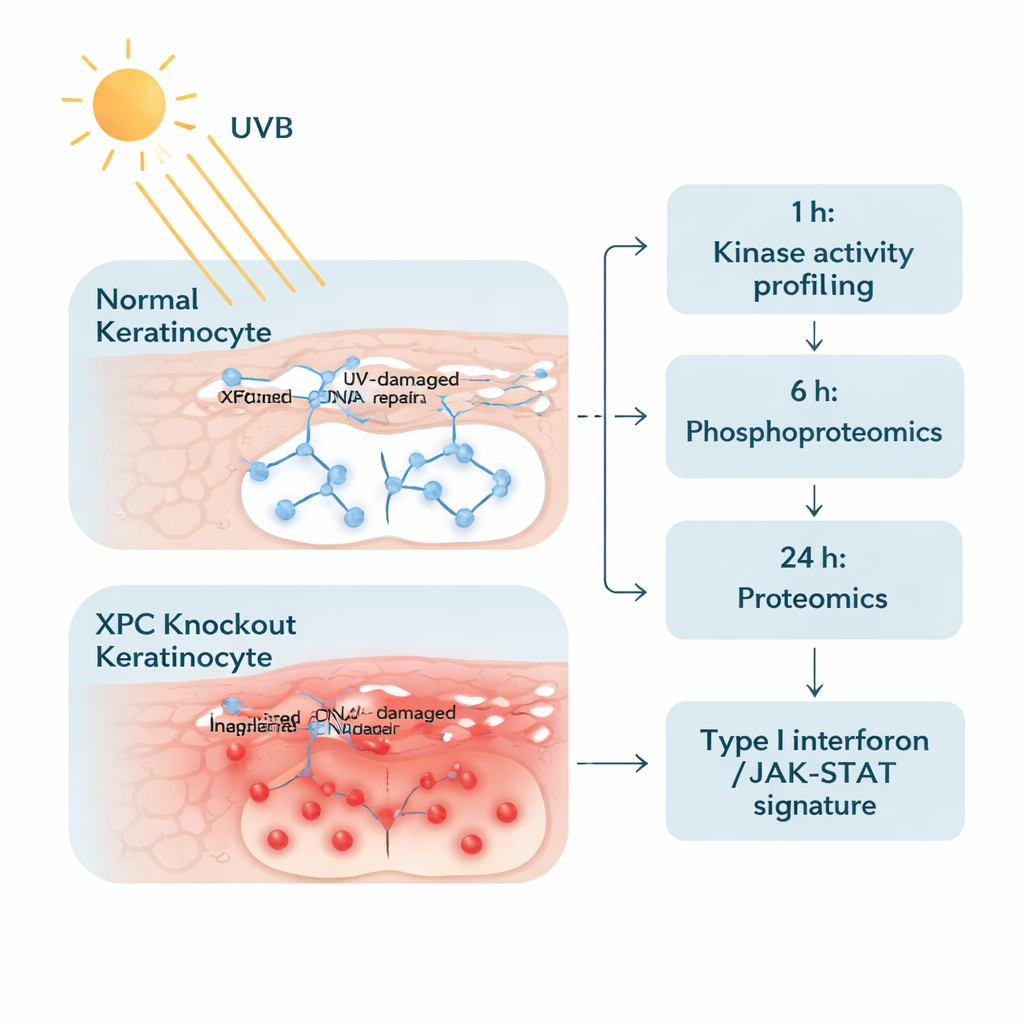
Ein entzündlicher Signalweg wird aktiv
Das frühe Kinase-Screening zeigte, dass XPC-defiziente Keratinozyten auf UVB mit einer Welle von Phosphorylierungen an mehr als hundert Stellen reagieren im Vergleich zu normalen Zellen. Auffällig war, dass viele dieser Veränderungen im JAK/STAT-Signalweg gruppiert waren — einer zentralen Kommunikationsroute, die normalerweise von Immunboten wie Interferonen genutzt wird. Marker, die mit JAK1, JAK2, JAK3, TYK2 und STAT-Proteinen verknüpft sind, waren in XP-C-Zellen bereits vor der UVB-Exposition aktiver und nach der Bestrahlung weiter verstärkt. Das deutet darauf hin, dass die Zellen in einem „hohen Alarmzustand“ vorgeprimt sind und bereit, Entzündungsbotschaften zu verstärken, sobald sie auf UV-induzierten Stress treffen.
Interferonartige Alarmgene in Hautzellen
Die spätere, breitere Proteomanalyse bestätigte und erweiterte dieses Bild. In XPC-Knockout-Zellen, besonders nach UVB, waren Hunderte von Proteinen verändert, und ein großer Cluster entsprach Genen, die normalerweise durch Typ-I-Interferone eingeschaltet werden — dieselben antiviralen Signale, mit denen der Körper Infektionen bekämpft. Proteine wie MX1, MX2, IFIT1, IFIT2, IFIT3, ISG15, OAS1 und IRF9, klassische „Interferon-aktivierte Gene“, waren stark erhöht. Netzwerk- und Pfadanalyse verknüpften diese Proteine mit JAK/STAT- und Typ-I-Interferon-Signalgebung als dominierendem Thema. Nachfolgende Western-Blot-Experimente bestätigten, dass Schlüssel-STAT-Proteine stärker phosphoryliert waren und dass diese interferonresponsiven Proteine in XP-C-Zellen viel stärker produziert wurden als in normalen Keratinozyten — sowohl im Ruhezustand als auch besonders nach UVB.
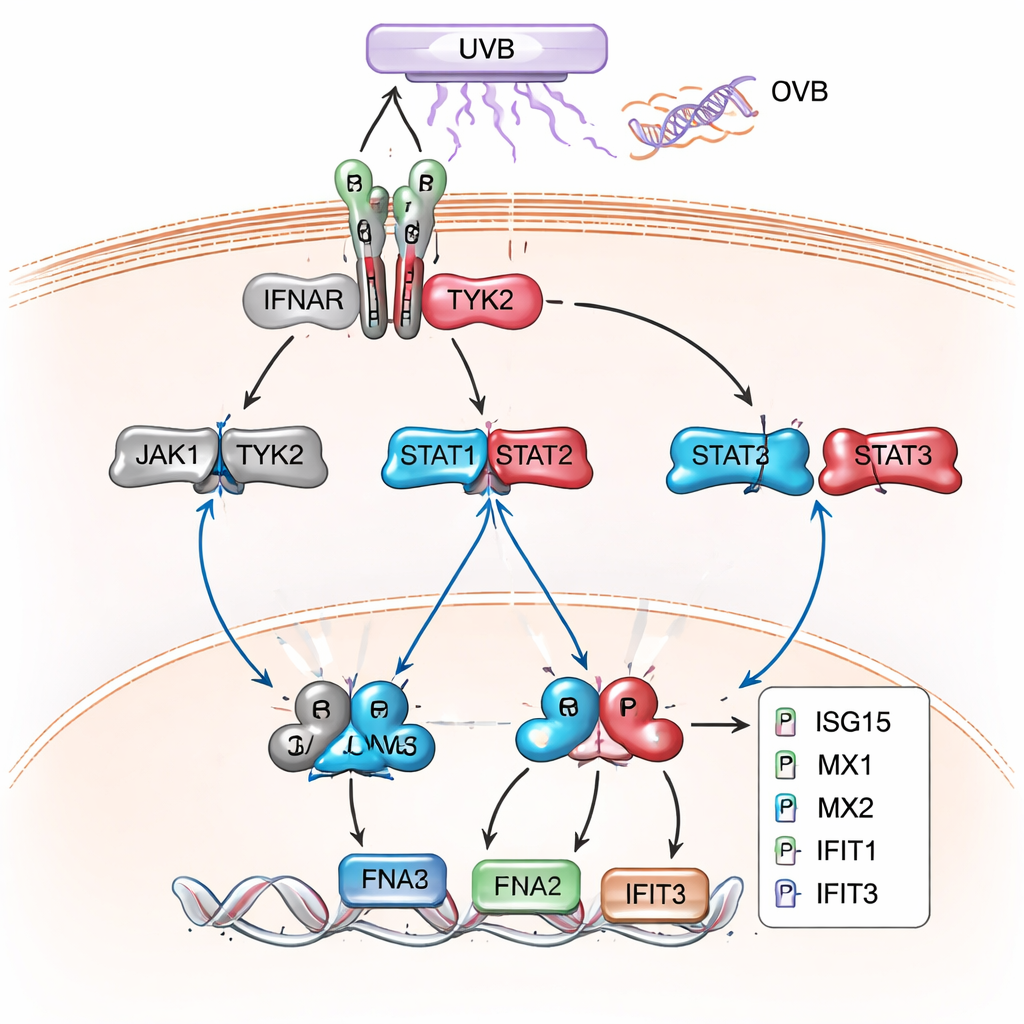
Was das für Patientinnen, Patienten und künftige Therapien bedeutet
In der Summe zeigen diese Ergebnisse, dass XP-C nicht nur eine Krankheit fehlerhafter DNA-Reparatur ist; sie ist auch durch einen anhaltenden, interferonähnlichen Entzündungszustand in Hautzellen gekennzeichnet, der über den JAK/STAT-Weg vermittelt und durch UV-Licht verstärkt wird. Für Laien bedeutet das: XP-C-Keratinozyten verhalten sich, als ob sie ständig gegen eine unsichtbare Infektion kämpften, sobald sie Sonnenlicht ausgesetzt sind, wodurch chronische Entzündung auf nicht reparierte DNA-Schäden auflagert. Zwar testet die Studie keine Therapien direkt, doch sie wirft die Möglichkeit auf, dass sorgfältig abgestimmte Medikamente, die JAK/STAT oder verwandte Entzündungskreisläufe hemmen, eines Tages helfen könnten, UV‑ausgelöste Schäden bei XP-C zu verringern — und möglicherweise auch bei anderen entzündlichen Hauterkrankungen, die dieses molekulare Signaturbild teilen.
Zitation: Nasrallah, A., Rezvani, HR., Belmudes, L. et al. Type I interferon signaling defines a novel disease signature in xeroderma pigmentosum C human keratinocytes. Sci Rep 16, 6559 (2026). https://doi.org/10.1038/s41598-026-37662-0
Schlüsselwörter: xeroderma pigmentosum, Hautkrebs, DNA-Reparatur, Interferon-Signalgebung, JAK-STAT-Signalweg