Clear Sky Science · de
Nichtlineare fraktionale stochastische Verzögerungsmodellierung und rechnerische Analyse der Dynamik des Herpes-simplex-Virus Typ II
Warum dieses Virus weiterhin wichtig ist
Genitalherpes, meist verursacht durch das Herpes-simplex-Virus Typ II (HSV‑II), betrifft weltweit Hunderte Millionen Menschen. Sobald das Virus aufgenommen ist, bleibt es in der Regel lebenslang im Körper, schlägt unvorhersehbar wieder auf und kann sich still verbreiten, auch wenn keine Bläschen sichtbar sind. Dieses Papier beschreibt kein neues Medikament oder einen Impfstoff; stattdessen nutzt es fortgeschrittene Mathematik und Computersimulationen, um besser zu verstehen, wie sich HSV‑II in einer Bevölkerung ausbreitet und welche Kontrollstrategien dazu beitragen könnten, es einzudämmen.
Den Ausbruch in einfache Gruppen zerlegen
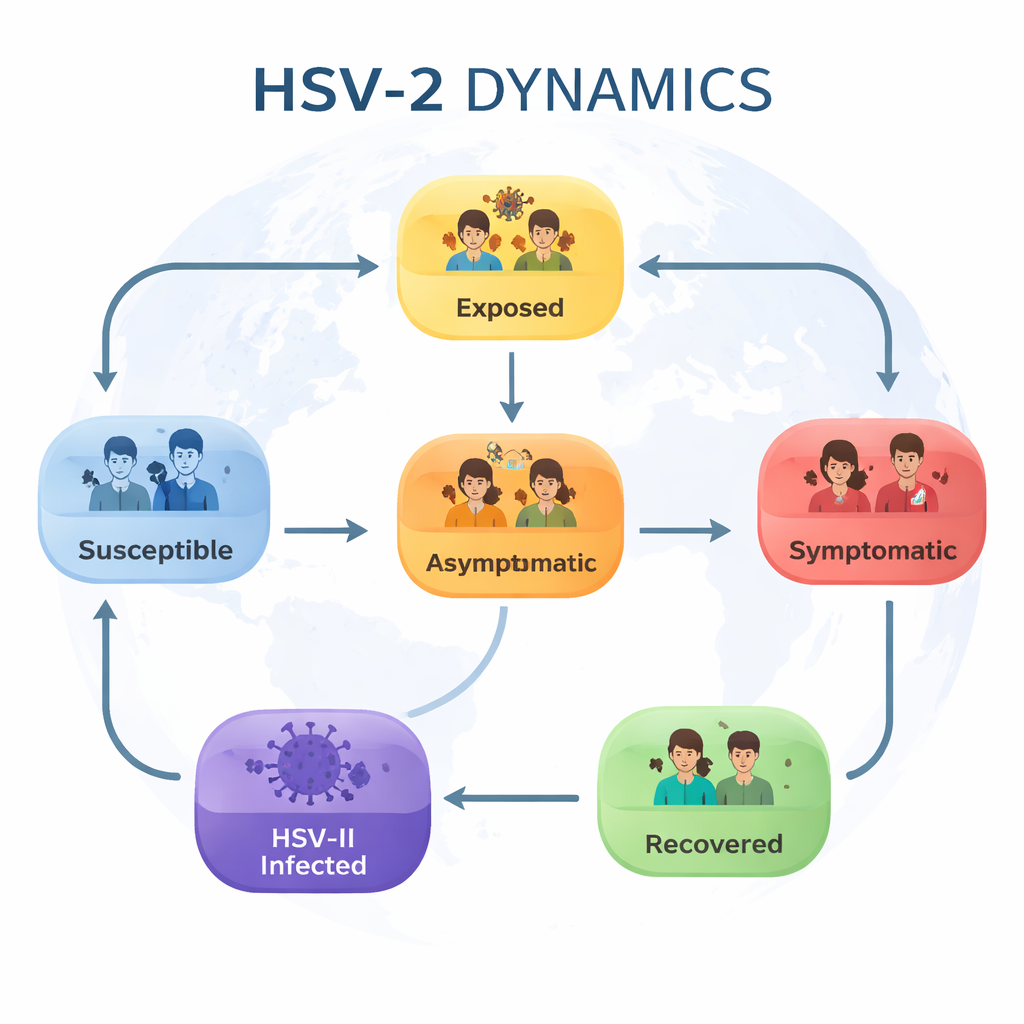
Die Autoren beginnen damit, die Bevölkerung in sechs Gruppen zu unterteilen, die die Hauptstadien einer HSV‑II-Infektion erfassen: Personen, die noch anfällig sind (suszeptibel), jene, die kürzlich infiziert, aber noch nicht ansteckend sind (exponiert), Menschen, die das Virus ohne Symptome tragen (asymptomatisch), Personen mit offensichtlichen Symptomen wie Genitalgeschwüren (symptomatisch), Individuen mit etablierter HSV‑II-Infektion und Menschen, die sich für eine Zeit erholt haben. Anschließend beschreiben sie, wie Menschen zwischen diesen Gruppen wechseln: sich durch Kontakt infizieren, von stiller zu symptomatischer Infektion übergehen, eine Behandlung erhalten, genesen oder temporären Schutz verlieren und wieder anfällig werden.
Erinnerung, Verzögerung und Zufälligkeit hinzufügen
Echte Infektionen folgen keinen perfekten, mechanischen Regeln, und das Modell spiegelt das wider. Zunächst enthält es einen eingebauten „Erinnerungseffekt“: die vergangene Infektionsgeschichte beeinflusst das aktuelle Verhalten und die Immunität, sodass das System nicht sofort vergisst, was zuvor geschah. Zweitens gibt es eine explizite Zeitverzögerung zwischen Infektion und Ansteckungsfähigkeit, die Inkubationszeiten und verzögerte Immunantworten widerspiegelt. Drittens erlaubt das Modell zufällige Schwankungen, wie zufällige Kontakte oder variable Immunstärke, indem sorgfältig gestaltete Rauschterme hinzugefügt werden. Zusammen erzeugen diese Merkmale ein reichhaltigeres und realistischeres Bild davon, wie sich HSV‑II über Monate und Jahre verhält, anstatt eine perfekt glatte Epidemiekurve anzunehmen.
Eine einzelne Zahl, die Gefahr signalisiert
Ein zentrales Ergebnis der Analyse ist die Basisreproduktionszahl, oft als R0 geschrieben. Diese einzelne Zahl fasst im Mittel zusammen, wie viele neue Infektionen eine ansteckende Person in einer überwiegend nicht infizierten Population verursacht. Liegt R0 unter 1, neigen Ausbrüche dazu, abzuflauen; liegt sie über 1, kann sich die Infektion etablieren und fortbestehen. Die Autoren zeigen, dass ihr HSV‑II-System zwei wesentliche Gleichgewichtszustände hat: einen, in dem das Virus verschwindet, und einen, in dem es langfristig vorhanden bleibt. Indem sie untersuchen, wie R0 von Kontaktquoten, dem Anteil stummer Fälle, Genesungsgeschwindigkeiten und Sterbe- oder Entferungsraten abhängt, identifizieren sie die Stellhebel, die am wichtigsten sind, um das System von Persistenz hin zur Eliminierung zu kippen.
Das Modell im Computer testen
Um diese Ideen numerisch zu untersuchen, entwickelt das Team ein spezielles Rechenschema, das die zugrundeliegende Biologie nachbildet, selbst wenn relativ große Zeitschritte verwendet werden. Dieser nichtstandardmäßige Ansatz stellt sicher, dass simulierte Populationsgrößen nie negativ werden und in realistischen Grenzen bleiben. Durch das Ausführen des Modells unter vielen Einstellungen verfolgen sie, wie sich die Zahlen von Suszeptiblen, Exponierten, Asymptomatischen, Symptomatischen, Infizierten und Genesenen im Laufe der Zeit ändern. Sie stellen beispielsweise fest, dass stärkere Erinnerungseffekte eine niedriggradige, schwelende Infektion verlängern können, während längere Verzögerungen epidemische Spitzen verschieben und strecken. Ihre Sensitivitätsberechnungen zeigen, dass die Erhöhung übertragungsbezogener Parameter R0 ansteigen lässt, während schnellere Genesung oder Entfernung R0 senken, womit aufgezeigt wird, wo Präventions- und Behandlungsmaßnahmen am effektivsten sind.
Was das für die alltägliche Gesundheit bedeutet
Für Nichtfachleute lautet die Botschaft dieser Arbeit: Die Zukunft von HSV‑II in einer Gemeinschaft ist kein reines Schicksal. Indem man sorgfältig modelliert, wie Menschen verschiedene Stadien der Infektion durchlaufen, und Verzögerungen, anhaltende Immuneffekte und Zufallsereignisse berücksichtigt, bauen die Autoren ein Werkzeug, das „Was-wäre-wenn“-Szenarien testen kann, bevor man sie in der realen Welt ausprobiert. Ihre Ergebnisse deuten darauf hin, dass die Reduzierung von Übertragungsmöglichkeiten und die Verbesserung von Behandlung und Genesung den Erreger gemeinsam in Richtung Ausrottung innerhalb einer Bevölkerung treiben können. Während diese Studie kein sofortiges Heilmittel bietet, liefert sie einen robusten Rahmen für die Gestaltung klügerer Strategien im öffentlichen Gesundheitsschutz, die Bewertung potenzieller Impfstoffe und letztlich die Verringerung der langfristigen Belastung durch Genitalherpes.
Zitation: Raza, A., Alsulami, M., Lampart, M. et al. Nonlinear fractional stochastic delay modeling and computational analysis of herpes simplex virus type II dynamics. Sci Rep 16, 7009 (2026). https://doi.org/10.1038/s41598-026-37658-w
Schlüsselwörter: Genitalherpes, HSV-2-Übertragung, mathematische Modellierung, stochastische Dynamik, fraktionaler Verzögerungsgrad